| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Гипонитрит | |||
| Систематическое название ИЮПАК Диазенебис (олат) | |||
| Другие имена Гипонитрит (2–) | |||
| Идентификаторы | |||
3D модель ( JSmol ) |
| ||
| 3DMet | |||
| ЧЭБИ | |||
| ChemSpider |
| ||
| 130273 | |||
| КЕГГ | |||
PubChem CID | |||
| |||
| |||
| Характеристики | |||
| N 2О2- 2 | |||
| Молярная масса | 60,012 г · моль -1 | ||
| Конъюгированная кислота | Азотная кислота | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
В химии , hyponitrite может относиться к анионной N
2О2-
2([ON = NO] 2− ), или к любому ионному соединению, которое его содержит. В органической химии он может также относиться к группе -O-N = N-O- или любому органическому соединению с общей формулой R 1 -O-N = N-O-R 2 , где R 1 и R 2 являются органические группы. [1] Такие соединения можно рассматривать как соли и сложные эфиры соответственно азотистой кислоты H
2N
2О
2 или HON = NOH.
Кислоты hyponitrite представляет собой ионное соединение с анионом HN
2О-
2([HON = NO] - ).
Гипонитрит-ион [ править ]
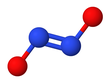
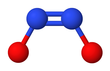
Гипонитрит проявляет цис-транс-изомерию . [2]
Транс ( Е ) форма , как правило , находится в hyponitrite солей , таких как hyponitrite натрия ( Na
2N
2О
2) и гипонитрита серебра (I) ( Ag
2N
2О
2).
Также может быть получена цис ( Z ) форма гипонитрита натрия, и она более реактивна, чем транс- форма. [2] цис hyponitrite анион почти плоские и почти симметрично, с длиной около 140 м для N-O связи и 120 часов для N-N св зь, и O-N-N углов от около 119 °. [3]
Реакции [ править ]
Ионы гипонитрита могут действовать как бидентатный лиганд либо в мостиковом, либо в хелатирующем режиме. В красной биядерной форме хлорида нитрозилпентамминкобальта (III), [Co (NH 3 ) 5 NO] Cl 2, имеется мостиковая цис- гипонитритная группа . [4]
Гипонитрит может действовать как восстанавливающий агент, например, восстанавливающий йод : [4]
- N
2О2-
2+ 3 я
2+ 3 часа
2O → НЕТ-
3+ НЕТ-
2 + 6 привет
Эфиры гипонитрита [ править ]
Органические транс- гипонитриты R 1 -O-N = N-O-R 2 могут быть получены реакцией транс- гипонитрита серебра (I) Ag
2N
2О
2с различными алкилгалогенидами . Например, реакция с трет- бутилхлоридом дает транс- ди- трет- бутилгипонитрит. [5] [6] [7] [8]
Другие алкильные радикалы, описанные в литературе, включают этил , [9] и бензил . [10] [11] [12] Эти соединения могут быть источником алкоксильных радикалов . [13]
См. Также [ править ]
Другие оксоанионы азота включают
- нитрат , NO-
3 - нитрит , NO-
2 - пероксонитрит , (пероксинитрит), OONO -
- пероксонитрат , HNO-
4 - триоксодинитрат , (гипонитрат), [ON = NO 2 ] 2–
- нитроксилат , [O 2 N-NO 2 ] 4-
- ортонитрат , НЕТ3-
4 - динитрамид , [O 2 N-N-NO 2 ] -
- нитрозилгипонитрит , [ONNONO] -
Ссылки [ править ]
- ^ MN Hughes (1968), «Гипонитриты». Ежеквартальные обзоры химического общества, том 22, выпуск 1, страницы 1–13. DOI : 10.1039 / QR9682200001 .
- ^ a b Эгон Виберг, Арнольд Фредерик Холлеман (2001) Неорганическая химия , Elsevier ISBN 0-12-352651-5
- ^ Клаус Фельдманн, Мартин Янсен (1996), « цис- гипонитрит натрия - новый препаративный путь и анализ кристаллической структуры». Angewandte Chemie International Edition на английском языке, том 35, выпуск 15, страницы 1728–1730. DOI : 10.1002 / anie.199617281 .
- ^ a b Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ Навамони Арулсами; Д. Скотт Боле; Джером А. Имониджи; Элизабет С. Саган (2000). «Корреляция геометрии структуры E / Z продукта и O / O по сравнению с O / N региоселективностью в диалкилировании гипонитрита». Варенье. Chem. Soc. 122 (23): 5539–5549. DOI : 10.1021 / ja994261o .
- ↑ Х. Кифер и Т. Г. Трейлор (1966), Tetrahedron Lett., Стр. 6163.
- ↑ RL Huang, TW Lee и SH Ong (1969), J. Chem. Soc. C, стр. 40.
- ^ RC Neuman и RJ Bussey (1970), J. Am. Chem. Soc., Том 92, стр. 2440.
- ^ JR Partington и CC Shah (1932), J. Chem. Soc., Стр. 2589.
- ^ JB Sousa и SK Ho (1961), J. Chem. Soc., Стр. 1788.
- ↑ JB Sousa и SK Ho (1960), Nature, том 186, стр. 776.
- ^ NH Ray (1960), J. Chem. Soc., Стр. 4023.
- ^ Крейг А. Огл; Стивен В. Мартин; Майкл П. Дзиобак; Марек В. Урбан; Дж. Дэвид Менденхолл (1983). «Скорости разложения, синтез и спектральные свойства ряда алкилгипонитритов». J. Org. Chem. 48 (21): 3728–3733. DOI : 10.1021 / jo00169a023 .