В области органической химии , А.Н. имид является функциональной группой , состоящей из двух ацильных групп , связанных с азотом . [1] Соединения структурно родственны ангидридам кислот , хотя имиды более устойчивы к гидролизу. С точки зрения коммерческого применения имиды наиболее известны как компоненты высокопрочных полимеров, называемых полиимидами . Неорганические имиды также известны как твердые или газообразные соединения, и имидогруппа (= NH) также может действовать как лиганд .
Номенклатура [ править ]
Большинство имидов представляют собой циклические соединения, производные от дикарбоновых кислот , и их названия отражают исходную кислоту. [2] Примерами являются сукцинимид , полученный из янтарной кислоты , и фталимид , полученный из фталевой кислоты . Для имидов, полученных из аминов (в отличие от аммиака), N -заместитель обозначен префиксом. Например, N-этилсукцинимид получают из янтарной кислоты и этиламина . Изоимиды изомеры с нормальными имидами и имеют формулу RC (O) OC (NR ') R ″. Часто они являются промежуточными продуктами, которые превращаются в более симметричные имиды. Органические соединения, называемыекарбодиимиды имеют формулу RN = C = NR. Они не имеют отношения к имидам.
Имиды дикарбоновых кислот [ править ]
В PubChem связь предоставляет доступ к дополнительной информации о соединениях, в том числе других имен, идентификаторы, токсичности и безопасности.
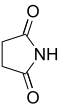
п Распространенное имя Систематическое название Структура PubChem исходная кислота структура 2 Сукцинимид Пирролидин-2,5-дион 
11439 Янтарная кислота 
2, ненасыщенные, цис-углерод-углеродные двойные связи Малеимид Пиррол-2,5-дион 
10935 Малеиновая кислота 
3 Глутаримид Пиперидин-2,6-дион 
70726 Глутаровая кислота 
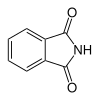
6 Фталимид Изоиндол-1,3-дион 
6809 Фталевая кислота
Свойства [ править ]
Обладая высокой полярностью, имиды хорошо растворяются в полярных средах. N – H-центр имидов, полученных из аммиака, является кислым и может участвовать в образовании водородных связей . В отличие от структурно родственных ангидридов кислот, они устойчивы к гидролизу, а некоторые из них даже могут перекристаллизовываться из кипящей воды.
Возникновение и применение [ править ]
Многие высокопрочные или электропроводящие полимеры содержат имидные субъединицы, то есть полиимиды . Одним из примеров является каптон, где повторяющееся звено состоит из двух имидных групп, полученных из ароматических тетракарбоновых кислот. [3] Другим примером полиимидов является полиглутаримид, который обычно получают из полиметилметакрилата (ПММА) и аммиака или первичного амина путем аминолиза и циклизации ПММА при высокой температуре и давлении, обычно в экструдере. Этот метод называется реактивной экструзией. Коммерческий полиглутаримидный продукт на основе метиламинного производного ПММА, названный Kamax, был произведен компанией Rohm and Haas. Прочность этих материалов отражает жесткость имидной функциональной группы.
Интерес к биоактивности имидсодержащих соединений был вызван ранним открытием высокой биоактивности циклогексимида как ингибитора биосинтеза белка в некоторых организмах. Талидомид , известный своими побочными эффектами, является одним из результатов этого исследования. Ряд фунгицидов и гербицидов содержат имидную функциональность. Примеры включают каптан , который при некоторых условиях считается канцерогенным, и процимидон . [4]
В 21 веке возник новый интерес к иммуномодулирующим эффектам талидомида, что привело к созданию класса иммуномодуляторов, известных как иммуномодулирующие имидные препараты (IMiD).
Подготовка [ править ]
Наиболее распространенные имиды получают путем нагревания дикарбоновых кислот или их ангидридов и аммиака или первичных аминов . Результатом является реакция конденсации : [5]
- (RCO) 2 O + R′NH 2 → (RCO) 2 NR ′ + H 2 O
Эти реакции протекают через амиды . Внутримолекулярная реакция карбоновой кислоты с амидом намного быстрее, чем межмолекулярная реакция, которая наблюдается редко.
Они также могут быть получены путем окисления амидов , особенно если исходить из лактамов . [6]
- R (CO) NHCH 2 R '+ 2 [O] → R (CO) N (CO) R' + H 2 O
Определенные имиды также могут быть получены в результате перегруппировки изоимида в имид Mumm .
Реакции [ править ]
Для имидов, полученных из аммиака, N – H-центр является слабокислым. Таким образом, соли имидов щелочных металлов могут быть получены с использованием обычных оснований, таких как гидроксид калия. Основанием, сопряженным с фталимидом, является фталимид калия . Эти анионы можно алкилировать с образованием N- алкилимидов, которые, в свою очередь, могут разлагаться с высвобождением первичного амина. На стадии высвобождения используются сильные нуклеофилы, такие как гидроксид калия или гидразин .
Обработка имидов галогенами и основанием дает N -галогенпроизводные. Примеры , которые являются полезными в органическом синтезе являются N - хлорсукцинимидом и N - бромсукцинимид , которые соответственно служат в качестве источников «Cl + » и «Br + » в органическом синтезе .
Имиды в координационной химии [ править ]
В координационной химии имидокомплексы переходных металлов содержат лиганд NR 2- . В некоторых отношениях они похожи на оксолиганды. В некоторых случаях угол MNC составляет 180 °, но часто угол явно изогнут. Исходный имид (NH 2- ) является промежуточным продуктом фиксации азота синтетическими катализаторами. [7]
Ссылки [ править ]
- ^ "Имидес" . Сборник химической терминологии ИЮПАК . 2009. DOI : 10,1351 / goldbook.I02948 . ISBN 978-0-9678550-9-7.
- ^ Мартынов, А.В. (2005-12-06). «Новый подход к синтезу имидов транс-аконитовой кислоты». ХимИнформ . 36 (49): нет. DOI : 10.1002 / chin.200549068 . ISSN 1522-2667 .
- ^ Уолтер У. Райт и Майкл Халлден-Аббертон "Полиимиды" в Энциклопедии промышленной химии Ульмана , 2002, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a21_253
- ^ Питер Акерманн, Пол Марго, Франц Мюллер «Фунгициды, сельскохозяйственные» в Энциклопедии промышленной химии Ульмана , 2002, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a12_085
- ^ Винсент Родескини, Найджел С. Симпкинс и Фенчжи Чжанги (2009). «Иллюстративное образование имида из амина и ангидрида» . Органический синтез .CS1 maint: несколько имен: список авторов ( ссылка ); Коллективный том , 11 , с. 1028
- ↑ Сперри, Джонатан (27 сентября 2011 г.). «Окисление амидов до имидов: мощное синтетическое преобразование». Синтез . 2011 (22): 3569–3580. DOI : 10,1055 / с-0030-1260237 .
- ^ Ньюджент, Вашингтон; Майер, Дж. М., "Множественные связи металл-лиганд", J. Wiley: New York, 1988.
- ^ Hazari, N .; Маунтфорд, П., "Реакции и применение имидо-комплексов титана", Acc. Chem. Res. 2005, 38, 839-849. DOI : 10.1021 / ar030244z
Внешние ссылки [ править ]
- ИЮПАК: имиды