 | |
 | |
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC (2 Z ) -Бут-2-ендиовая кислота | |
| Другие имена ( Z ) -бутендиовая кислота; цис- бутендиовая кислота; Маленовая кислота; Малеиновая кислота; Токсиловая кислота | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| 3DMet | |
| 605762 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.003.403 |
| Номер ЕС |
|
| 49854 | |
| КЕГГ | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| С 4 Н 4 О 4 | |
| Молярная масса | 116,072 г · моль -1 |
| Внешность | Белое твердое вещество |
| Плотность | 1,59 г / см³ [1] |
| Температура плавления | 135 ° C (275 ° F, 408 K) (разлагается) [2] |
| 478,8 г / л при 20 ° C [2] | |
| Кислотность (p K a ) | p k a1 = 1,9 p k a2 = 6,07 [3] |
Магнитная восприимчивость (χ) | -49,71 · 10 −6 см 3 / моль |
| Опасности | |
| Паспорт безопасности | Паспорт безопасности материалов от JT Baker |
| Пиктограммы GHS | |
| Сигнальное слово GHS | Предупреждение |
Формулировки опасности GHS | H302 , H315 , H317 , H319 , H335 |
Меры предосторожности GHS | Р261 , Р264 , Р270 , Р271 , P272 , P280 , P301 + 312 , P302 + 352 , Р304 + 340 , P305 + 351 + 338 , P312 , P321 , P330 , P332 + 313 , P333 + 313 , P337 + 313 , P362 , P363 , P403 + 233 , P405 , P501 |
| NFPA 704 (огненный алмаз) |  0 3 0 |
| Родственные соединения | |
Родственные карбоновые кислоты | фумаровая кислота янтарная кислота кротоновая кислота |
Родственные соединения | малеиновый ангидрид малеимид |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
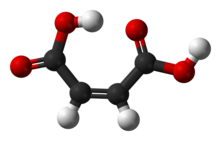
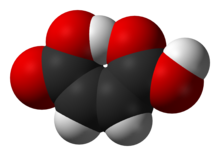
Малеиновая кислота или цис- бутендиовая кислота - это органическое соединение, которое представляет собой дикарбоновую кислоту , молекулу с двумя карбоксильными группами. Его химическая формула: HO 2 CCH = CHCO 2 H или C 4 H 4 O 4 . Малеиновая кислота представляет собой цис- изомер бутендиовой кислоты, тогда как фумаровая кислота является транс- изомером. Он в основном используется в качестве предшественника фумаровой кислоты, и по сравнению с исходным малеиновым ангидридом малеиновая кислота имеет мало применений.
Физические свойства [ править ]
Малеиновая кислота имеет теплоту сгорания -1,355 кДж / моль, [4] на 22,7 кДж / моль выше, чем у фумаровой кислоты. Малеиновая кислота более растворима в воде, чем фумаровая кислота . Температура плавления малеиновой кислоты (135 ° C) также намного ниже, чем у фумаровой кислоты (287 ° C). Оба свойства малеиновой кислоты можно объяснить за счет внутримолекулярной водородной связи [5], которая происходит в малеиновой кислоте за счет межмолекулярных взаимодействий, и которые невозможны в фумаровой кислоте по геометрическим причинам.
Производство и промышленное применение [ править ]
В промышленности, малеиновой кислоты получают путем гидролиза из малеинового ангидрида , причем последний получают путем окисления из бензола или бутана . [6]
Малеиновая кислота - это промышленное сырье для производства глиоксиловой кислоты путем озонолиза . [7]
Малеиновая кислота может быть использована для образования кислотно-аддитивных солей с лекарствами, чтобы сделать их более стабильными, такими как индакатерол малеат.
Малеиновая кислота также используется в качестве усилителя адгезии для различных субстратов, таких как нейлон и металлы с цинковым покрытием, например оцинкованная сталь, в клеях на основе метилметакрилата.
Изомеризация в фумаровую кислоту [ править ]
Основное промышленное использование малеиновой кислоты - ее преобразование в фумаровую кислоту . Это превращение, изомеризация , катализируется различными реагентами, такими как минеральные кислоты и тиомочевина . Опять же, большая разница в растворимости в воде облегчает очистку фумаровой кислоты.
Изомеризация является популярной темой в школах. Малеиновая кислота и фумаровая кислота не превращаются самопроизвольно, потому что вращение вокруг двойной углерод-углеродной связи не является энергетически выгодным. Однако преобразование цис- изомера в транс- изомер возможно путем фотолиза в присутствии небольшого количества брома . [8] Свет превращает элементарный бром в радикал брома , который атакует алкен радикальным присоединением.реакция на бромалкановый радикал; и теперь возможно вращение одинарной связи. Радикалы брома рекомбинируют и образуется фумаровая кислота. В другом методе (используемом в качестве демонстрации в классе) малеиновая кислота превращается в фумаровую кислоту в процессе нагревания малеиновой кислоты в растворе соляной кислоты . Обратимое добавление (H + ) приводит к свободному вращению вокруг центральной связи CC и образованию более стабильной и менее растворимой фумаровой кислоты.
Некоторые бактерии производят фермент малеат-изомеразу , который используется бактериями в метаболизме никотината. Этот фермент катализирует изомеризацию фумарата и малеата.
Другие реакции [ править ]
Хотя малеиновая кислота не применяется на практике, она может быть превращена в малеиновый ангидрид путем дегидратации , в яблочную кислоту путем гидратации и в янтарную кислоту путем гидрирования ( этанол / палладий на угле ). [9] Он реагирует с тионилхлоридом или пентахлоридом фосфора с образованием хлорангидрида малеиновой кислоты (выделить хлорангидрид одноатомной кислоты невозможно). Малеиновая кислота, будучи электрофильной, участвует в качестве диенофила во многих реакциях Дильса-Альдера .
Maleates [ править ]
Малеат ион является ионизированной формой малеиновой кислоты. Ион малеата полезен в биохимии в качестве ингибитора трансаминазных реакций. Сложные эфиры малеиновой кислоты также называют малеатами, например диметилмалеат .
Использование в фармацевтических препаратах [ править ]
Многие препараты, содержащие амины , представлены в виде соли малеиновой кислоты , например карфеназин , хлорфенирамин , пириламин , метилэргоновин и тиэтилперазин .
См. Также [ править ]
- Фумаровая кислота
- Яблочная кислота
- Малоновая кислота
- Янтарная кислота
Ссылки [ править ]
- ^ Budavari, Susan, изд. (1996), Индекс Мерк: Энциклопедия химикатов, лекарств и биологических препаратов (12-е изд.), Мерк, ISBN 0911910123
- ^ a b Запись в базе данных веществ GESTIS Института безопасности и гигиены труда
- ^ Справочник CRC по химии и физике, 73-е изд .; CRC Press: Бока-Ратон, Флорида, 1993.
- ^ Малеиновый ангидрид, малеиновая кислота, фумаровая кислота и архивации 2013-11-02 в Wayback Machine , Huntsman нефтехимической корпорация
- ^ MN G Джеймс, GJ B Уильямс (1974). «Уточнение кристаллической структуры малеиновой кислоты» . Acta Crystallographica . B30 (5) (5): 1249–1275. DOI : 10.1107 / S0567740874004626 .
- ^ Курт Lohbeck, Герберт Haferkorn, Вернер Фурман и Норберт Fedtke "фумаровой кислот" в энциклопедии Ульмана промышленной химии, Wiley-VCH, Weinheim, 2000. DOI : 10.1002 / 14356007.a16_053
- ^ Производство глиоксиловой кислоты DSM. Архивировано 30 ноября 2005 г. в Wayback Machine.
- ^ Light изомеризация эксперимент архивация 2005-11-27 в Wayback Machine (из университета Регенсбурга , с видео)
- ^ Kwesi Amoa (2007). «Каталитическое гидрирование малеиновой кислоты при умеренных давлениях, лабораторная демонстрация». Журнал химического образования . 84 (12): 1948. DOI : 10.1021 / ed084p1948 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме малеиновой кислоты . |
- Международная карта химической безопасности 1186
- Калькулятор: активность воды и растворенных веществ в водном растворе малеиновой кислоты