Дикарбоновая кислота представляет собой органическое соединение , содержащее две карбоксильных функциональных групп (-СООН). Общая молекулярная формула дикарбоновых кислот может быть записана как HO 2 C-R-CO 2 H, где R может быть алифатическим или ароматическим. Как правило, дикарбоновые кислоты демонстрируют химическое поведение и реакционную способность, подобные монокарбоновым кислотам . Дикарбоновые кислоты также используются при получении сополимеров, таких как полиамиды и сложные полиэфиры . Наиболее широко используемой в промышленности дикарбоновой кислотой является адипиновая кислота , которая является прекурсором, используемым в производственейлон . Другие примеры дикарбоновых кислот включают аспарагиновую кислоту и глутаминовую кислоту , две аминокислоты в организме человека. Название может быть сокращено до дикислоты .
Линейные насыщенные дикарбоновые кислоты [ править ]
Общая формула HO
2C (CH
2)
пCO
2H . [1] PubChem ссылки предоставляет доступ к дополнительной информации о соединениях, в том числе других имен, идентификаторы, токсичности и безопасности.
п Распространенное имя Систематическое название ИЮПАК Структура pK a 1 pK a 2 PubChem 0 Щавелевая кислота этандиовая кислота 
1,27 4,27 971 1 Малоновая кислота пропандиовая кислота 
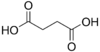
2,85 5,05 867 2 Янтарная кислота бутандиовая кислота 
4,21 5,41 1110 3 Глутаровая кислота пентандиовая кислота 
4,34 5,41 743 4 Адипиновая кислота гександиовая кислота 
4,41 5,41 196 5 Пимелиновая кислота гептандиовая кислота 
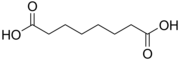
4,50 5,43 385 6 Субериновая кислота октандиовая кислота 
4,526 5,498 10457 7 Азелаиновая кислота нонандиовая кислота 4,550 5,498 2266 8 Себациновая кислота декандиовая кислота 4,720 5,450 5192 9 ундекандиовая кислота 15816 10 додекандиовая кислота 12736 11 Брассиловая кислота тридекандиовая кислота 10458 14 Тапсиновая кислота гексадекандиовая кислота 10459 19 Японская кислота генейкозадионовая кислота 9543668 20 Феллогеновая кислота докозандиовая кислота 244872 28 Эквизетоловая кислота триаконтандиовая кислота 5322010
Возникновение [ править ]
- Адипиновая кислота, несмотря на свое название (на латыни adipis означает жир), не является нормальным компонентом природных липидов, а является продуктом окислительной прогорклости . Впервые его получили окислением касторового масла ( рицинолевая кислота ) азотной кислотой. В настоящее время его производят в промышленных масштабах путем окисления циклогексанола или циклогексана , в основном для производства нейлона 6-6 . Он имеет несколько других промышленных применений в производстве клеев , пластификаторов , желатинизирующих агентов, гидравлических жидкостей , смазочных материалов , смягчающих веществ , пенополиуретана ,дубление кожи , уретан, а также в качестве подкислителя в пищевых продуктах.
- Пимелиновая кислота (греч. Pimelh , жир) также была впервые выделена из окисленного масла. Производные пимелиновой кислоты участвуют в биосинтезе лизина .
- Впервые субериновая кислота была получена путем окисления пробки азотной кислотой (лат. Suber). Эта кислота также образуется при окислении касторового масла. Субериновая кислота используется в производстве алкидных смол и в синтезе полиамидов ( варианты нейлона ).
- Название азелаиновой кислоты связано с действием азотной кислоты (азот, азот или азотная, азотная) окисления олеиновой кислоты или элаидиновой кислоты . Был обнаружен среди продуктов прогорклых жиров. Его происхождение объясняется его присутствием в плохо сохранившихся образцах льняного масла и в образцах мази, взятых из египетских гробниц возрастом 5000 лет. Азелаиновая кислота была получена окислением олеиновой кислоты перманганатом калия , но теперь окислительным расщеплением олеиновой кислоты хромовой кислотой или озонолизом. Азелаиновая кислота используется в виде простых эфиров или сложных эфиров с разветвленной цепью) при производстве пластификаторов (для винилхлоридасмолы, резина), смазки и консистентные смазки. Азелаиновая кислота сейчас используется в косметике (лечение прыщей). Он проявляет бактериостатические и бактерицидные свойства в отношении различных аэробных и анаэробных микроорганизмов, присутствующих на коже с акне. . Азелаиновая кислота была идентифицирована как молекула, которая накапливалась в повышенных количествах в некоторых частях растений, и было показано, что она способна повышать устойчивость растений к инфекциям. [2]
- Себациновая кислота, названная от кожного сала ( сала ). Тенар выделил это соединение из продуктов перегонки говяжьего жира в 1802 году. Его производят в промышленных масштабах путем деления касторового масла щелочью. [3] Себациновая кислота и ее производные имеют множество промышленных применений в качестве пластификаторов, смазок, масел для диффузионных насосов, косметики, свечей и т. Д. Она также используется в синтезе полиамида, как нейлон, и алкидных смол. Изомер, изосебациновая кислота, имеет несколько применений в производстве пластификаторов виниловой смолы, экструзионных пластиков, клеев, смазок на основе сложных эфиров, полиэфиров, полиуретановых смол и синтетического каучука .
- Брассиловая кислота может быть получена из эруковой кислоты путем озонолиза, но также с помощью микроорганизмов ( Candida sp. ) Из тридекана . Эта двухосновная кислота производится в Японии в небольших коммерческих масштабах для изготовления ароматизаторов. [4]
- Додекандиовая кислота используется в производстве нейлона (нейлон-6,12), полиамидов, покрытий, клеев, смазок, полиэфиров, красителей, моющих средств, антипиренов и ароматизаторов. В настоящее время он производится путем ферментации длинноцепочечных алканов со специфическим штаммом Candida tropicalis . [4] Травматическая кислота - ее мононенасыщенный аналог.
- Тапсиновую кислоту выделяли из сушеных корней средиземноморской «смертоносной моркови» Thapsia garganica ( Apiaceae ).
Японский воск представляет собой смесь триглицеридов дикарбоновых кислот C21, C22 и C23, полученных из дерева сумаха ( Rhus sp.).
Большой обзор дикарбоновых кислот, присутствующих в средиземноморских орехах, выявил необычные компоненты. [5] Всего было определено 26 второстепенных кислот (от 2 в пекане до 8% в арахисе): 8 видов, полученных из янтарной кислоты , вероятно, связанных с фотосинтезом , и 18 видов с цепочкой от 5 до 22 атомов углерода. Кислоты с более высоким весом (> C20) обнаруживаются в суберине, присутствующем на поверхности растений (внешняя кора, эпидермис корня). С16 по С26 a, ω-диовые кислоты считаются диагностическими для суберина. С C18: 1 и C18: 2 их содержание составляет от 24 до 45% от всего суберина. Они присутствуют в низком количестве (<5%) в кутине растений , за исключением Arabidopsis thaliana.где их содержание может быть выше 50%. [6]
Было показано, что гипертермофильные микроорганизмы специфически содержат большое количество дикарбоновых кислот. [7] Это, вероятно, самое важное отличие этих микроорганизмов от других морских бактерий. Дикарбоновые жирные кислоты из С16 до С22 были найдены в гипертермофильном archaeon , Pyrococcus furiosus . Короткие и средней длиной цепи (до 11 атомов углерода) дикарбоновых кислот были обнаружены в цианобактерии рода Aphanizomenon . [8]
Дикарбоновые кислоты могут образовываться в результате ω-окисления жирных кислот во время их катаболизма . Было обнаружено, что эти соединения появляются в моче после введения трикаприна и триундецилина. Хотя значение их биосинтеза остается малоизученным, было продемонстрировано, что ω-окисление происходит в печени крысы, но с низкой скоростью, требует кислорода, NADPH и цитохрома P450 . Позже было показано, что эта реакция более важна у голодающих или страдающих диабетом животных, где 15% пальмитиновой кислоты подвергается ω-окислению, а затем tob-окислению, при этом образуется малонил-коА, который в дальнейшем используется в синтезе насыщенных жирных кислот. [9]Определение дикарбоновых кислот, образующихся при перманганат-периодатном окислении моноеновых жирных кислот, было полезно для изучения положения двойной связи в углеродной цепи. [10]
Дикарбоновые кислоты с разветвленной цепью [ править ]
Длинноцепочечные дикарбоновые кислоты, содержащие вицинальные диметиловые разветвления около центра углеродной цепи, были обнаружены у бактерий рода Butyrivibrio , которые участвуют в переваривании целлюлозы в рубце. [11] Эти жирные кислоты, называемые диаболовыми кислотами , имеют длину цепи в зависимости от жирной кислоты, используемой в культуральной среде. Самая распространенная диаболовая кислота в Butyrivibrio имела длину цепи из 32 атомов углерода. Дьявольские кислоты были также обнаружены в основных липидах рода Thermotoga отряда Thermotogales , бактерий, обитающих в источниках солфатар., глубоководные морские гидротермальные системы и высокотемпературные морские и континентальные нефтяные месторождения. [12] Было показано, что около 10% их липидной фракции составляли симметричные дьявольские кислоты от C30 до C34. Диаболовые кислоты C30 (13,14-диметилоктакозандиовая кислота) и C32 (15,16-диметилтриаконтандиовая кислота) описаны в Thermotoga maritima . [13]
Некоторые исходные двухосновные кислоты от C29 до C32, но с метильными группами на атомах углерода C-13 и C-16, были выделены и охарактеризованы из липидов термофильных анаэробных эубактерий Themanaerobacter ethanolicus. [14] Самой распространенной двухосновной кислотой была C30α, ω-13,16-диметилоктакозандиовая кислота.
Бифитановые двухосновные кислоты присутствуют в геологических отложениях и считаются индикаторами анаэробного окисления метана в прошлом. [15] Несколько форм без или с одним или двумя пентациклическими кольцами были обнаружены в кайнозойских просачиваемых известняках. Эти липиды могут быть неизвестными метаболитами архей.
Кроцетин является основным соединением кроцинов (гликозидов кроцетина), которые являются основными красными пигментами рыльц шафрана ( Crocus sativus ) и плодов гардении ( Gardenia jasminoides ). Кроцетин представляет собой дикарбоновую кислоту с 20 углеродными цепями, которая является дитерпененоидом и может рассматриваться как каротиноид. Это был первый растительный каротиноид, который был признан еще в 1818 году, а история выращивания шафрана насчитывает более 3000 лет. Основным активным ингредиентом шафрана является желтый пигмент кроцин 2.(известны три других производных с различным гликозилированием), содержащие гентиобиозную (дисахаридную) группу на каждом конце молекулы. Был разработан простой и специфический метод ВЭЖХ-УФ для количественной оценки пяти основных биологически активных ингредиентов шафрана, а именно четырех кроцинов и кроцетина. [16]
Ненасыщенные дикарбоновые кислоты [ править ]
Тип Распространенное имя Название ИЮПАК Изомер Структурная формула PubChem Мононенасыщенный Малеиновая кислота (Z) -бутендиовая кислота СНГ 444266 Фумаровая кислота (E) -бутендиовая кислота транс 444972 Ацетилендикарбоновая кислота Но-2-яндиовая кислота непригодный 371 Глутаконовая кислота (Z) -Пент-2-ендиовая кислота СНГ 5370328 (E) -Пент-2-ендиовая кислота транс 5280498 2-децендиовая кислота транс 6442613 Травматическая кислота Додек-2-ендиовая кислота транс 5283028 Ненасыщенный Муконовая кислота (2E, 4E) -Гекса-2,4-диендиовая кислота транс, транс 5356793 (2Z, 4E) -Гекса-2,4-диендиовая кислота цис, транс 280518 (2Z, 4Z) -Гекса-2,4-диендиовая кислота СНГ, СНГ 5280518 Глютиновая кислота
(аллен-1,3-дикарбоновая кислота)(RS) - Пента-2,3-диендиовая кислота HO 2 CCH = C = CHCO 2 H 5242834 Разветвленный Цитраконовая кислота (2Z) -2-метилбут-2-ендиовая кислота СНГ 643798 Мезаконовая кислота (2E) -2-метил-2-бутендиовая кислота транс 638129 Итаконовая кислота 2-Methylidenebutanedioic кислота - 811
Травматическая кислота была одной из первых биологически активных молекул, выделенных из тканей растений. Было показано, что эта дикарбоновая кислота является сильнодействующим средством для заживления ран у растений, которое стимулирует деление клеток рядом с участком раны [17], ее получают из гидропероксидов жирных кислот 18: 2 или 18: 3 после превращения в оксожирные кислоты .
транс, транс- муконовая кислота является метаболитом бензола в организме человека. Поэтому определение его концентрации в моче используется в качестве биомаркера воздействия бензола на рабочем месте или в окружающей среде. [18] [19]
Глютиновая кислота, замещенный аллен , была выделена из Alnus glutinosa (Betulaceae). [20]
В то время как полиненасыщенные жирные кислоты необычны для кутикулы растений, о диненасыщенной дикарбоновой кислоте сообщалось как о компоненте поверхностных восков или сложных полиэфиров некоторых видов растений. Так, октадека-с6, с9-диен-1,18-диоат, производное линолевой кислоты , присутствует в кутикуле Arabidopsis и Brassica napus . [21]
Алкилитаконаты [ править ]
PubChem 811
Несколько дикарбоновых кислот, имеющих боковую алкильную цепь и итаконатное ядро, были выделены из лишайников и грибов , итаконовая кислота (метилен янтарная кислота) является метаболитом, продуцируемым нитчатыми грибами. Среди этих соединений несколько аналогов, называемых хетомеллиновыми кислотами, с разной длиной цепи и степенью ненасыщенности, были выделены из различных видов лишайников Chaetomella . Было показано, что эти молекулы являются ценными в качестве основы для разработки противораковых препаратов из-за их сильного ингибирующего действия на фарнезилтрансферазу . [22]
Ряд алкил- и алкенил-итаконатов, известных как церипоровая кислота ( Pub Chem 52921868 ), был обнаружен в культурах гриба, селективно разлагающего лигнин (гриб белой гнили ), Ceriporiopsis subvermispora. [23] [24] Абсолютная конфигурация церипоровых кислот, их стереоселективный путь биосинтеза и разнообразие их метаболитов были подробно обсуждены. [25]
Замещенные дикарбоновые кислоты [ править ]
Распространенное имя Название ИЮПАК Структурная формула PubChem Тартроновая кислота 2-гидроксипропандиовая кислота 45 Мезоксалевая кислота Оксопропандиовая кислота 10132 Яблочная кислота Гидроксибутандиовая кислота 525 Винная кислота 2,3-дигидроксибутандиовая кислота 875 Щавелевоуксусная кислота Оксобутандиовая кислота 970 Аспарагиновая кислота 2-аминобутандиовая кислота 5960 диоксоянтарная кислота диоксобутандиовая кислота 82062 α-гидроксиГлутаровая кислота 2-гидроксипентандиовая кислота 43 Арабинаровая кислота 2,3,4-тригидроксипентандиовая кислота 109475 Ацетонедикарбоновая кислота 3-оксопентандиовая кислота 68328 α-кетоглутаровая кислота 2-оксопентандиовая кислота 51 Глютаминовая кислота 2-аминопентандиовая кислота 611 Диаминопимелиновая кислота (2R, 6S) -2,6-диаминогептандиовая кислота 865 Сахарная кислота (2S, 3S, 4S, 5R) -2,3,4,5-Тетрагидроксигександиовая кислота 33037
Ароматические дикарбоновые кислоты [ править ]
Общие имена Название ИЮПАК Структура PubChem Фталевая кислота
о- фталевая кислотаБензол-1,2-дикарбоновая кислота 1017 Изофталевая кислота
м- фталевая кислотаБензол-1,3-дикарбоновая кислота 8496 Кислоты терефталевой
р -phthalic кислотыБензол-1,4-дикарбоновая кислота 7489 Дифеновая кислота Бифенил
-2,2'-дикарбоновая кислота2- (2-карбоксифенил) бензойная кислота 10210 2,6-нафталиндикарбоновая кислота 2,6-нафталиндикарбоновая кислота 14357
Терефталевая кислота - это товарный химикат, используемый при производстве полиэфира, известный под торговыми марками, такими как ПЭТ, терилен, дакрон и лавсан .
Свойства [ править ]
Дикарбоновые кислоты представляют собой твердые кристаллические вещества. Растворимость в воде и температура плавления α, ω- соединений прогрессируют последовательно по мере того, как углеродные цепи становятся длиннее с чередованием нечетного и четного числа атомов углерода, так что для четного числа атомов углерода температура плавления выше, чем для следующий в серии с нечетным номером. [26] Эти соединения представляют собой слабые двухосновные кислоты с pK a, стремящимся к значениям ок. 4.5 и 5.5 по мере увеличения расстояния между двумя карбоксилатными группами. Таким образом, в водном растворе при pH около 7, типичном для биологических систем, уравнение Хендерсона – Хассельбаха указывает, что они существуют преимущественно в виде дикарбоксилат-анионов.
Дикарбоновые кислоты, особенно маленькие и линейные, можно использовать в качестве сшивающих реагентов. [27] Дикарбоновые кислоты, в которых карбоксильные группы не разделены ни одним атомом углерода, или одним атомом углерода, разлагаются при нагревании с выделением диоксида углерода и остаются монокарбоновые кислоты. [26]
Правило Бланка гласит, что нагревание бариевой соли дикарбоновой кислоты или ее дегидратация с помощью уксусного ангидрида дает ангидрид циклической кислоты, если атомы углерода, несущие кислотные группы, находятся в положениях 1 и (3,4 или 5). Таким образом, янтарная кислота дает янтарный ангидрид . Для кислот с карбоксильными группами в положениях 1 и 6 эта дегидратация вызывает потерю диоксида углерода и воды с образованием циклического кетона, например, адипиновая кислота образует циклопентанон . [26]
Производные [ править ]
Что касается монофункциональных карбоновых кислот, существуют производные тех же типов. Однако существует дополнительная сложность, заключающаяся в том, что одна или две карбоксильные группы могут быть изменены. Если изменен только один, то производное называется «кислотным», а если изменяются оба конца, оно называется «нормальным». Эти производные включают соли, хлориды, сложные эфиры, амиды и ангидриды. В случае ангидридов или амидов две карбоксильные группы могут объединяться с образованием циклического соединения, например сукцинимида . [28]
См. Также [ править ]
- Трикарбоновая кислота
Ссылки [ править ]
- ^ Мальчик Cornils, Питер Lappe "дикарбоновой кислоты, алифатический" в энциклопедии Ульмана промышленной химии 2006, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a08_523
- ^ Юнг, Хо Вон; Чаплински, Тимоти Дж .; Ван, Линь; Глейзбрук, Джейн; Гринберг, Джин Т. (2009). «Прайминг системного иммунитета растений». Наука . 324 (3 апреля 2009 г.): 89–91. Bibcode : 2009Sci ... 324 ... 89W . DOI : 10.1126 / science.1170025 . PMID 19342588 .
- ^ Кадеш, Ричард Г. (ноябрь 1954 г.). «Двухосновные кислоты». Журнал Американского общества химиков-нефтяников . 31 (11): 568–573. DOI : 10.1007 / BF02638574 .
- ^ a b Кроха, Кайл (сентябрь 2004 г.). «Промышленная биотехнология предоставляет возможности для промышленного производства новых длинноцепочечных двухосновных кислот». Информ . 15 : 568–571.
- ^ Дембицкий, Валерий М; Гольдшлаг, Паулина; Сребник, Моррис (апрель 2002 г.). «Встречаемость дикарбоновых (диоевых) кислот в некоторых средиземноморских орехах». Пищевая химия . 76 (4): 469–473. DOI : 10.1016 / S0308-8146 (01) 00308-9 .
- ^ Поллард, Майк; Бейссон, Фред; Ольрогге, Джон Б. (3 апреля 2009 г.). «Строительство липидных барьеров: биосинтез кутина и суберина». Тенденции в растениеводстве . 13 (5): 89–91. DOI : 10.1016 / j.tplants.2008.03.003 .
- ^ Carballeira, Нью-Мексико; Reyes, M .; Sostre, A .; Huang, H .; Верхаген, М.Ф .; Адамс, MW (2009). «Необычный состав жирных кислот гипертермофильных архей Pyrococcus furiosus и бактерии Thermotoga maritima» . J. Bacteriol . 179 (8): 2766–2768. DOI : 10.1128 / jb.179.8.2766-2768.1997 . PMC 179030 . PMID 9098079 .
- ^ Дембицкий, ВМ; Шкроб, И .; Вперед, СП (2001). «Дикарбоновые и жирнокислотные составы цианобактерий рода Aphanizomenon». Биохимия (Москва) . 66 (1): 72–76. DOI : 10,1023 / A: 1002837830653 . PMID 11240396 .
- ^ Wada, F .; Усами М. (1997). «Исследования антикетогенного действия жирных кислот ω-окисления и глюконеогенности дикарбоновых кислот». Biochimica et Biophysica Acta (BBA) - липиды и липидный метаболизм . 487 (2): 261–268. DOI : 10.1016 / 0005-2760 (77) 90002-9 .
- ^ Longmuir, Кеннет Дж .; Росси, Мэри Э .; Резеле-Тиден, Кристина (1987). «Определение положения двойной связи моноеновой жирной кислоты перманганат-периодатным окислением с последующей высокоэффективной жидкостной хроматографией фенациловых эфиров карбоновых кислот». Аналитическая биохимия . 167 (2): 213–221. DOI : 10.1016 / 0003-2697 (87) 90155-2 . PMID 2831753 .
- ^ Кляйн, РА; Hazlewood, GP; Кемп, П; Доусон, РМ (1 декабря 1979 г.). «Новая серия длинноцепочечных дикарбоновых кислот с вицинальным диметиловым разветвлением, обнаруженных в качестве основных компонентов липидов Butyrivibrio spp» . Биохимический журнал . 183 (3): 691–700. DOI : 10.1042 / bj1830691 . PMC 1161651 . PMID 540040 .
- ^ Хубер, Роберт; Langworthy, Thomas A .; Кениг, Гельмут; Томм, Майкл; Woese, Carl R .; Sleytr, Uwe B .; Стеттер, Карл О. (май 1986 г.). «Thermotoga maritima sp. Nov. Представляет собой новый род уникальных чрезвычайно теплолюбивых эубактерий, растущих до 90 ° C». Архив микробиологии . 144 (4): 324–333. DOI : 10.1007 / BF00409880 .
- ^ Carballeira, Нью-Мексико; Рейес, М; Состре, А; Хуанг, Н; Верхаген, М.Ф .; Адамс, MW (апрель 1997 г.). «Необычный состав жирных кислот гипертермофильных архей Pyrococcus furiosus и бактерии Thermotoga maritima» . Журнал бактериологии . 179 (8): 2766–8. DOI : 10.1128 / jb.179.8.2766-2768.1997 . PMC 179030 . PMID 9098079 .
- ^ Юнг, S; Zeikus, JG; Холлингсуорт, Род-Айленд (июнь 1994 г.). «Новое семейство очень длинноцепочечных альфа, омега-дикарбоновых кислот является основным структурным жирным ацильным компонентом мембранных липидов Thermoanaerobacter ethanolicus 39E». Журнал липидных исследований . 35 (6): 1057–65. PMID 8077844 .
- ^ Биргель, Дэниел; Элверт, Маркус; Хан, Xiqiu; Пекманн, Йорн (январь 2008 г.). «Бифитановые двухосновные кислоты, обедненные 13C, как индикаторы анаэробного окисления метана в прошлом». Органическая геохимия . 39 (1): 152–156. DOI : 10.1016 / j.orggeochem.2007.08.013 .
- ^ Ли, На; Лин, Ге; Кван, Ю-Ва; Минь, Чжи-Да (июль 1999 г.). «Одновременное количественное определение пяти основных биологически активных ингредиентов шафрана с помощью высокоэффективной жидкостной хроматографии». Журнал хроматографии A . 849 (2): 349–355. DOI : 10.1016 / S0021-9673 (99) 00600-7 . PMID 10457433 .
- ^ Фермер, Эдвард Э. (1994). «Передача сигналов жирных кислот в растениях и связанных с ними микроорганизмах». Молекулярная биология растений . 26 (5): 1423–1437. DOI : 10.1007 / BF00016483 . PMID 7858198 .
- ^ Wiwanitkit В, Soogarun S, Suwansaksri J (2007). «Корреляционное исследование параметров красных кровяных телец и трансмуконовой кислоты в моче у субъектов с профессиональным воздействием бензола». Токсикологическая патология . 35 (2): 268–9. DOI : 10.1080 / 01926230601156278 . PMID 17366320 .
- ^ Уивер В.М., Даволи СТ, Хеллер П.Дж. и др. (1996). «Воздействие бензола, оцениваемое по трансмуконовой кислоте в моче, у городских детей с повышенным уровнем свинца в крови» . Environ. Перспектива здоровья . 104 (3): 318–23. DOI : 10.2307 / 3432891 . JSTOR 3432891 . PMC 1469300 . PMID 8919771 .
- ^ Сати, Сушил Чандра; Сати, Нитин; Сати, ОП (2011). «Биоактивные компоненты и лекарственное значение рода Alnus » . Обзоры фармакогнозии . 5 (10): 174–183. DOI : 10.4103 / 0973-7847.91115 . PMC 3263052 . PMID 22279375 .
- ↑ Бонавентура, Густаво; Ольрогге, Джон; Поллард, Майк (2004). «Анализ алифатического мономерного состава полиэфиров, связанных с эпидермисом Arabidopsis: наличие октадека-цис-6, цис-9-диен-1,18-диоата в качестве основного компонента» . Заводской журнал . 40 (6): 920–930. DOI : 10.1111 / j.1365-313X.2004.02258.x . PMID 15584957 .
- ^ Сингх, SB; Джаясурия, H; Сильверман, KC; Бонфлио, Калифорния; Уильямсон, JM; Лингем, РБ (март 2000 г.). «Эффективный синтез, ингибирующая активность фарнезил-протеинтрансферазы человека и дрожжей хетомеллиновых кислот и аналогов». Биоорганическая и медицинская химия . 8 (3): 571–80. DOI : 10.1016 / S0968-0896 (99) 00312-0 . PMID 10732974 . - через ScienceDirect (может потребоваться подписка или контент может быть доступен в библиотеках.)
- ^ Enoki, Макико; Ватанабэ, Такаши; Хонда, Йоичи; Кувахара, Масааки (2000). «Новая флуоресцентная дикарбоновая кислота, (Z) -1,7-нонадекадиен-2,3-дикарбоновая кислота, продуцируемая грибком белой гнили Ceriporiopsis subvermispora». Письма по химии . 29 (1): 54–55. DOI : 10,1246 / cl.2000.54 .
- ^ Амирта, Рудианто; Фухимори, Кения; Шираи, Нобуаки; Хонда, Йоичи; Ватанабэ, Такаши (декабрь 2003 г.). «Церипоровая кислота С, гексадеценилитаконат, продуцируемый разлагающим лигнин грибком Ceriporiopsis subvermispora». Химия и физика липидов . 126 (2): 121–131. DOI : 10.1016 / S0009-3084 (03) 00098-7 . PMID 14623447 .
- ↑ Нисимура, Хироши; Мураяма, Киоко; Ватанабэ, Такахито; Хонда, Йоичи; Ватанабэ, Такаши (июнь 2009 г.). «Абсолютная конфигурация церипоровых кислот, метаболитов, подавляющих окислительно-восстановительный потенциал железа, вырабатываемых селективным разрушающим лигнин грибком Ceriporiopsis subvermispora». Химия и физика липидов . 159 (2): 77–80. DOI : 10.1016 / j.chemphyslip.2009.03.006 . PMID 19477313 .
- ^ a b c Шмидт, Юлиус (1955). Органическая химия . Лондон: Оливер и Бойд. С. 283–284.
- ^ Могхадас, Бабак; Солоук, Атефе; Садеги, Давуд (24.08.2020). «Разработка хитозановой мембраны с использованием нетоксичных сшивающих агентов для потенциальных применений для перевязки ран» . Полимерный бюллетень . DOI : 10.1007 / s00289-020-03352-8 . ISSN 1436-2449 .
- ^ Bernthsen, A. (1922). Органическая химия . Лондон: Блэки и сын. п. 242.
Внешние ссылки [ править ]
- Липидомический портал Структура База данных Дикарбоновые кислоты
- Дейкстра, Альберт Дж. «Тривиальные названия жирных кислот - Часть 1» . lipidlibrary.aocs.org . Проверено 24 июня 2019 .