 | |
 | |
| Имена | |
|---|---|
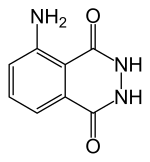
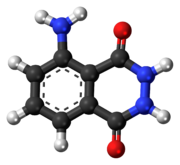
| Предпочтительное название IUPAC 5-амино-2,3-дигидрофталазин-1,4-дион | |
| Другие названия 5-амино-2,3-дигидро-1,4-фталазиндион о- аминофталоилгидразид о- аминофталилгидразид 3-аминофтальгидразид 3-аминофталевый гидразид | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.007.556 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| C 8 H 7 N 3 O 2 | |
| Молярная масса | 177,16 г / моль |
| Температура плавления | 319 ° С (606 ° F, 592 К) |
| Опасности | |
| Паспорт безопасности | MSDS для люминола |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Люминол (C 8 H 7 N 3 O 2 ) представляет собой химическое вещество, которое проявляет хемилюминесценцию с голубым свечением при смешивании с подходящим окислителем . Люминол - это кристаллическое твердое вещество от белого до бледно-желтого цвета, растворимое в большинстве полярных органических растворителей, но не растворимое в воде.
Судебно-медицинские эксперты используют люминол для обнаружения следов крови на месте преступления , поскольку он вступает в реакцию с железом, содержащимся в гемоглобине . Биологи используют его в клеточных анализах для обнаружения меди , железа , цианидов , а также определенных белков с помощью вестерн-блоттинга . [2]
Когда люминол распыляется равномерно по площади, следовые количества активирующего окислителя заставляют люминол излучать голубое свечение, которое можно увидеть в затемненной комнате. Свечение длится всего около 30 секунд, но может быть задокументировано фотографически. Свечение сильнее в областях, на которые наносится больше брызг; интенсивность свечения не указывает на количество крови или другого активатора.
Синтез [ править ]
Люминол синтезируется в двухступенчатом процессе, начиная с 3- нитрофталевой кислоты . [3] [4] Сначала гидразин (N 2 H 4 ) нагревают с 3-нитрофталевой кислотой в высококипящем растворителе, таком как триэтиленгликоль и глицерин . Замещение ацил реакция конденсации происходит с потерей воды, образуя 3-nitrophthalhydrazide. Снижение нитрогруппы до аминогруппы с дитионитом натрия (Na 2 S 2 O 4 ), с помощью переходного гидроксиламина промежуточный, производит люминол.
Соединение было впервые синтезировано в Германии в 1902 г. [5], но называлось «люминол» только в 1934 г. [3] [6]
Хемилюминесценция [ править ]
Для проявления люминесценции люминол необходимо активировать окислителем. Обычно активатором является раствор, содержащий перекись водорода (H 2 O 2 ) и ионы гидроксида в воде. В присутствии катализатора, такого как соединение железа или периодата , перекись водорода разлагается с образованием кислорода и воды:
- 2 Н 2 О 2 → О 2 + 2 Н 2 О
- Н 2 О 2 + КИО 4 → КИО 3 + О 2 + Н 2 О
В лабораторных условиях в качестве катализатора часто используют феррицианид калия или периодат калия . При судебно-медицинском обнаружении крови катализатором является железо, присутствующее в гемоглобине . [7] Ферменты в различных биологических системах также могут катализировать разложение перекиси водорода.
Точный механизм хемилюминесценции люминола представляет собой сложную многоступенчатую реакцию, особенно в водных условиях. Недавнее теоретическое исследование позволило прояснить каскад реакций, как показано ниже. [8] Люминол сначала депротонируется в основных условиях, а затем окисляется до анионного радикала. Что, в свою очередь, имеет два доступных пути для получения ключевого промежуточного α-гидроксипероксида. После циклизации до эндопероксида моноанион будет подвергаться разложению без люминесценции, если pH слишком низкий (<8,2) для второго депротонирования. Однако эндопероксидный дианион может давать ретро-продукт Дильса-Альдера: 1,2-диоксан-3,6-дион дианион. И после химического возбужденияпосредством двух одноэлектронных переносов (SET) дает дианион 3-аминофталата в его первом синглетном возбужденном состоянии (S1). Эта очень нестабильная молекула релаксирует в основное состояние, испуская свет длиной около 425 нм (пурпурно-синий), так называемая хемилюминесценция .
Использование в уголовном расследовании [ править ]
История [ править ]
В 1928 году немецкий химик Х.О. Альбрехт обнаружил, что кровь , среди других веществ, усиливает люминесценцию люминола в щелочном растворе перекиси водорода. [9] [10] В 1936 году Карл Глеу и Карл Пфаннштиль подтвердили это улучшение в присутствии гематина , компонента крови. [11] В 1937 году немецкий судебно-медицинский эксперт Вальтер Шпехт провел обширные исследования применения люминола для обнаружения крови на местах преступления. [12] В 1939 году патологи Сан-Франциско Фредерик Проешер и А.М. Муди сделали три важных наблюдения относительно люминола: [13] [14]
- хотя тест является предположительным, можно быстро исследовать большие участки предполагаемого материала;
- засохшая и разложившаяся кровь давала более сильную и продолжительную реакцию, чем свежая кровь; и
- если люминесценция исчезнет, ее можно воспроизвести, нанеся свежий раствор люминола и перекиси водорода; Таким образом, засохшие пятна крови могут многократно становиться люминесцентными.
Теория [ править ]
Следователи на месте преступления используют люминол для поиска следов крови, даже если ее кто-то очистил или удалил. Исследователь распыляет раствор люминола и окислителя. Железо в крови катализирует свечение. Количество катализатора, необходимое для того, чтобы вызвать реакцию, очень мало по сравнению с количеством люминола, что позволяет обнаруживать даже следовые количества крови. Синее свечение длится около 30 секунд на одно нанесение. Для обнаружения свечения требуется довольно темная комната. Любое обнаруженное свечение может быть задокументировано фотографией с длинной выдержкой .
Недостатки [ править ]
Использование люминола при расследовании на месте преступления несколько затруднено из-за того, что он реагирует на соединения, содержащие железо и медь , [15] отбеливатели , хрен , мочу , фекалии или остатки дыма. [ требуется пояснение ] [14] Применение люминола к вещественному доказательству может помешать проведению других тестов; однако ДНК была успешно извлечена из образцов, подвергшихся воздействию люминола. [16]
Связанные молекулы [ править ]
- Люминол: 5-амино-2,3-дигидро-1,4-фталазиндион; 3-аминофтальгидразид; 1,4-фталазиндион, 5-амино-2,3-дигидро; CAS: [521-31-3]
С 8 Н 7 N 3 O 2 - MW: 177,16
λ абс (в 0,1 N NaOH) λ макс 1: 347 нм и λ макс 2: 300 нм; ЭК (при λ max 1): 7650 л / моль × см
λ абс / λ em (MeOH): 355/413 нм - Люминол, натриевая соль: 3-аминофтальгидразид натрия; CAS: [20666-12-0]
C 8 H 6 N 3 O 2 Na - молекулярная масса: 199,12 - Полугидрат люминола: гидрат 3-аминофтальгидразида натрия; CAS: [206658-90-4]
C 8 H 6 N 3 O 2 Na • H 2 O - молекулярная масса: 217,16 - Люминола гидрохлорид: гидрохлорид 3-аминофтальгидразида; CAS: [74165-64-3]
C 8 H 7 N 3 O 2 · HCl. ММ: 213,62 - Изолюминол: 4-аминофтальгидразид; CAS: [3682-14-1]
C 8 H 7 N 3 O 2 - МВ: 117,16 (Xi) - Моногидрат изолюминола: моногидрат 4-аминофтальгидразида
C 8 H 7 N 3 O 2 • H 2 O - молекулярная масса: 195,15 - Изолюминол ABEI: моногидрат 4-аминофтальгидразида; CAS: [66612-29-1]
См. Также [ править ]
- Флуоресцеин
- Дифенил оксалат
Ссылки [ править ]
- Перейти ↑ Merck Index , 11-е издание, 5470 .
- ^ Хан, Парвез; Идрис, датский; MOxley, Michael A .; и другие. (Май 2014 г.). «Хемилюминесцентные сигналы на основе люминола: клиническое и неклиническое применение и будущее использование» . Прикладная биохимическая биотехнология . 173 (2): 333–355. DOI : 10.1007 / s12010-014-0850-1 . PMC 4426882 . PMID 24752935 .
- ^ a b Эрнест Хантресс; Лестер Стэнли; Алмон Паркер (1934). «Препарат 3-аминофтальгидразида для демонстрации хемилюминесценции». Журнал Американского химического общества . 56 (1): 241–242. DOI : 10.1021 / ja01316a077 .
- ^ Синтез люминола
- ^ См .:
- Алоис Йозеф Шмитц, "Ueber das Hydrazid der Trimesinsäure und der Hemimellithsäure" Архивировано 2 января 2015 года на Wayback Machine (О гидразиде тримезиновой кислоты [1,3,5-бензолтрикарбоновой кислоты] и гемимеллитовой кислоты [1,2, 3-бензолтрикарбоновая кислота]), инаугурационная диссертация, Гейдельбергский университет, 1902 г .; С. 17, 39–43. Шмитц называет люминол «1-амино-2,3-фтальсоригидразидом».
- Примечание: Гилл утверждает, что люминол был получен еще в 1853 году. См .: Стивен К. Гилл (1983) «Новые разработки в исследованиях хемилюминесценции», Aldrichimica Acta 16 (3): 59–61; есть сноска 2 на стр. 60. Доступно по адресу: Aldrichimica Acta. Архивировано 8 января 2015 г. в Wayback Machine . Однако источники, которые цитирует Гилл, не упоминают о получении люминола до 1902 года. Гилл, вероятно, перепутал люминол с лофином (2,4,5-трифенил- 1H- имидазолом), о чем упоминают источники, которые он цитирует. Лофин также является хемилюминесцентным и был впервые приготовлен в 1844 году Огюстом Лораном. (См .: Огюст Лоран (1844) "Sur un nouvel alcali organique, la lophine"(О новой органической щелочи, лофине), Revue scientifique et INDustrielle , 18 : 272–278.) Хемилюминесценцию лофина впервые наблюдали: Радзишевский, Бронислав Л. (1877) "Untersuchungen über Hydrobenzamid, Amarin und Lophin" Архив за 2015 г. -12-14 в Wayback Machine (Исследования гидробензамида, амарина и лофина), Berichte der Deutschen chemischen Gesellschaft zu Berlin , 10 : 70–75. В 1853 году Людвиг Тейхманн разработал тест на кровь, но он не полагался на хемилюминесценцию. См .: Л. Тайхманн (1853) "Ueber die Krystallisation der Organischen Bestandtheile des Bluts"(О кристаллизации органических компонентов крови), Zeitschrift für rationelle Medicin , новая серия, 3 : 375–388.
- ↑ См. Также: Эрнест Х. Хантресс, Лестер Н. Стэнли и Алмон С. Паркер (март 1934 г.) «Окисление 3-аминофтальгидразида (« люминол ») как лекционная демонстрация хемилюминесценции», Journal of Chemical Education , 11 ( 3): 142–145.
- ↑ Плес, Марек. «Хемилюминесценция, активируемая кровью» . www.weirdscience.eu (на польском языке). Архивировано из оригинала на 2015-01-03 . Проверено 23 декабря 2014 .
- ^ а б Юэ, Линг; Лю И-Тонг (2020-09-03). «Механическое понимание pH-зависимой хемилюминесценции люминола в водном растворе» . Журнал физической химии B . 124 (35): 7682–7693. DOI : 10.1021 / acs.jpcb.0c06301 . ISSN 1520-6106 . PMID 32790377 .
- ^ HO Альбрехт (1928) "Uber die Chemiluminescenz des Aminophthalsäurehydrazids" (О хемилюминесценции гидразида аминофталевой кислоты) Zeitschrift für Physikalische Chemie 136 : 321–330.
- ^ Стюарт Х. Джеймс и Уильям Г. Эккерт, Интерпретация доказательств пятен крови на местах преступлений , 2-е изд. (Бока-Ратон, Флорида: CRC Press LLC, 1998), страница 154 Архивировано 15 февраля 2017 г. в Wayback Machine .
- ^ Глеу, Карл; Пфанштиль, Карл (1936) "Убер-3-аминофтальзавр-гидразид" Journal für Praktische Chemie 146 : 137–150.
- ^ Specht, Вальтер (1937) "Die Chemiluminescenz des Hämins, ein Hilfsmittel zur Auffindung und Erkennung forensisch wichtiger Blutspuren" (Хемилюминесценция гемина, помощь в обнаружении и распознавании значимых следов крови), Angewandte Chemie 50 (8) 155–157.
- ^ Проешер Ф. и Муди AM (1939) "Обнаружение крови с помощью хемилюминесценции", Журнал лабораторной и клинической медицины , 24 : 1183–1189.
- ^ а б Джеймс, Стюарт; Киш, Пол Э .; Саттон, Полетт Саттон (2005). Принципы анализа образцов кровавых пятен . Бока-Ратон, Лондон, Нью-Йорк, Сингапур: Тейлор и Фрэнсис Групп. п. 376 . ISBN 0-8493-2014-3.
- ↑ Плес, Марек. «Хемилюминесценция люминола, активированного соединением меди» . www.weirdscience.eu (на польском языке). Архивировано из оригинала на 2015-01-03 . Проверено 23 декабря 2014 .
- ^ Техническое примечание о Hemaglow архивной 2 января 2015 года, в Wayback Machine
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме люминола . |
- HowStuffWorks «Как работает люминол»
- Демонстрация люминола в Турине
