 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Азидометан | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
PubChem CID | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| CH 3 N 3 | |||
| Молярная масса | 57,05 | ||
| Появление | белый порошок | ||
| слабо растворимый | |||
| Растворимость | алкан, эфир | ||
| Взрывоопасные данные | |||
| Чувствительность к ударам | Высокая | ||
| Чувствительность к трению | Высокая | ||
| Опасности | |||
| Основные опасности | Очень взрывоопасен | ||
| Родственные соединения | |||
Родственные соединения | Азотистоводородная кислота , хлор азид , этиловый азид | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
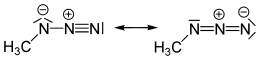
Метил азид представляет собой ковалентные молекулы , связанные с азотистоводородной кислотой и другими алкильными азидами .
Подготовка и свойства [ править ]
Метил азид может быть получен с помощью метилирования из азида натрия , например , с диметилсульфатом в щелочном растворе, с последующим пропусканием через трубку безводного хлорида кальция или гидроксид натрия для удаления загрязняющего азотистоводородной кислоты . [1] О первом синтезе было сообщено в 1905 году. [2]
Он разлагается в реакции первого порядка : [3]
- CH 3 N 3 → CH 3 N + N 2
Метилазид может быть потенциальным предшественником в синтезе пребиотических молекул через неравновесные реакции на межзвездных льдах, инициированные энергетическими галактическими космическими лучами (ГКЛ) и фотонами . [4]
Меры предосторожности [ править ]
Метилазид стабилен при температуре окружающей среды, но может взорваться при нагревании. Присутствие ртути увеличивает чувствительность к ударам и искрам. Несовместим с метанолом и диметилмалонатом . [5] При нагревании до разложения выделяет токсичные пары NO x . [ необходима цитата ] Его можно хранить неограниченное время в темноте при -80 ° C. [1]
Ссылки [ править ]
- ^ a b Чэ, Чонхён (2008-03-14), «Метилазид», в John Wiley & Sons, Ltd (ред.), Энциклопедия реагентов для органического синтеза , Чичестер, Великобритания: John Wiley & Sons, Ltd, стр. . rn00795, DOI : 10.1002 / 047084289x.rn00795 , ISBN 978-0-471-93623-7
- ^ Dimroth, O .; Wislicenus, W. (1905). «Убер дас метилазид» . Berichte der Deutschen Chemischen Gesellschaft . 38 (2): 1573–1576. DOI : 10.1002 / cber.19050380254 .
- ^ О'Делл, MS; Дарвент, Б. (1970). «Термическое разложение метилазида» . Канадский химический журнал . 48 (7): 1140–1147. DOI : 10.1139 / v70-187 .
- ^ Quinto-Hernandez, A .; Водтке, AM; Беннетт, CJ; Kim, YS; Кайзер, Р.И. (2011). «О взаимодействии льдов метилазида (CH 3 N 3 ) с ионизирующим излучением: образование метанимина (CH 2 NH), цианида водорода (HCN) и изоцианида водорода (HNC)». Журнал физической химии . 115 (3): 250–264. DOI : 10.1021 / jp103028v . PMID 21162584 .
- ^ Урбен, PG, изд. (2006). Справочник Бретерика по опасностям реактивных химических веществ (7-е изд.). Эльзевир. ISBN 9780123725639.
Внешние ссылки [ править ]
- Graner, G .; Hirota, E .; Иидзима, Т .; Kuchitsu, K .; Рамзи, Д.А.; Vogt, J .; Фогт, Н. (1999). «CH 3 N 3 Метилазид». В Кучицу, К. (ред.). Группа II Молекулы и радикалы: числовые данные и функциональные отношения в науке и технике . Ландольт-Бёрнштейн - молекулы и радикалы группы II. 25 B . п. 1. дои : 10.1007 / 10653318_320 . ISBN 3-540-63645-5.
- «Метилазид» . Интернет-книга NIST . Национальный институт стандартов и технологий.
| HN 3 | Он | ||||||||||||||||||
| LiN 3 | Быть (N 3 ) 2 | В (N 3 ) 3 | CH 3 N 3 , C (N 3 ) 4 | NH 4 N 3 N 3 NO N (N 3 ) 3 , H 2 N — N 3 | О | FN 3 | Ne | ||||||||||||
| NaN 3 | Мг (N 3 ) 2 | Al (N 3 ) 3 | Si (N 3 ) 4 | п | SO 2 (N 3 ) 2 | ClN 3 | Ar | ||||||||||||
| Кн 3 | Ca (N 3 ) 2 | СБН (N 3 ) 3 | Ti (N 3 ) 4 | ВО (№ 3 ) 3 | Cr (N 3 ) 3 , CrO 2 (N 3 ) 2 | Mn (N 3 ) 2 | Fe (N 3 ) 2 , Fe (N 3 ) 3 | Co (N 3 ) 2 , Co (N 3 ) 3 | Ni (N 3 ) 2 | CuN 3 , Cu (N 3 ) 2 | Zn (N 3 ) 2 | Ga (N 3 ) 3 | Ge | В виде | Se (N 3 ) 4 | 3 руб. | Kr | ||
| 3 руб. | Sr (N 3 ) 2 | Y | Zr (N 3 ) 4 | Nb | Пн | Tc | Ru (N 3 ) 6 3- | Rh (N 3 ) 6 3- | Pd (N 3 ) 2 | AgN 3 | Cd (N 3 ) 2 | В | Sn | Sb | Te | В 3 | Xe (N 3 ) 2 | ||
| ЦСН 3 | Ba (N 3 ) 2 | Hf | Та | W | Re | Операционные системы | Ir (N 3 ) 6 3- | Pt (N 3 ) 6 2− | Au (N 3 ) 4 - | Hg 2 (N 3 ) 2 , Hg (N 3 ) 2 | TlN 3 | Pb (N 3 ) 2 | Би (N 3 ) 3 | По | В | Rn | |||
| Пт | Ra (N 3 ) 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Ур. | Ц | Og | |||
| ↓ | |||||||||||||||||||
| Ла | Ce (N 3 ) 3 , Ce (N 3 ) 4 | Pr | Nd | Вечера | См | Евросоюз | Gd (N 3 ) 3 | Tb | Dy | Хо | Э | Тм | Yb | Лу | |||||
| Ac | Чт | Па | UO 2 (N 3 ) 2 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||||

