 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Азид водорода | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.029.059 |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| HN 3 | |
| Молярная масса | 43,03 г / моль |
| Внешность | бесцветная, легколетучая жидкость |
| Плотность | 1,09 г / см 3 |
| Температура плавления | -80 ° С (-112 ° F, 193 К) |
| Точка кипения | 37 ° С (99 ° F, 310 К) |
| хорошо растворим | |
| Растворимость | растворим в щелочах , спирте , эфире |
| Кислотность (p K a ) | 4.6 [1] |
| Основание конъюгата | Азид |
| Структура | |
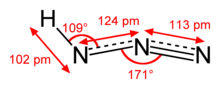
| приблизительно линейный | |
| Опасности | |
| Основные опасности | Сильнотоксичный, взрывоопасный, реактивный |
| R-фразы (устаревшие) | R3 , R27 / 28 |
| S-фразы (устаревшие) | S33 , S36 / 37 , S38 |
| NFPA 704 (огненный алмаз) |  4 0 3 |
| Родственные соединения | |
Другие катионы | Азид натрия |
Родственные гидриды азота | Аммиак Гидразин |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Азотистоводородная кислота , также известная как азид водорода или azoimide , [2] , представляет собой соединение с химической формулой HN 3 . [3] Это бесцветная, летучая и взрывоопасная жидкость при комнатной температуре и давлении. Это соединение азота и водорода и, следовательно, гидрид пниктогена . Впервые он был выделен в 1890 году Теодором Курцием . [4] Кислота имеет несколько применений, но ее сопряженное основание , азид- ион, используется в специализированных процессах.
Гидразойная кислота, как и другие минеральные кислоты , растворяется в воде. Неразбавленная азотная кислота является взрывоопасной [5] со стандартной энтальпией образования Δ f H o (l, 298 K) = +264 кДжмоль -1 . [6] При разбавлении газ и водные растворы (<10%) можно безопасно обрабатывать.
Производство [ править ]
Кислота обычно образуется при подкислении азидной соли, такой как азид натрия . Обычно растворы азида натрия в воде содержат следовые количества азида кислоты в равновесии с солью азида, но введение более сильной кислоты может преобразовать первичные частицы в растворе в азидную кислоту. Затем чистую кислоту можно получить фракционной перегонкой в виде чрезвычайно взрывоопасной бесцветной жидкости с неприятным запахом. [2]
- NaN 3 + HCl → HN 3 + NaCl
Его водный раствор также можно приготовить путем обработки раствора азида бария разбавленной серной кислотой , фильтруя нерастворимый сульфат бария . [7]
Первоначально он был получен реакцией водного гидразина с азотистой кислотой .
- N 2 H 4 + HNO 2 → HN 3 + 2 H 2 O
Также можно использовать другие окислители, такие как перекись водорода , нитрозилхлорид , трихлорамин или азотная кислота . [8]
Реакции [ править ]
По своим свойствам гидразойная кислота проявляет некоторую аналогию с галогеновыми кислотами, поскольку образует малорастворимые (в воде) соли свинца, серебра и ртути (I). Все соли металлов кристаллизуются в безводной форме и разлагаются при нагревании, оставляя остаток чистого металла. [2] Это слабая кислота (p K a = 4,75. [6] ) Ее соли тяжелых металлов взрывоопасны и легко взаимодействуют с иодидами алкила . Азиды более тяжелых щелочных металлов (за исключением лития ) или щелочноземельных металлов не взрывоопасны, но разлагаются более контролируемым образом при нагревании, выделяя спектроскопически чистый азот.
2газ. [9] Растворы азойной кислоты растворяют многие металлы (например, цинк , железо ) с выделением водорода и образованием солей, которые называются азидами (ранее также назывались азоимидами или гидразоатами).
Гидразойная кислота может реагировать с карбонильными производными, включая альдегиды, кетоны и карбоновые кислоты, с образованием амина или амида с вытеснением азота. Это называется реакцией Шмидта или перегруппировкой Шмидта.
При растворении в самых сильных кислотах образуются взрывоопасные соли, содержащие H
2N = N = N+
ion, например: [9]
- HN = N = N + HSbCl
6→ [H
2N = N = N]+
[SbCl
6]-
Ион H
2N = N = N+
является изоэлектронным к диазометано .
Разложение азотной кислоты при ударе, трении, искре и т. Д. Происходит следующим образом:
- 2 HN
3→ H
2+ 3 N
2
Токсичность [ править ]
Гидразойная кислота летучая и очень токсичная. Он имеет резкий запах, и его пары могут вызывать сильные головные боли . Соединение действует как некумулятивный яд.
Приложения [ править ]
2-Фуронитрил , фармацевтический промежуточный продукт и потенциальный искусственный подслащивающий агент, был получен с хорошим выходом путем обработки фурфурола смесью азотной кислоты (HN 3 ) и хлорной кислоты в присутствии перхлората магния в бензольном растворе при 35 ° C. [10] [11]
Полностью газофазный йодный лазер (AGIL) смешивает газообразную азотистую кислоту с хлором для получения возбужденного хлорида азота , который затем используется для генерации йода ; это позволяет избежать требований к жидкой химии лазеров COIL .
Ссылки [ править ]
- ^ Прадёт Патнаик. Справочник неорганических химикатов . Макгроу-Хилл, 2002, ISBN 0-07-049439-8
- ^ a b c Чисхолм, Хью, изд. (1911). . Британская энциклопедия . 3 (11-е изд.). Издательство Кембриджского университета. С. 82–83. Он также содержит подробное описание одновременного производственного процесса.
- ^ Словарь неорганических и металлоорганических соединений . Чепмен и Холл.
- ^ Курций, Теодор (1890). "Ueber Stickstoffwasserstoffsäure (Азоимид) N 3 H" [О азоимиде азоимида N 3 H]. Berichte der Deutschen Chemischen Gesellschaft . 23 (2): 3023–3033. DOI : 10.1002 / cber.189002302232 .
- ^ Фурман, Дэвид; Дубникова, Фаина; ван Дуин, Адри, Коннектикут; Зейри, Иегуда; Кослофф, Ронни (2016-03-10). «Поле реактивных сил для жидкой азотной кислоты с приложениями к детонационной химии». Журнал физической химии C . 120 (9): 4744–4752. DOI : 10.1021 / acs.jpcc.5b10812 . ISSN 1932-7447 .
- ^ а б Кэтрин Э. Хаукрофт; Алан Г. Шарп (2008). «Глава 15: Группа 15 элементов». Неорганическая химия, 3-е издание . Пирсон. п. 449. ISBN. 978-0-13-175553-6.
- ^ L. Ф. Одриет, Азид водорода К.Ф. Гиббса в водном и эфирном растворах "Неорганические синтезы 1939 г., том 1, стр. 71-79.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 432. ISBN. 978-0-08-037941-8.
- ^ а б Эгон Виберг; Нильс Виберг; Арнольд Фредерик Холлеман (2001). «Азотная группа». Неорганическая химия . Академическая пресса. п. 625. ISBN 978-0-12-352651-9.
- ^ П.А. Павлов; Кульневич, В.Г. (1986). «Синтез 5-замещенных фураннитрилов и их реакция с гидразином». Химия Гетероциклических Соединений . 2 : 181–186.
- ^ Б. Бандгар; Маконе, С. (2006). «Органические реакции в воде. Превращение альдегидов в нитрилы с использованием NBS в мягких условиях». Синтетические коммуникации . 36 (10): 1347–1352. DOI : 10.1080 / 00397910500522009 . S2CID 98593006 .
Внешние ссылки [ править ]
- СМИ, связанные с азидом водорода на Викискладе?
- OSHA: гидразойная кислота
| HN 3 | Он | ||||||||||||||||||
| LiN 3 | Быть (N 3 ) 2 | В (N 3 ) 3 | CH 3 N 3 , C (N 3 ) 4 | N (N 3 ) 3 , H 2 N — N 3 | О | FN 3 | Ne | ||||||||||||
| NaN 3 | Мг (N 3 ) 2 | Al (N 3 ) 3 | Si (N 3 ) 4 | п | SO 2 (N 3 ) 2 | ClN 3 | Ar | ||||||||||||
| Кн 3 | Ca (N 3 ) 2 | СБН (N 3 ) 3 | Ti (N 3 ) 4 | ВО (№ 3 ) 3 | Cr (N 3 ) 3 , CrO 2 (N 3 ) 2 | Mn (N 3 ) 2 | Fe (N 3 ) 2 , Fe (N 3 ) 3 | Co (N 3 ) 2 , Co (N 3 ) 3 | Ni (N 3 ) 2 | CuN 3 , Cu (N 3 ) 2 | Zn (N 3 ) 2 | Ga (N 3 ) 3 | Ge | В качестве | Se (N 3 ) 4 | 3 руб. | Kr | ||
| 3 руб. | Sr (N 3 ) 2 | Y | Zr (N 3 ) 4 | Nb | Пн | Tc | Ru (N 3 ) 6 3- | Rh (N 3 ) 6 3- | Pd (N 3 ) 2 | AgN 3 | Cd (N 3 ) 2 | В | Sn | Sb | Te | В 3 | Xe (N 3 ) 2 | ||
| ЦСН 3 | Ba (N 3 ) 2 | Hf | Та | W | Re | Операционные системы | Ir (N 3 ) 6 3- | Pt (N 3 ) 6 2− | Au (N 3 ) 4 - | Hg 2 (N 3 ) 2 , Hg (N 3 ) 2 | TlN 3 | Pb (N 3 ) 2 | Би (N 3 ) 3 | По | В | Rn | |||
| Пт | Ra (N 3 ) 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Ур. | Ц | Og | |||
| ↓ | |||||||||||||||||||
| Ла | Ce (N 3 ) 3 , Ce (N 3 ) 4 | Pr | Nd | Вечера | См | Европа | Gd (N 3 ) 3 | Tb | Dy | Хо | Э | Тм | Yb | Лу | |||||
| Ac | Чт | Па | UO 2 (N 3 ) 2 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||||