 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Коболмин |
| AHFS / Drugs.com | Международные названия лекарств |
| Пути администрирования | пероральный, сублингвальный, инъекционный. |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard | 100.033.200 |
| Химические и физические данные | |
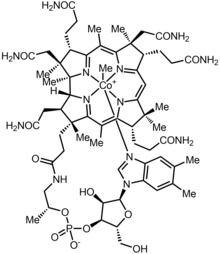
| Формула | C 63 H 91 Co N 13 O 14 P |
| Молярная масса | 1 344 .405 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
| | |
Метилкобаламин (мекобаламин, MeCbl или MeB 12 ) представляет собой кобаламин , форму витамина B 12 . Он отличается от цианокобаламина тем, что цианогруппа у кобальта заменена метильной группой . [1] Метилкобаламин имеет октаэдрический центр кобальта (III) и может быть получен в виде ярко-красных кристаллов. [2] С точки зрения координационной химии , метилкобаламин примечателен как редкий пример соединения, содержащего металл-алкильные связи. Никель- метиловые промежуточные соединения были предложены для заключительной стадии метаногенеза .
Метилкобаламин эквивалентно физиологически витамина B 12 , [3] и могут быть использованы для предотвращения или лечения патологии , возникающие из - за недостатка витамина В 12 приема ( витамин B 12 недостаточности ).
Метилкобаламин также используется при лечении периферической нейропатии , диабетической невропатии и в качестве предварительного лечения бокового амиотрофического склероза . [4]
Метилкобаламин, который попадает в организм, не используется непосредственно в качестве кофактора, а сначала превращается MMACHC в аламин cob (II). Затем аламин Cob (II) превращается в две другие формы, аденозилкобаламин и метилкобаламин для использования в качестве кофакторов. То есть метилкобаламин сначала деалкилируется, а затем регенерируется. [5] [6] [7]
По словам одного автора, важно лечить дефицит витамина B 12 с помощью гидроксокобаламина или цианокобаламина или комбинации аденозилкобаламина и метилкобаламина, а не только метилкобаламина. [8]
Производство [ править ]
Метилкобаламин может быть получен в лаборатории за счетом снижения цианокобаламина с боргидридом натрия в щелочном растворе, с последующим добавлением метилйодида . [2]
Функции [ править ]
Этот витамер является одним из двух активных коферментов, используемых витамином B 12 -зависимыми ферментами, и специфической формой витамина B 12, используемой 5-метилтетрагидрофолат-гомоцистеинметилтрансферазой (MTR), также известной как метионинсинтаза. [ необходима цитата ]
Метилкобаламин участвует в пути Вуда-Люнгдаля , который представляет собой путь, по которому некоторые организмы используют углекислый газ в качестве источника органических соединений. На этом пути метилкобаламин обеспечивает метильную группу, которая соединяется с монооксидом углерода (полученным из CO 2 ) с образованием ацетил-КоА . Ацетил-КоА - это производное уксусной кислоты, которое превращается в более сложные молекулы, как того требует организм. [9]
Метилкобаламин вырабатывается некоторыми бактериями . [ необходима цитата ] Он играет важную роль в окружающей среде. В окружающей среде он отвечает за биометилирование некоторых тяжелых металлов . Например, высокотоксичная метилртуть образуется под действием метилкобаламина. [10] В этой роли, метилкобаламин служит в качестве источника «CH 3 + ».
Недостаток кобаламина может привести к мегалобластной анемии и подострой комбинированной дегенерации спинного мозга. [11]
См. Также [ править ]
- Кобамамид
- Цианокобаламин
- Гидроксокобаламин
- Витамин B12
- Биосинтез кобаламина
Ссылки [ править ]
- ^ Макдауэлл LR (2000-10-11). Витамины в пище животных и человека . Booksgoogle.com . ISBN 9780813826301. Проверено 28 января 2018 .
- ^ a b Приготовление восстановленных форм витамина B 12 и некоторых аналогов кофермента витамина B 12, содержащих кобальт-углеродную связь. Д. Б. Маккормик и Л. Д. Райт, ред . 1971; Т. XVIII: 34-54. DOI : 10.1016 / S0076-6879 (71) 18006-8 .
- ↑ Sil A, Kumar H, Mondal RD, Anand SS, Ghosal A, Datta A, Sawant SV, Kapatkar V, Kadhe G, Rao S (июль 2018 г.). «Рандомизированное открытое исследование, сравнивающее сывороточные уровни кобаламина после трех доз по 500 мкг против однократной дозы метилкобаламина в 1500 мкг у пациентов с периферической невропатией» . Корейский журнал боли . 31 (3): 183–190. DOI : 10.3344 / kjp.2018.31.3.183 . PMC 6037815 . PMID 30013732 .
- ^ «Eisai представляет новую заявку на лекарство для препарата сверхвысокой дозы мекобаламина в качестве лечения бокового амиотрофического склероза в Японии» (PDF) . Eisai.com . Проверено 28 января 2018 .
- ^ Ким Дж, Ганнибал л, Герасим С, Джекобсен DW, Бэнерджи R (ноябрь 2009 г.). «Человеческий белок с витамином B12 использует активность глутатионтрансферазы для обработки алкилкобаламинов» . Журнал биологической химии . 284 (48): 33418–24. DOI : 10.1074 / jbc.M109.057877 . PMC 2785186 . PMID 19801555 .
- ↑ Hannibal L, Kim J, Brasch NE, Wang S, Rosenblatt DS, Banerjee R, Jacobsen DW (август 2009 г.). «Обработка алкилкобаламинов в клетках млекопитающих: роль продукта гена MMACHC (cblC)» . Молекулярная генетика и метаболизм . 97 (4): 260–6. DOI : 10.1016 / j.ymgme.2009.04.005 . PMC 2709701 . PMID 19447654 .
- ^ Фреза DS, Гравий RA (ноябрь 2010). «Генетические нарушения обмена витамина B₁₂: восемь групп комплементации - восемь генов» . Обзоры экспертов в области молекулярной медицины . 12 : e37. DOI : 10.1017 / S1462399410001651 . PMC 2995210 . PMID 21114891 .
- ^ Thakkar K, Billa G (январь 2015). «Лечение дефицита витамина B12 - метилкобаламин? Цианкобаламин? Гидроксокобаламин? - устранение путаницы» . Европейский журнал клинического питания . 69 (1): 1–2. DOI : 10.1038 / ejcn.2014.165 . PMID 25117994 .
- ^ Fontecilla-Camps JC, Amara P, Cavazza C, Nicolet Y, Volbeda A (август 2009). «Структурно-функциональные отношения анаэробных металлоферментов газопереработки». Природа . 460 (7257): 814–22. Bibcode : 2009Natur.460..814F . DOI : 10,1038 / природа08299 . PMID 19675641 .
- ^ Schneider Z, Stroiński A (1987), Комплексный B12: химия, биохимия, питание, экология, медицина , ISBN 9783110082395
- ^ Bémeur C, et al. (2011). Blass JP (ред.). Нейрохимические механизмы в болезни . Springer. С. 112 –3.