| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Бутан [3] | |||
| Систематическое название ИЮПАК Тетракарбан (никогда не рекомендуется [3] ) | |||
| Другие имена | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 969129 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.136 | ||
| Номер ЕС |
| ||
| Номер E | E943a (глазурь, ...) | ||
| 1148 | |||
| КЕГГ | |||
| MeSH | бутан | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1011 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 4 Н 10 | |||
| Молярная масса | 58,124 г · моль -1 | ||
| Внешность | Бесцветный газ | ||
| Запах | Подобное бензину или природному газу [1] | ||
| Плотность | 2,48 кг / м 3 (при 15 ° C (59 ° F)) | ||
| Температура плавления | От -140 до -134 ° С; От -220 до -209 ° F; 133–139 К | ||
| Точка кипения | От -1 до 1 ° С; От 30 до 34 ° F; От 272 до 274 К | ||
Растворимость в воде | 61 мг л -1 (при 20 ° C (68 ° F)) | ||
| журнал P | 2,745 | ||
| Давление газа | ~ 170 кПа при 283 К [4] | ||
Константа закона Генри ( k H ) | 11 нмоль Па -1 кг -1 | ||
| Конъюгированная кислота | Бутан | ||
Магнитная восприимчивость (χ) | -57,4 · 10 −6 см 3 / моль | ||
| Термохимия | |||
Теплоемкость ( C ) | 98.49 Дж -1 моль -1 | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | −126,3–−124,9 кДж моль −1 | ||
Std энтальпии сгорания (Δ с Н ⦵ 298 ) | −2,8781–−2,8769 МДж моль −1 | ||
| Опасности [5] | |||
| Паспорт безопасности | См .: страницу данных | ||
| Пиктограммы GHS | |||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H220 | ||
Меры предосторожности GHS | P210 | ||
| NFPA 704 (огненный алмаз) |  1 4 0 SA | ||
| точка возгорания | -60 ° С (-76 ° F, 213 К) | ||
самовоспламенения температуру | 405 ° С (761 ° F, 678 К) | ||
| Пределы взрываемости | 1,8–8,4% | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | нет [1] | ||
REL (рекомендуется) | TWA 800 частей на миллион (1900 мг / м 3 ) [1] | ||
IDLH (Непосредственная опасность) | 1600 частей на миллион [1] | ||
| Родственные соединения | |||
Родственные алканы |
| ||
Родственные соединения | Перфторбутан | ||
| Страница дополнительных данных | |||
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. | ||
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ | ||
Спектральные данные | УФ , ИК , ЯМР , МС | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
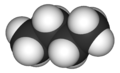
Бутан ( / б JU т eɪ п / ) или п -бутан представляет собой алкан с формулой С 4 Н 10 . Бутан - это газ при комнатной температуре и атмосферном давлении. Бутан - легковоспламеняющийся, бесцветный, легко сжижаемый газ, который быстро испаряется при комнатной температуре. Название бутан происходит от корней but- (от масляной кислоты , названной в честь греческого слова, обозначающего масло) и -ane . Он был открыт химиком Эдвардом Франкландом в 1849 году. [6]Он был обнаружен растворенным в сырой нефти в 1864 году Эдмундом Рональдсом , который первым описал его свойства. [7] [8]
Изомеры [ править ]
| Распространенное имя | нормальный бутан неразветвленный бутан н -бутан | изобутан и -бутан |
| Название ИЮПАК | бутан | метилпропан |
| Молекулярная диаграмма | ||
Диаграмма скелета |
Вращение вокруг центральной С-С связи производит два различных конформаций ( транс и гош ) для п изобутан. [9]
Реакции [ править ]
Когда кислорода много, бутан горит с образованием углекислого газа и водяного пара; когда кислород ограничен, также может образоваться углерод ( сажа ) или монооксид углерода . Бутан плотнее воздуха.
Когда кислорода достаточно:
- 2 C 4 H 10 + 13 O 2 → 8 CO 2 + 10 H 2 O
Когда кислород ограничен:
- 2 C 4 H 10 + 9 O 2 → 8 CO + 10 H 2 O
По весу бутан содержит около 49,5 МДж / кг (13,8 кВтч / кг; 22,5 МДж / фунт ) или по объему жидкости 29,7 мегаджоулей на литр (8,3 кВтч / л; 112 МДж / галлон США; 107000 БТЕ / галлон США).
Максимальная адиабатическая температура пламени бутана с воздухом составляет 2243 К (1970 ° C; 3578 ° F).
н- Бутан является сырьем для каталитического процесса DuPont для получения малеинового ангидрида :
- 2 СН 3 СН 2 СН 2 СН 3 + 7 О 2 → 2 С 2 Н 2 (СО) 2 О + 8 Н 2 О
н- Бутан, как и все углеводороды, подвергается свободнорадикальному хлорированию, давая как 1-хлор-, так и 2-хлорбутаны, а также более сильно хлорированные производные. Относительные скорости хлорирования частично объясняются разными энергиями диссоциации связи , 425 и 411 кДж / моль для двух типов связей CH.
Использует [ редактировать ]
Нормальный бутан может использоваться для смешивания бензина в качестве топливного газа, растворителя для экстракции ароматизаторов, отдельно или в смеси с пропаном , а также в качестве сырья для производства этилена и бутадиена , ключевого ингредиента синтетического каучука . Изобутан в основном используется нефтеперерабатывающими заводами для повышения (увеличения) октанового числа автомобильного бензина. [10] [11] [12] [13]
При смешивании с пропаном и другими углеводородами он может называться LPG для сжиженного нефтяного газа. Он используется в качестве компонента бензина, в качестве сырья для производства основных нефтехимических продуктов при паровом крекинге , в качестве топлива для зажигалок и в качестве пропеллента в аэрозольных распылителях, таких как дезодоранты . [14]
Очень чистые формы бутана, особенно изобутана, могут использоваться в качестве хладагентов и в значительной степени заменили галометаны , разрушающие озоновый слой , например, в бытовых холодильниках и морозильниках. Рабочее давление в системе для бутана ниже, чем для галометанов, таких как R-12 , поэтому системы R-12, такие как автомобильные системы кондиционирования воздуха, при преобразовании в чистый бутан не будут работать оптимально, и, следовательно, смесь изобутана и пропана используется для обеспечения производительности системы охлаждения, сравнимой с R-12.
Бутан также используется в качестве более легкого топлива для обычной зажигалки или бутановой горелки и продается в бутылках в качестве топлива для приготовления пищи, барбекю и походных печей. На мировом рынке канистр с бутаном доминируют производители из Южной Кореи . [15]
В качестве топлива его часто смешивают с небольшими количествами сероводорода и меркаптанов, которые придают несгоревшему газу неприятный запах, который легко уловить человеческим носом. Таким образом можно легко определить утечку бутана. Хотя сероводород и меркаптаны токсичны, они присутствуют в таких низких количествах, что опасность удушья и возгорания бутаном становится проблемой задолго до токсичности. [16] [17] Наиболее коммерчески доступный бутан также содержит определенное количество загрязняющего масла, которое может быть удалено путем фильтрации, но которое в противном случае оставит отложение в точке воспламенения и может в конечном итоге заблокировать равномерный поток газа. [18] Бутан, используемый для экстракции ароматизаторов, не содержит этих загрязняющих веществ.[19] и газы бутан могут вызвать взрыв газа в плохо вентилируемых помещениях, если утечки остаются незамеченными и воспламеняются от искры или пламени. [5]
| Канистры бутанового топлива для использования в походных печах. | Бутановая зажигалка с резервуаром для жидкого бутана | Аэрозольный баллончик, в котором в качестве пропеллента может использоваться бутан. | Баллон с бутаном, используемый для приготовления пищи |
Эффекты и проблемы со здоровьем [ править ]
Вдыхание бутана может вызвать эйфорию , сонливость , потерю сознания , асфиксию , сердечную аритмию , колебания артериального давления и временную потерю памяти при злоупотреблении непосредственно из контейнера под высоким давлением и может привести к смерти от удушья и фибрилляции желудочков . Он попадает в кровоток и в течение нескольких секунд вызывает интоксикацию. [20] Бутан является наиболее распространенным летучим веществом в Великобритании и был причиной 52% смертей, связанных с растворителями, в 2000 году. [21]Распыляя бутан прямо в горло, струя жидкости может быстро охладиться до -20 ° C (-4 ° F) за счет расширения, вызывая длительный ларингоспазм . [22] Синдром « внезапной смерти сниффера », впервые описанный Бассом в 1970 г. [23], является наиболее частой причиной смерти, связанной с растворителями, приводя к 55% известных смертельных случаев. [22]
См. Также [ править ]
- Изобутан
- Циклобутан
- Диметиловый эфир
- Злоупотребление летучими веществами
- Бутан (страница данных)
- Бутанон
- н- бутанол
- Сжиженный газ
- Промышленный газ
- Бутановая горелка
- Взрывы газа
Ссылки [ править ]
- ^ a b c d e Карманный справочник NIOSH по химической опасности. «# 0068» . Национальный институт охраны труда и здоровья (NIOSH).
- ↑ Хофманн, Август Вильгельм Фон (1 января 1867 г.). «I. О действии трихлорида фосфора на соли ароматических монаминов». Труды Лондонского королевского общества . 15 : 54–62. DOI : 10.1098 / rspl.1866.0018 . S2CID 98496840 .
- ^ a b «Передний вопрос». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 4. DOI : 10.1039 / 9781849733069-FP001 . ISBN 978-0-85404-182-4.
Точно так же сохраненные названия «этан», «пропан» и «бутан» никогда не заменялись систематическими названиями «дикарбан», «трикарбан» и «тетракарбан», как рекомендовано для аналогов силана, «дисилана»; фосфан, трифосфан; и сульфан, «тетрасульфан».
- ↑ WB Kay (1940). «Соотношение давление-объем-температура для н-бутана». Промышленная и инженерная химия . 32 (3): 358–360. DOI : 10.1021 / ie50363a016 .
- ^ a b «Паспорт безопасности, название материала: N-бутан» (PDF) . США: Matheson Tri-Gas Incorporated. 5 февраля 2011. Архивировано из оригинального (PDF) 1 октября 2011 года . Проверено 11 декабря 2011 года .
- ↑ Рассел, Колин А. (20 марта 2009 г.). "Франкленд - первый химик-металлоорганизм" (PDF) . Шестая лекция Уиллера . Королевское химическое общество. Архивировано 17 апреля 2017 года. CS1 maint: неподходящий URL ( ссылка )
- ^ Watts, H .; Мьюир, MMP; Морли, HF (1894). Химический словарь Уоттса . Химический словарь Уоттса. Лонгманс, Грин. п. 385.
- ^ Maybery, CF (1896). «О составе серных нефтей Огайо и Канады». Труды Американской академии искусств и наук . 31 : 1–66. DOI : 10.2307 / 20020618 . JSTOR 20020618 .
- ↑ Роман М. Балабин (2009). «Разница энтальпии между конформациями нормальных алканов: исследование спектроскопии комбинационного рассеяния н- пентана и н- бутана». J. Phys. Chem. . 113 (6): 1012–9. DOI : 10.1021 / jp809639s . PMID 19152252 .
- ^ MarkWest Energy Partners, форма 10-K LP . Sec.gov
- ^ Copano Energy, LLC Форма 10-K . Sec.gov. Проверено 12 декабря 2012.
- ^ Targa Resources Partners LP Form10-k . Sec.gov. Проверено 12 декабря 2012.
- ^ Crosstex Energy, LP ФОРМА 10-K . Sec.gov
- ^ Учебник по смешиванию бензина . Информационный меморандум EPRINC
- ^ «Предприниматель преодолел невзгоды китайской тюрьмы» . houstonchronicle.com . 21 июня 2016 . Проверено 20 сентября 2018 года .
- ↑ Грешэм, Чип (16 ноября 2019 г.). «Токсичность сероводорода: основы практики, патофизиология, этиология» . Ссылка на Medscape . Проверено 22 марта 2021 года .
- ^ Комитет по нормативам острой экспозиции; Комитет по токсикологии; Совет по экологическим исследованиям и токсикологии; Отдел исследований Земли и жизни; Национальный исследовательский совет (26 сентября 2013 г.). 2. Нормативные уровни острого воздействия метилмеркаптана . Книжная полка NCBI .CS1 maint: несколько имен: список авторов ( ссылка )
- ^ "BHO Mystery Oil" . Сканк Фарм Исследования . 2013-08-26 . Проверено 5 декабря 2019 .
- ^ «Окончательный отчет об оценке безопасности изобутана, изопентана, н-бутана и пропана». Журнал Американского колледжа токсикологии . Публикации SAGE. 1 (4): 127–142. 1982. DOI : 10,3109 / 10915818209021266 . ISSN 0730-0913 .
- ^ «Нейротоксические эффекты от бутанового газа» . thcfarmer.com. 19 декабря 2009 . Проверено 3 октября +2016 .
- ^ Филд-Смит М., Бланд Дж. М., Тейлор Дж. С. и др. «Тенденции смертности, связанной со злоупотреблением летучими веществами, 1971–2004» (PDF) . Департамент наук об общественном здравоохранении. Лондон: Медицинская школа Святого Георгия. Архивировано из оригинального (PDF) 27 марта 2007 года.
- ^ а б Рэмси Дж., Андерсон Х.Р., Блур К. и др. (1989). «Введение в практику, распространенность и химическую токсикологию злоупотребления летучими веществами». Hum Toxicol . 8 (4): 261–269. DOI : 10.1177 / 096032718900800403 . PMID 2777265 . S2CID 19617950 .
- ↑ Басс М. (1970). «Внезапная нюхательная смерть». ДЖАМА . 212 (12): 2075–2079. DOI : 10,1001 / jama.1970.03170250031004 . PMID 5467774 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме Бутана . |
- Международная карта химической безопасности 0232
- Карманный справочник NIOSH по химической опасности