 | |
 | |
| Имена | |
|---|---|
| Систематическое название ИЮПАК Перманганат | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
PubChem CID | |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| MnO- 4 | |
| Молярная масса | 118,934 г · моль -1 |
| Конъюгированная кислота | Пермангановая кислота |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
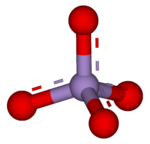
Перманганата это общее название для химического соединения , содержащего манганат (VII) ион , ( MnO-
4). Поскольку марганец находится в степени окисления +7 , перманганат-ион (VII) является сильным окислителем . Ион имеет тетраэдрическую геометрию . [1] Растворы перманганата имеют пурпурный цвет и стабильны в нейтральной или слабощелочной среде. Точная химическая реакция зависит от присутствующих органических загрязнителей и используемого окислителя. Например, трихлорэтан (C 2 H 3 Cl 3 ) окисляется перманганат-ионами с образованием диоксида углерода (CO 2 ), диоксида марганца (MnO 2 ), ионов водорода (H + ) и ионов хлорида (Cl -). [2]
- 8 MnO-
4+ 3 С
2ЧАС
3Cl
3→ 6 СО
2+ 8 MnO
2+ H+
+ 4 часа
2O + 9 Cl-
В кислом растворе перманганат (VII) восстанавливается до бледно-розовой степени окисления +2 иона марганца (II) (Mn 2+ ).
- 8 часов+
+ MnO-
4+ 5 е - → Mn 2+ + 4 H 2 O
В сильно щелочном растворе перманганат (VII) восстанавливается до зеленой +6 степени окисления манганат- иона MnO.2-
4.
- MnO-
4+ е - → MnO2-
4
Однако в нейтральной среде он восстанавливается до коричневой степени окисления +4 диоксида марганца MnO 2 .
- 2 Н 2 О + MnO-
4+ 3 e - → MnO 2 + 4 OH -
Производство [ править ]
Перманганаты могут быть получены путем окисления соединений марганца, таких как хлорид марганца или сульфат марганца , сильными окислителями, например, гипохлоритом натрия или диоксидом свинца :
- 2 MnCl 2 + 5 NaClO + 6 NaOH → 2 NaMnO 4 + 9 NaCl + 3 H 2 O
- 2 MnSO 4 + 5 PbO 2 + 3 H 2 SO 4 → 2 HMnO 4 + 5 PbSO 4 + 2 H 2 O
Он также может быть получен путем диспропорционирования из манганатов , с диоксидом марганца в качестве побочного продукта:
- 3 Na 2 MnO 4 + 2 H 2 O → 2 NaMnO 4 + MnO 2 + 4 NaOH
Их производят в промышленных масштабах путем электролиза или окисления на воздухе щелочных растворов манганатных солей ( MnO2-
4). [3]
Свойства [ править ]
Перманганаты (VII) являются солями из марганцовой кислоты . Они имеют темно-фиолетовый цвет из-за перехода заряда . Перманганат (VII) - сильный окислитель , похожий на перхлорат . Поэтому он широко используется в качественном анализе, который включает окислительно-восстановительные реакции ( перманганометрия ). Согласно теории, перманганат достаточно силен, чтобы окислять воду, но на самом деле этого не происходит ни в какой степени. Кроме того, он стабилен.
Это полезный реагент, хотя он не очень селективен к органическим соединениям. Перманганат калия используется как дезинфицирующее средство и добавка для очистки воды в аквакультуре. [4]
Манганаты (VII) термически не очень стабильны. Например, перманганат калия разлагается при 230 ° C на манганат калия и диоксид марганца , выделяя газообразный кислород :
- 2 KMnO 4 → K 2 MnO 4 + MnO 2 + O 2
Перманганата может окислять собой амин в нитросоединения , [5] [6] спирт до кетона , [7] альдегид до карбоновой кислоты , [8] [9] терминал алкен к карбоновой кислоте , [10] щавелевая кислота с диоксидом углерода , [11] и алкен до диола . [12] Этот список не является исчерпывающим.
При окислении алкена одним промежуточным продуктом является циклическая разновидность Mn (V) [ ссылка ] :
Соединения [ править ]
- Перманганат аммония , NH 4 MnO 4
- Перманганат кальция , Ca (MnO 4 ) 2
- Перманганат калия , KMnO 4
- Перманганат натрия , NaMnO 4
- Перманганат серебра , AgMnO 4
См. Также [ править ]
- Перхлорат , аналогичный ион с центром хлора (VII)
- Хромат , изоэлектронный перманганату
- Пертехнетат
Ссылки [ править ]
- ^ Сукалян Даш, Сабита Патель и Биджай К. Мишра (2009). «Окисление перманганатом: синтетические и механистические аспекты». Тетраэдр . 65 (4): 707–739. DOI : 10.1016 / j.tet.2008.10.038 .
- ^ http://geocleanse.com/permanaganate.asp
- ^ Коттон, Ф. Альберт; Уилкинсон, Джеффри; Карлос А. Мурильо; Манфред Бохманн (1999). Высшая неорганическая химия (6-е изд.). Нью-Йорк: John Wiley & Sons, Inc., стр. 770. ISBN 978-0471199571.
- ^ Зиндель. «Дезинфицирующее средство на основе перманганата калия и натрия» .
- ↑ A. Calder, AR Forrester1 и SP Hepburn (1972). «2-метил-2-нитрозопропан и его димер» . Органический синтез . 6 : 803.CS1 maint: несколько имен: список авторов ( ссылка ); Сборник , 52 , с. 77
- ^ Натан Корнблюм и Уиллард Дж. Джонс (1963). «4-нитро-2,2,4-триметилпентан» . Органический синтез . 5 : 845.; Сборник , 43 , с. 87
- ^ JW Корнфорт (1951). «Этилпируват» . Органический синтез . 4 : 467.; Сборник , 31 , стр. 59
- ^ RL Shriner и EC Kleiderer (1930). «Пиперониловая кислота» . Органический синтез . 2 : 538.; Сборник , 10 , стр. 82
- ^ Джон Р. Рухофф (1936). «н-гептановая кислота» . Органический синтез . 2 : 315.; Сборник , 16 , стр. 39
- ^ Дональд Г. Ли, Шеннон Э. Лэмб и Виктор С. Чанг (1981). «Карбоновые кислоты от окисления концевых алкенов перманганатом: нонадекановая кислота» . Органический синтез . 7 : 397.CS1 maint: несколько имен: список авторов ( ссылка ); Сборник , 60 , стр. 11
- Перейти ↑ Kovacs KA, Grof P, Burai L, Riedel M (2004). «Пересмотр механизма реакции перманганат / оксалат». J. Phys. Chem. . 108 (50): 11026. Bibcode : 2004JPCA..10811026K . DOI : 10.1021 / jp047061u .
- ^ EJ Witzemann, Wm. Ллойд Эванс, Генри Хасс и Э. Ф. Шредер (1931). «этилацеталь dl-глицеральдегида» . Органический синтез . 2 : 307.CS1 maint: несколько имен: список авторов ( ссылка ); Коллективный том , 11 , с. 52