Эта статья включает в себя список общих ссылок , но он остается в значительной степени непроверенным, поскольку в нем отсутствует достаточное количество соответствующих встроенных ссылок . ( Июль 2014 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
Метаболизм пуринов относится к метаболическим путям синтеза и расщепления пуринов , которые присутствуют во многих организмах.
Биосинтез [ править ]
Пурины синтезируются биологически в виде нуклеотидов и, в частности, в виде риботидов, то есть оснований, прикрепленных к рибозо-5-фосфату . И аденин, и гуанин являются производными нуклеотид- инозинмонофосфата (IMP), который является первым соединением в метаболическом пути, которое имеет полностью сформированную пуриновую кольцевую систему.
IMP [ править ]
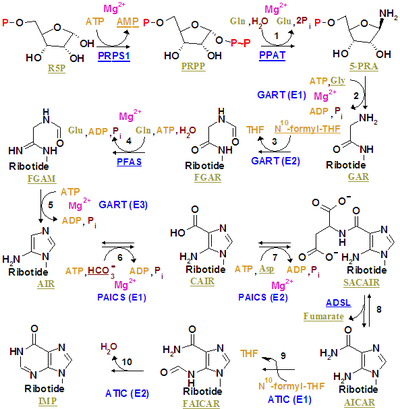
Монофосфат инозина синтезируется на уже существующем рибозофосфате сложным путем (как показано на рисунке справа). Источники атомов углерода и азота пуринового кольца, 5 и 4 соответственно, происходят из нескольких источников. Аминокислота глицин вносит все свои атомы углерода (2) и азота (1) с дополнительными атомами азота из глутамина (2) и аспарагиновой кислоты (1) и дополнительными атомами углерода из формильных групп (2), которые переносятся из кофермент тетрагидрофолат в виде 10-формилтетрагидрофолата и атом углерода из бикарбоната(1). Формильные группы образуют углерод-2 и углерод-8 в пуриновой кольцевой системе, которые действуют как мосты между двумя атомами азота.
Ключевым регуляторным этапом является производство 5-фосфо-α- D- рибозил-1-пирофосфата ( PRPP ) рибозофосфатпирофосфокиназой , которая активируется неорганическим фосфатом и инактивируется пуриновыми рибонуклеотидами. Это не обязательная стадия синтеза пурина, потому что PRPP также используется в синтезе пиримидина и в путях восстановления.
Первым обязательным этапом является реакция PRPP, глутамина и воды с 5'-фосфорибозиламином (PRA), глутаматом и пирофосфатом, катализируемая амидофосфорибозилтрансферазой , которая активируется PRPP и ингибируется AMP , GMP и IMP .
PRPP + L-глутамин + H 2 O → PRA + L-глутамат + PPi
На второй стадии реагируют PRA , глицин и АТФ с образованием GAR , ADP и пирофосфата, катализируемые фосфорибозиламин-глицинлигазой (GAR-синтетазой). Из-за химической лабильности PRA, период полураспада которого составляет 38 секунд при pH 7,5 и 37 ° C, исследователи предположили, что соединение направляется от амидофосфорибозилтрансферазы к GAR-синтетазе in vivo. [1]
PRA + глицин + ATP → GAR + ADP + Pi
Третий катализируется фосфорибозилглицинамид формилтрансферазой .
GAR + fTHF → fGAR + THF
Четвертый катализируется фосфорибозилформилглицинамидинсинтазой .
fGAR + L-глутамин + ATP → fGAM + L-глутамат + ADP + Pi
Пятый катализируется синтетазой AIR (циклаза FGAM) .
fGAM + АТФ → ВОЗДУХ + АДФ + Pi + H 2 O
Шестой катализируется фосфорибозиламиноимидазолкарбоксилазой .
ВОЗДУХ + CO 2 → CAIR + 2H +
Седьмой катализируется фосфорибозиламиноимидазолесукцинокарбоксамидсинтазой .
CAIR + L-аспартат + АТФ → SAICAR + ADP + Pi
Восьмерка катализируется аденилосукцинатлиазой .
SAICAR → AICAR + Фумарат
Продукты AICAR и фумарат идут двумя разными путями. AICAR служит реагентом для девятой стадии, в то время как фумарат транспортируется в цикл лимонной кислоты, который затем может пропустить стадии выделения диоксида углерода для получения малата. Превращение фумарата в малат катализируется фумаразой. Таким образом, фумарат связывает синтез пурина с циклом лимонной кислоты. [2]
Девятый катализируется фосфорибозиламиноимидазолкарбоксамид формилтрансферазой .
AICAR + fTHF → FAICAR + THF
Последняя стадия катализируется инозинмонофосфатсинтазой .
FAICAR → IMP + H 2 O
У эукариот второй, третий и пятый этапы катализируются трифункциональным пуриновым биосинтетическим белком аденозином-3 , который кодируется геном GART.
И девятый, и десятый этапы выполняются одним белком, называемым бифункциональным белком биосинтеза пуринов PURH, кодируемым геном ATIC.
GMP [ править ]
- IMP-дегидрогеназа (IMPDH) превращает IMP в XMP
- GMP-синтаза преобразует XMP в GMP
- GMP-редуктаза преобразует GMP обратно в IMP
AMP [ править ]
- аденилосукцинатсинтаза превращает IMP в аденилосукцинат
- аденилосукцинатлиаза превращает аденилосукцинат в AMP
- Дезаминаза AMP превращает AMP обратно в IMP
Деградация [ править ]
Пурины метаболизируются несколькими ферментами :
Гуанин [ править ]
- Нуклеазы освобождает нуклеотид
- Нуклеотидаза создает гуанозин
- Пуриновая нуклеозидфосфорилаза превращает гуанозин в гуанин
- Гуаназа превращает гуанин в ксантин
- Ксантиноксидаза (форма ксантин оксидоредуктазы) катализирует окисление ксантина до мочевой кислоты.
Аденин [ править ]
- Нуклеазы освобождает нуклеотид
- Нуклеотидаза создает аденозин , то аденозиндезаминаза создает инозин
- Альтернативно, AMP-дезаминаза создает инозиновую кислоту , а затем нуклеотидаза создает инозин.
- Пуриновая нуклеозидфосфорилаза воздействует на инозин с образованием гипоксантина.
- Ксантиноксидаза катализирует биотрансформацию гипоксантина в ксантин.
- Ксантиноксидаза воздействует на ксантин, создавая мочевую кислоту
Регламенты биосинтеза пуриновых нуклеотидов [ править ]
Образование 5'-фосфорибозиаламина из глутамина и PRPP, катализируемое PRPP-аминотрансферазой, является точкой регуляции синтеза пурина. Фермент является аллостерическим ферментом, поэтому он может быть преобразован из IMP, GMP и AMP в высокой концентрации, связывает фермент и оказывает ингибирование, в то время как PRPP в большом количестве связывается с ферментом, вызывающим активацию. Итак, IMP, GMP и AMP являются ингибиторами, а PRPP - активатором. Между образованием 5'-фосфорибозила, аминоимидазола и ИМФ нет известной стадии регуляции.
Утиль [ править ]
Пурины из оборота клеточных нуклеиновых кислот (или из пищи) также могут быть спасены и повторно использованы в новых нуклеотидах.
- Фермент аденинфосфорибозилтрансфераза (APRT) спасает аденин .
- Фермент гипоксантин-гуанинфосфорибозилтрансфераза (HGPRT) спасает гуанин и гипоксантин . [3] (Генетический дефицит HGPRT вызывает синдром Леша – Найхана .)
Заболевания [ править ]
Когда дефектный ген вызывает появление пробелов в метаболическом процессе рециркуляции пуринов и пиримидинов, эти химические вещества не метаболизируются должным образом, и взрослые или дети могут страдать от одного из двадцати восьми наследственных заболеваний, некоторые из которых, возможно, еще неизвестны. Симптомы могут включать подагру , анемию, эпилепсию, задержку развития, глухоту, компульсивное прикусывание, почечную недостаточность или камни или потерю иммунитета.
Метаболизм пуринов может иметь дисбаланс, который может возникать из-за включения вредных нуклеотидных трифосфатов в ДНК и РНК, что в дальнейшем приводит к генетическим нарушениям и мутациям и, как следствие, вызывает несколько типов заболеваний. Некоторые из болезней:
- Тяжелый иммунодефицит из-за потери аденозиндезаминазы.
- Гиперурикемия и синдром Леша – Найхана из-за потери гипоксантин-гуанинфосфорибозилтрансферазы.
- Различные виды рака из-за увеличения активности ферментов, таких как дегидрогеназа IMP. [4]
Фармакотерапия [ править ]
Модуляция пуринового обмена имеет фармакотерапевтическое значение.
Ингибиторы синтеза пуринов подавляют пролиферацию клеток, особенно лейкоцитов . Эти ингибиторы включают азатиоприн , иммунодепрессант, используемый при трансплантации органов , аутоиммунное заболевание, такое как ревматоидный артрит, или воспалительное заболевание кишечника, такое как болезнь Крона и язвенный колит .
Микофенолятмофетил - иммунодепрессант, используемый для предотвращения отторжения при трансплантации органов; он подавляет синтез пурина, блокируя инозитолмонофосфатдегидрогеназу. Также метотрексат косвенно подавляет синтез пурина, блокируя метаболизм фолиевой кислоты (он является ингибитором дигидрофолатредуктазы ).
Аллопуринол - это лекарство, которое ингибирует фермент ксантин оксидоредуктазу и, таким образом, снижает уровень мочевой кислоты в организме. Это может быть полезно при лечении подагры, заболевания, вызванного избытком мочевой кислоты, образующей кристаллы в суставах.
См. Также [ править ]
- Пуринергическая сигнализация
- Модифицирующий заболевание противоревматический препарат (DMARD)
Ссылки [ править ]
- ^ Antle В.Д., Лю Д, Маккеллар БР, Caperelli СА, Хуа М, Винс R (апрель 1996 г.). «Субстратная специфичность глицинамидрибонуклеотидсинтетазы из куриной печени» . Журнал биологической химии . 271 (14): 8192–5. DOI : 10.1074 / jbc.271.14.8192 . PMID 8626510 .
- ^ Garrett RH, Гришэм CM (2016-02-11). Биохимия (Шестое изд.). Бостон, Массачусетс. стр. 666 и 934. ISBN 9781305577206. OCLC 914290655 .
- ^ Ансари МОИ, Equbal А, Dikhit MR, R - Мансури, Рана S, Али В, и др. (Февраль 2016 г.). «Установление корреляции между тестовым анализом in-silico и in vitro против Leishmania HGPRT к ингибиторам». Международный журнал биологических макромолекул . 83 : 78–96. DOI : 10.1016 / j.ijbiomac.2015.11.051 . PMID 26616453 .
- ^ Пэнг Б., Макфалин Дж. Л., Берджис Н. Э., Донг М., Тагизаде К., Салливан М. Р. и др. (Февраль 2012 г.). «Дефекты метаболизма пуриновых нуклеотидов приводят к существенному включению ксантина и гипоксантина в ДНК и РНК» . Труды Национальной академии наук Соединенных Штатов Америки . 109 (7): 2319–24. Bibcode : 2012PNAS..109.2319P . DOI : 10.1073 / pnas.1118455109 . JSTOR 41477470 . PMC 3289290 . PMID 22308425 .
Внешние ссылки [ править ]
- Страница медицинской биохимии
- Метаболизм пуринов - контрольный путь
- PUMPA: Ассоциация пациентов с метаболизмом пуринов