 | |
 | |
| Имена | |
|---|---|
| Другие имена Теллурит натрия IV, динатриевая соль теллуристой кислоты | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.231 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| Na 2 TeO 3 | |
| Молярная масса | 221,57774 г / моль |
| Внешность | белые кристаллы, порошок |
| Плотность | 6,245 г / см 3 |
| Температура плавления | 710 ° С (1310 ° F, 983 К) |
| Точка кипения | неизвестно (очень высокий) |
| растворим больше или равно 100 мг / мл при 68 ° F | |
| Структура | |
| ромбический | |
| Опасности | |
| R-фразы (устаревшие) | R23 R24 R25 |
| S-фразы (устаревшие) | S22 S36 S37 S39 S45 |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 83 мг / кг (крыса, перорально) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Теллурит натрия - это неорганическое соединение теллура с формулой Na 2 TeO 3 . Это водорастворимое твердое вещество белого цвета и слабый восстановитель . Теллурит натрия является промежуточным продуктом при извлечении элемента, теллура; это продукт, получаемый из анодных шламов и предшественник теллура.
Подготовка [ править ]
Основным источником теллура являются медные анодные шламы, содержащие драгоценные металлы, а также различные теллуриды. Эти шламы обжигаются с карбонатом натрия и кислородом для получения теллурита натрия. [1]
- Ag 2 Te + Na 2 CO 3 + O 2 → 2Ag + Na 2 TeO 3 + CO 2 (400–500 ° C)
Это реакция с теллуридом серебра. Теллурид окисляется до теллурита, а серебро (I) восстанавливается до серебра.
Очищение [ править ]
Электролиз раствора теллурита урожайности очищает теллур. [1]
- Анод: 4OH - → 2H 2 O + O 2 + 4e -
- Катод: TeO 3 2− + 3H 2 O + 4e - → Te + 6OH -
Структура и свойства [ править ]
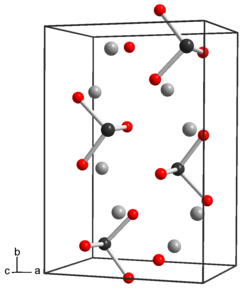
Теллур по свойствам похож на серу и селен. В безводной форме Na 2 TeO 3 атомы теллура имеют 6 координат, три Te-O при 1,87 Å и три при 2,9 Å , с искаженными октаэдрами, имеющими общие края. [2] В пентагидрате Na 2 TeO 3 .5H 2 O присутствуют дискретные анионы теллурита, TeO 3 2- , пирамидальные. Расстояние Te-O составляет 1,85 - 1,86 Å, а угол O-Te-O близок к 99,5 °. [3] Теллурит-анион является слабым основанием. Теллуритно натрий будет похожи на селенит натрия и сульфит натрия. Теллурит натрия является одновременно слабым окислителем и слабым восстановителем.
[ править ]
- H 2 TeO 3 → H + + HTeO 3 - pK 2,48
Теллуровая кислота теряет протон при этом pKa.
- HTeO 3 - → H + + TeO 3 2− pK 7,7
Теллурит водорода теряет протон при этом pKa и становится ионом теллурита. Это могло бы произойти в реакции теллуриновой кислоты с гидроксидом натрия с образованием теллурита натрия.
- TeO 2 + 2OH - → TeO 3 2− + H 2 O
Это реакция диоксида теллура с основанием с образованием соли теллурита.
Приложения [ править ]
Теллурит натрия улучшает коррозионную стойкость никелевых гальванических слоев. Растворы теллурита натрия используются для нанесения черных или сине-черных покрытий на железо, сталь, алюминий и медь. В микробиологии теллурит натрия может быть добавлен в питательную среду для выделения бактерий, обладающих физиологической устойчивостью к его токсичности. [4]
Ссылки [ править ]
- ^ а б Виберг, Эгон; Холлеман, Арнольд Фредерик (2001). Нильс Виберг (ред.). Неорганическая химия . переведена Мэри Иглсон. Академическая пресса. п. 588. ISBN. 0-12-352651-5.
- ^ Masse, R .; Guitel, JC; Торджман, И. (1980). «Приготовление химического вещества и кристаллической структуры теллуритов натрия и вещества: Na 2 TeO 3 , Ag 2 TeO 3 ». Бюллетень материаловедения . 15 (4): 431–436. DOI : 10.1016 / 0025-5408 (80) 90048-3 . ISSN 0025-5408 .
- ^ "Кристаллографический этюд теллурита натрия в чистых молекулах, Na 2 Te IV O 3 · 5H 2 O". Acta Crystallogr. B . 35 : 1337–1340. 1979. DOI : 10,1107 / S0567740879006403 .
- ^ Борсетти, Франческа; Тонинелло, Антонио; Заннони, Давиде (2003). «Поглощение теллурита клетками факультативного фототрофа Rhodobacter capsulatus является pH-зависимым процессом». Федерация европейских биохимических обществ. Volume 554, Issue 3, 20 ноября 2003 г., стр. 315–318. Elsevier BV doi : 10.1016 / S0014-5793 (03) 01180-3
- Cameo Chemicals. Теллурит натрия. Проверено 8 марта 2009 г. Веб-сайт: http://cameochemical.noaa.gov/chemical/5185 .
- Нокерт, Гай (2002). «Теллур и соединения теллура». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a26_177.pub2 .