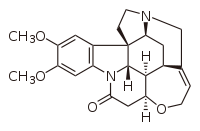
Энантиоселективный синтез
Энантиоселективный синтез , также называемый асимметричным синтезом , [1] представляет собой форму химического синтеза. Он определяется IUPAC как: химическая реакция (или последовательность реакций), в которой один или несколько новых элементов хиральности образуются в молекуле субстрата и которая производит стереоизомерные ( энантиомерные или диастереоизомерные ) продукты в неравных количествах . [2]
Проще говоря: это синтез соединения методом, способствующим образованию определенного энантиомера или диастереомера. Энантиомеры представляют собой стереоизомеры, имеющие противоположные конфигурации в каждом хиральном центре. Диастереомеры — стереоизомеры, отличающиеся одним или несколькими хиральными центрами.
Энантиоселективный синтез является ключевым процессом в современной химии и особенно важен в области фармацевтики , поскольку разные энантиомеры или диастереомеры молекулы часто обладают разной биологической активностью .
Многие строительные блоки биологических систем, такие как сахара и аминокислоты , производятся исключительно в виде одного энантиомера . В результате живые системы обладают высокой степенью химической хиральности и часто по-разному реагируют с различными энантиомерами данного соединения. Примеры этой избирательности включают:
Поскольку такой энантиоселективный синтез имеет большое значение, его также может быть трудно осуществить. Энантиомеры обладают одинаковыми энтальпиями и энтропиями и, следовательно, должны производиться в равных количествах ненаправленным процессом, приводящим к рацемической смеси. Энантиоселективный синтез может быть достигнут за счет использования хирального свойства, которое способствует образованию одного энантиомера вместо другого за счет взаимодействий в переходном состоянии . Это смещение известно как асимметричная индукция и может включать хиральные свойства субстрата , реагента , катализатора или окружающей среды [9] .энергия активации , необходимая для образования одного энантиомера, ниже, чем у противоположного энантиомера. [10]
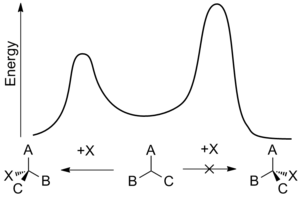
Энантиоселективность обычно определяется относительной скоростью стадии энантиодифференцирования — точки, в которой один реагент может стать одним из двух энантиомерных продуктов. Константа скорости k для реакции является функцией энергии активации реакции, иногда называемой энергетическим барьером , и зависит от температуры. Использование свободной энергии Гиббса энергетического барьера, Δ G *, означает, что относительные скорости противоположных стереохимических результатов при данной температуре T равны:
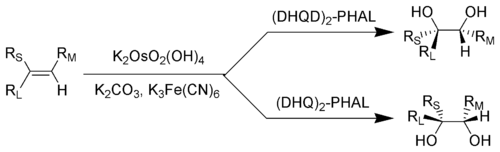
. Ключ: RL = наибольший заместитель; R M = заместитель среднего размера; R S = наименьший заместитель
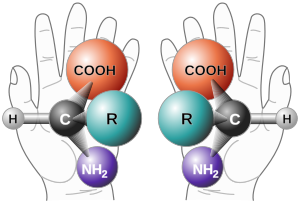

Слева: ( S )-талидомид
Справа: ( R )-талидомид