 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC N , N , N- хлорид триэтилэтанаминия | |
| Другие названия Хлорид тетраэтиламмония N , N , N , N- Хлорид тетраэтиламмония | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.000.243 |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| C 8 H 20 Cl N | |
| Молярная масса | 165,71 г · моль -1 |
| Появление | Бесцветное расплывающееся вещество |
| Плотность | 1,08 г / см 3 [1] |
| Температура плавления | 360 ° C (680 ° F, 633 K) тетрагидрат [1] |
| хорошо растворим | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
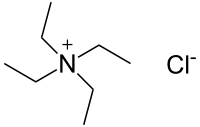
Хлорид тетраэтиламмония ( TEAC ) представляет собой четвертичное аммониевое соединение с химической формулой (C 2 H 5 ) 4 N + Cl - , иногда обозначаемое как Et 4 N + Cl - . По внешнему виду это гигроскопичное бесцветное кристаллическое твердое вещество. Он использовался в качестве источника ионов тетраэтиламмония в фармакологических и физиологических исследованиях, но также используется в органическом химическом синтезе.
Подготовка и структура [ править ]
TEAC получают путем алкилирования триэтиламина этилхлоридом. [2]
TEAC существует в виде одного из двух стабильных гидратов, моногидрата и тетрагидрата. [3] Кристаллическая структура TEAC.H 2 O была определена [4], как и структура тетрагидрата TEAC.4H 2 O. [5]
Подробности получения больших призматических кристаллов TEAC.H 2 O предоставлены Хармоном и Габриэлем, которые провели ИК-спектроскопические исследования этого и родственных соединений. [6] Эти исследователи также отметили, что, хотя свежеочищенный TEAC.H 2 O не содержит гидрохлорида триэтиламина , небольшие количества этого соединения образуются при нагревании TEAC в результате элиминации Хофмана :
- Cl - + H-CH 2 -CH 2 -N + Et 3 → Cl-H + H 2 C = CH 2 + Et 3 N
Синтетические приложения [ править ]
В значительной степени синтетические применения TEAC напоминают применение бромида тетраэтиламмония (TEAB) и йодида тетраэтиламмония (TEAI), хотя одна из солей может быть более эффективной, чем другая в конкретной реакции. Например, TEAC дает более высокие выходы, чем TEAB или TEAI в качестве сокатализатора в реакции получения диарилмочевины из ариламинов , нитроароматических соединений и монооксида углерода . [7]
В других примерах, таких как следующий, TEAC не так эффективен, как TEAB или TEAI:
- 2-гидроксиэтилирования (присоединение -CH 2 -CH 2 -OH) с помощью карбоната этилена из карбоновых кислот и некоторых гетероциклов , имеющих кислотную NH. [8]
- Катализатор фазового переноса в геминальным диалкилировании из флуореных , N, N-диалкилирования из анилина и N-алкилирования карбазола с использованием водного гидроксида натрия и алкилгалогенидов . [9]
Биология [ править ]
Общий с тетраэтиламмонией бромидом и иодидом тетраэтиламмонии , TEAC был использован в качестве источника ионов тетраэтиламмонии для многочисленных клинических и фармакологических исследований, которые покрыты более подробно в записи для тетраэтиламмония . Вкратце, TEAC был исследован клинически на предмет его блокирующих ганглиозных свойств [10], хотя в настоящее время он практически устарел как лекарство и все еще используется в физиологических исследованиях из-за его способности блокировать K + каналы в различных тканях. [11] [12]
Токсичность [ править ]
Токсичность TEAC в первую очередь связана с ионом тетраэтиламмония, который был тщательно изучен. Острая токсичность TEAC сопоставима с токсичностью тетраэтиламмония бромида и тетраэтиламмония йодида . Эти данные [13] предназначены для сравнения; дополнительные сведения можно найти в статье о тетраэтиламмонии .
LD 50 (диапазоны ошибок не показаны): Мышь: 65 мг / кг, внутрибрюшинно; 900 мг / кг, перорально
См. Также [ править ]
- Тетраэтиламмоний
- Бромид тетраэтиламмония
- Йодид тетраэтиламмония
- Тетраметиламмоний хлорид
Ссылки [ править ]
- ^ a b Индекс Merck , 10-е изд., стр. 1316, Rahway: Merck & Co.
- ^ Руз, Питер; Эллер, Карстен; Хенкес, Эрхард; Россбахер, Роланд; Хёке, Хартмут (2015). «Амины алифатические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a02_001.pub2 .
- ↑ KM Harmon, JM Gabriele и J. Harmon (1990). "Водородная связь Часть 30. Новые корреляции ИК-спектра и структуры для моногидратов тетраэтиламмония, тетраметиламмония и N, N-диметил-пирролидиния фторида, моногидрата хлорида тетраэтиламмония и дигидрата гидроксида тетраметиламмония; доказательства плоскогокластера(H 2 O.F - ) 2 " . J. Mol. Struct. 216 53-62.
- ^ JH Loehlin и А. Квик (1978). «Моногидрат хлорида тетраэтиламмония». Acta Crystallographica Section B 34 3488–3490.
- ^ Ю.-С. Лам и TCW Мак (1978). «Кристаллические данные для некоторых гидратов солей тетраэтиламмония». 11 193.
- ^ Хармон, Кеннет М .; Габриэле, Джули М. (1981). «Водородная связь. 11. Инфракрасное исследование водно-хлоридного ионного кластера в гидрате хлорида тетраэтиламмония». Неорганическая химия . 20 (11): 4013–4015. DOI : 10.1021 / ic50225a087 .
- ^ HA Dieck, RM Laine и RF Heck (1975). «Катализируемый палладием синтез N, N'-диарилмочевины низкого давления из нитросоединений, аминов и монооксида углерода». J. Org. Chem. 40 2819–2822.
- ^ T.Yoshino et al. (1977). «Синтетические исследования с карбонатами. Часть 6. Синтезы 2-гидроксиэтильных производных реакциями этиленкарбоната с карбоновыми кислотами или гетероциклами в присутствии галогенидов тетраэтиламмония или в автокаталитических условиях». J. Chem. Soc., Perkin 1, 1266–1272.
- ^ Г. Сайкия и П.К. Айер (2010). «Простое алкилирование CH в воде: создание бездефектных материалов для оптоэлектронных устройств». J. Org. Chem. 75 2714–2717.
- ^ GK Моу и WA Freyburger (1950). «Ганглиоблокирующие агенты». Pharmacol. Ред. 2 61–95.
- ^ Б. Хилле (1967). «Избирательное ингибирование задержанных калиевых токов в нерве ионами тетраэтиламмония». J. Gen. Physiol. 50 1287–1302.
- ^ CM Армстронг и Б. Хилле (1972). «Внутренний четвертичный аммониевый рецептор в калиевых каналах узла Ранвье». J. Gen. Physiol. 59 388–400.
- ^ ОМ Gruhzit, RA Fisken и BJ Купер (1948). «Тетраэтиламмоний хлорид [(C 2 H 5 ) 4 NCl]. Острая и хроническая токсичность у экспериментальных животных». J. Pharmacol. Exp. Ther. 92 103–107.