 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC N , N , N- йодид триэтилэтанаминия | |
| Другие названия Йодид тетамона; Тетрамон J; TEAI | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.000.615 |
PubChem CID | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| C 8 H 20 I N | |
| Молярная масса | 257,159 г · моль -1 |
| Появление | Бесцветное или желтоватое кристаллическое твердое вещество |
| Плотность | 1,566 г / см 3 [1] |
| Температура плавления | 280 ° С (536 ° F, 553 К) (разлагается) |
| растворимый | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
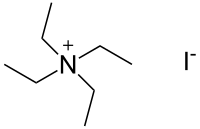
Йодид тетраэтиламмония представляет собой четвертичное аммониевое соединение с химической формулой C 8 H 20 N + I - . Он использовался в качестве источника ионов тетраэтиламмония в фармакологических и физиологических исследованиях, но также используется в органическом химическом синтезе.
Химия [ править ]
Подготовка [ править ]
Йодид тетраэтиламмония имеется в продаже, но его можно получить реакцией между триэтиламином и этилиодидом . [2]
Структура [ править ]
Определена кристаллическая структура иодида тетраэтиламмония. [3] Кристаллическая структура представляет собой искаженную решетку вюрцита . У атома азота координация представляет собой уплощенный тетраэдр. Угол N − C − C немного больше тетраэдрического угла.
Синтетические приложения [ править ]
Примеры включают:
- СТЕРЕОСЕЛЕКТИВНОЕ образование (Z) -diiodoalkenes обработки алкин с ICl в присутствии иодида тетраэтиламмонии. [4]
- 2-гидроксиэтилирования (присоединение -CH 2 -CH 2 -OH) с помощью карбоната этилена из карбоновых кислот и некоторых гетероциклов , имеющих кислотную NH. Например, бензойная кислота превращается в сложный эфир, 2-гидроксиэтилбензоат, обработкой этиленкарбонатом в присутствии иодида тетраэтиламмония. [5]
- Катализатор фазового переноса в геминальным диалкилировании из флуореных , N, N-диалкилирования из анилина и N-алкилирования карбазола с использованием водного гидроксида натрия и алкилгалогенидов . [6]
Токсичность [ править ]
LD 50 : 35 мг / кг (мышь, внутрибрюшинно); 56 мг / кг (мышь, в / в) [ необходима ссылка ]
См. Также [ править ]
- Тетраэтиламмоний
- Бромид тетраэтиламмония
- Тетраэтиламмоний хлорид
Ссылки [ править ]
- ^ The Merck Index , 10 Ed, p.1316, Rahway:. Merck & Co.
- ↑ AA Vernon и JL Sheard (1948). «Растворимость иодида тетраэтиламмония в смесях бензол-этилендихлорид». Варенье. Chem. Soc. 70 2035-2036.
- ^ Э. Уэйт и HM Пауэлл (1958). «Кристаллическая и молекулярная структура иодида тетраэтиламмония». J. Chem. Soc. 1872-1875 гг.
- ^ Н. Hénaff и А. Уайтинг (2000). «Стереоселективное образование 1,2-дииодалкенов и их применение в стереоселективном синтезе высокофункциональных алкенов посредством реакций сочетания Сузуки и Стилле». J. Chem. Soc., Perkin 1 395-400.
- ^ T.Yoshino et al. (1977). «Синтетические исследования с карбонатами. Часть 6. Синтезы 2-гидроксиэтильных производных реакциями этиленкарбоната с карбоновыми кислотами или гетероциклами в присутствии галогенидов тетраэтиламмония или в автокаталитических условиях». J. Chem. Soc., Perkin 1, 1266–1272.
- ^ G. Saikia и PK Iyer (2010). «Простое алкилирование CH в воде: создание бездефектных материалов для оптоэлектронных устройств». J. Org. Chem. 75 2714-2717.