 | |
| Имена | |
|---|---|
| Другие названия Монойодид таллия Йодид таллия | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.029.272 |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| TlI | |
| Молярная масса | 331,287 г / моль [1] |
| Появление | желтые кристаллы [1] |
| Плотность | 7,1 г / см 3 [1] |
| Температура плавления | 441,7 ° С (827,1 ° F, 714,8 К) [1] |
| Точка кипения | 824 ° C (1515 ° F, 1097 К) [1] |
| 0,085 г / л (25 ° C) [1] | |
| Растворимость | не растворим в спирте [1] |
| -82,2 · 10 -6 см 3 / моль [2] | |
| Опасности | |
Классификация ЕС (DSD) (устарела) | Очень токсично ( T + ) Опасно для окружающей среды ( N ) |
| R-фразы (устаревшие) | R26 / 28 , R33 , R51 / 53 |
| S-фразы (устаревшие) | (S1 / 2) , S13 , S28 , S45 , S61 |
| точка возгорания | Не воспламеняется |
| Родственные соединения | |
Другие анионы | Фторид таллия (I) Хлорид таллия (I) Бромид таллия (I) |
Другие катионы | Иодид галлия (I) Иодид индия (I) |
Родственные соединения | Йодид ртути (II) Иодид свинца (II) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Иодид таллия (I) представляет собой химическое соединение с формулой TlI . Он необычен тем, что является одним из немногих нерастворимых в воде иодидов металлов , наряду с AgI , CuI , SnI 2 , SnI 4 , PbI 2 и HgI 2 .
Химия [ править ]
TlI может быть образован в водном растворе путем метатезиса любой растворимой соли таллия с иодид-ионом. Он также образуется как побочный продукт при йодировании фенолов с помощью таллия (I) ацетатом таллия.
Попытки окислить TlI до иодида таллия (III) терпят неудачу, поскольку в результате окисления образуется трииодид таллия (I) , Tl + I 3 - .
Физические свойства [ править ]
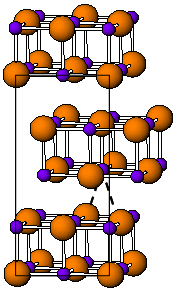
Форма TlI при комнатной температуре имеет желтый цвет и имеет ромбическую структуру [3], которую можно рассматривать как искаженную структуру NaCl. Считается, что искаженная структура вызвана благоприятными взаимодействиями таллий-таллий, ближайшее расстояние Tl-Tl составляет 383 пм. [4] При 175 ° C желтая форма превращается в красную форму CsCl . Этот фазовый переход сопровождается скачком электропроводности примерно на два порядка. Структуру CsI можно стабилизировать до комнатной температуры путем легирования TlI другими галогенидами, такими как RbI, CsI, KI, AgI, TlBr и TlCl. [5] Таким образом, присутствие примесей может быть причиной сосуществования кубического и орторомбического TlI.фазы при окружающих условиях. [3] Под высоким давлением 160 кбар TlI становится металлическим проводником. Нанометровый тонкий ИТ пленка , выращенная на LiF, NaCl или KBr подложках обладает кубической каменной солью структуры. [6]
Приложения [ править ]
Иодид таллия (I) добавляют в ртутные дуговые лампы для улучшения их характеристик [7]. Излучаемый свет находится в основном в сине-зеленой части видимого спектра света, наименее поглощаемой водой, поэтому они использовались для подводного освещения. [8] Йодид таллия (I) также используется в следовых количествах с NaI или CsI для производства сцинтилляторов, используемых в детекторах излучения.
Естественное явление [ править ]
Природный йодид таллия (I) был обнаружен только недавно в виде ромбического полиморфа, называемого наталиямаликитом. Имеет фумарольное происхождение. [9]
Безопасность [ править ]
Как и все соединения таллия, иодид таллия (I) очень токсичен.
Ссылки [ править ]
- ^ Б с д е е ж Хейнс, стр. 4,94
- ^ Хейнс, стр. 4,136
- ^ а б Лаундес, РП; Перри, CH (1973). «Молекулярная структура и ангармонизм в иодиде таллия». Журнал химической физики . 58 (1): 271–278. Bibcode : 1973JChPh..58..271L . DOI : 10.1063 / 1.1678917 .
- ^ Mudring, Anja-Верена (2007). «Галогениды таллия - новые аспекты стереохимической активности одиночных электронных пар тяжелых элементов основной группы». Европейский журнал неорганической химии . 2007 (6): 882–890. DOI : 10.1002 / ejic.200600975 .
- ^ Султана, Сайма; Рафиуддин (2009). «Электропроводность в композитном твердом электролите TlI – TiO2». Physica B: конденсированное вещество . 404 (1): 36–40. Bibcode : 2009PhyB..404 ... 36S . DOI : 10.1016 / j.physb.2008.10.002 .
- ^ Шульц, LG (1951). «Полиморфизм галогенидов цезия и таллия». Acta Crystallographica . 4 (6): 487–489. DOI : 10.1107 / S0365110X51001641 .
- ^ Рейлинг, Гилберт Х. (1964). «Характеристики ртутных пара-металлических иодидных дуговых ламп». Журнал Оптического общества Америки . 54 (4): 532. Полномочный код : 1964JOSA ... 54..532R . DOI : 10.1364 / JOSA.54.000532 .
- ^ Подводный журнал и информационный бюллетень, IPC Science and Technology Press, (1973), стр. 245
- ^ «Наталиямаликит: информация о минералах, данные и местонахождение» . www.mindat.org .
Цитированные источники [ править ]
- Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press . ISBN 1439855110.