 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Бромид титана (IV) | |
| Другие имена Тетрабромид титана | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ECHA InfoCard | 100.029.259 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| TiBr 4 | |
| Молярная масса | 367,483 г / моль |
| Внешность | коричневые кристаллы гигроскопичны |
| Плотность | 3,25 г / см 3 |
| Температура плавления | 39 ° С (102 ° F, 312 К) |
| Точка кипения | 230 ° С (446 ° F, 503 К) |
| гидролизует | |
| Растворимость в других растворителях | хлороуглероды, бензол |
| Структура | |
| кубическая, Па 3 , Z = 8 | |
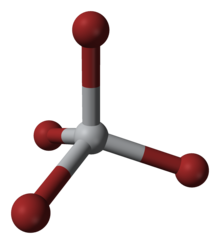
| Тетраэдр | |
| 0 Д | |
| Опасности | |
| Основные опасности | разъедающий |
| R-фразы (устаревшие) | 14-34 |
| S-фразы (устарели) | 26-36 / 37 / 39-45 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Негорючий |
| Родственные соединения | |
Другие анионы | Хлорид титана (IV) Фторид титана (IV) Иодид титана (IV) |
Родственные соединения | Бромид титана (III) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Тетрабромид титана представляет собой химическое соединение с формулой TiBr 4 . Это наиболее летучий бромид переходного металла. Свойства TiBr 4 являются средними для TiCl 4 и TiI 4 . Некоторыми ключевыми свойствами этих четырехкоординированных разновидностей Ti (IV) являются их высокая кислотность по Льюису и их высокая растворимость в неполярных органических растворителях. TiBr 4 является диамагнитным, что отражает конфигурацию металлического центра d 0 . [1]
Подготовка и структура [ править ]
Этот четырехкоординированный комплекс имеет тетраэдрическую геометрию. Его можно получить несколькими способами: (i) из элементов, (ii) посредством реакции TiO 2 с углеродом и бромом (см. Процесс Кролла ) и (iii) путем обработки TiCl 4 с помощью HBr .
Реакции [ править ]
Тетрабромид титана образует такие аддукты, как TiBr 4 ( THF ) 2 и [TiBr 5 ] - . [2] С объемными донорными лигандами, такими как 2-метилпиридин (2-Mepy), образуются пятикоординированные аддукты. TiBr 4 (2-MePy) является тригонально-бипирамидальным с пиридином в экваториальной плоскости. [3]
TiBr 4 использовался в качестве катализатора кислоты Льюиса в органическом синтезе . [4]
Тетрабромид и тетрахлориды титана реагируют с образованием статистической смеси смешанных тетрагалогенидов TiBr 4-x Cl x (x = 0-4). Механизм этой реакции перераспределения неясен. Один из предложенных путей задействует промежуточность димеров . [5]
Безопасность [ править ]
TiBr 4 быстро и потенциально опасно гидролизуется с выделением бромистого водорода , также известного как бромистоводородная кислота.
Ссылки [ править ]
- ^ Holleman, AF; Виберг, Э. "Неорганическая химия" Academic Press: Сан-Диего, 2001. ISBN 0-12-352651-5 .
- ^ Колин С. Кризер и Дж. Алан Крейтон (1975). «Пентахлор- и пентабром-титанат (IV) ионы». J. Chem. Soc., Dalton Trans. (14): 1402–1405. DOI : 10.1039 / DT9750001402 .
- ^ Hensen, K .; Lemke, A .; Болте, М. (2000). «Тетрабром (2-метилпиридин-N) -титанат (IV)». Acta Crystallographica . C56 (12): e565 – e566. DOI : 10.1107 / S0108270100015407 .
- ^ Б. Паттерсона, S. Marumoto & SD Rychnovsky (2003). "Циклизация альдол-принса Мукаяма, стимулированная титаном (IV)". Орг. Lett. 5 (17): 3163–3166. DOI : 10.1021 / ol035303n . PMID 12917007 .
- ^ SP Webb & MS Gordon (1999). «Межмолекулярные самовзаимодействия тетрагалогенидов титана TiX4 (X = F, Cl, Br)» . Варенье. Chem. Soc. 121 (11): 2552–2560. DOI : 10.1021 / ja983339i .
