| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Триметиларсан | |||
Другие названия
| |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 1730780 | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.008.925 | ||
| Номер ЕС |
| ||
| 141657 | |||
| MeSH | Триметиларсин | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 3 H 9 As | |||
| Молярная масса | 120,027 г · моль -1 | ||
| Появление | Бесцветная жидкость | ||
| Плотность | 1,124 г см −3 | ||
| Температура плавления | -87,3 ° С (-125,1 ° F, 185,8 К) | ||
| Точка кипения | 56 ° С (133 ° F, 329 К) | ||
| Слабо растворим | |||
| Растворимость в других растворителях | органические растворители | ||
| Состав | |||
| Тригонально-пирамидальный | |||
| 0,86 D | |||
| Опасности | |||
| Основные опасности | Легковоспламеняющийся | ||
| Паспорт безопасности | См .: страницу данных Внешний паспорт безопасности материала | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H331 , H301 , H410 | ||
| точка возгорания | -25 ° С (-13 ° F, 248 К) | ||
| Родственные соединения | |||
Родственные соединения | Какодиловая кислота Трифениларсин Пентаметиларшьяк Триметилфосфин Триметиламин | ||
| Страница дополнительных данных | |||
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. | ||
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ | ||
Спектральные данные | УФ , ИК , ЯМР , МС | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
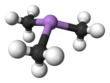
Триметиларсин (сокращенно ТМА или ТМА) представляет собой химическое соединение с формулой (СН 3 ) 3 Ас, обычно сокращенно Ме 3 или ТМА. Это органическое производное арсина использовалось в качестве источника мышьяка в промышленности микроэлектроники [1], как строительный блок для других органических соединений мышьяка , а также в качестве лиганда в координационной химии . Имеет отчетливый « чесночный » запах. Триметиларсин был открыт еще в 1854 году.
Структура и подготовка [ править ]
AsMe 3 представляет собой пирамидальную молекулу. Расстояние As-C составляет в среднем 1,519 Å, а углы C-As-C составляют 91,83 ° [2].
Trimethylarsine может быть получен путем обработкой оксида мышьяка с триметилалюминием : [3]
- As 2 O 3 + 1,5 [AlMe 3 ] 2 → 2 AsMe 3 + 3 / n (MeAl-O) n
Возникновение и реакции [ править ]
Триметиларсин является летучим побочным продуктом микробного воздействия на неорганические формы мышьяка, которые естественным образом встречаются в горных породах и почвах на уровне миллионных долей. [4] Триметиларсин зарегистрирован только в следовых количествах (частей на миллиард) в свалочном газе из Германии, Канады и США, и он является основным содержащим мышьяк соединением в газе. [5] [6] [7]
Триметиларсин пирофорен из-за экзотермической природы следующей реакции, которая инициирует горение:
- AsMe 3 + 1/2 O 2 → OAsMe 3 (TMAO)
История [ править ]
Предполагалось, что случаи отравления газом, выделяемым определенными микробами, связаны с содержанием мышьяка в краске. В 1893 году итальянский врач Бартоломео Гозио опубликовал свои результаты по «газу Гозио», который, как впоследствии было показано, содержит триметиларсин. [8] Во влажных условиях плесень Scopulariopsis brevicaulis продуцирует значительное количество метиларсинов за счет метилирования [9] неорганических пигментов , содержащих мышьяк , особенно Paris Green и Scheele's Green., которые когда-то использовались в обоях для дома. Более новые исследования показывают, что триметиларсин имеет низкую токсичность и поэтому не может служить причиной смерти и серьезных проблем со здоровьем, наблюдавшихся в 19 веке. [10] [11]
Безопасность [ править ]
Триметиларсин потенциально опасен [12] [13] [14], хотя его токсичность часто преувеличивается. [10]
Ссылки [ править ]
- ↑ Хосино, Масатака (1991). «Масс-спектрометрическое исследование разложения триметиларсина (ТМА) с триэтилгаллием (ТЭГа)». Журнал роста кристаллов . 110 (4): 704–712. DOI : 10.1016 / 0022-0248 (91) 90627-H .
- ^ Уэллс, AF (1984). Структурная неорганическая химия, пятое издание . Издательство Оксфордского университета. ISBN 978-0-19-855370-0.
- ↑ Гавриленко В.В., Чекулаева Л.А., Писарева И.В. «Высокоэффективный синтез триметиларсина» Известия Академии Наук. Серия химическая, 1996, № 8, с. 2122–2123.
- Перейти ↑ Cullen, WR, Reimer, KJ (1989). «Видообразование мышьяка в окружающей среде». Chem. Ред . 89 (4): 713–764. DOI : 10.1021 / cr00094a002 . ЛВП : 10214/2162 .CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Фельдман, J., Каллен, WR (1997). "Появление летучих соединений переходных металлов в свалочном газе: синтез карбонилов молибдена и вольфрама в". Environ. Sci. Technol . 31 (7): 2125–2129. DOI : 10.1021 / es960952y .CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Пинель-Raffaitin П., LeHecho И., Амуру Д., Потин-Готье, М. (2007). «Распространение и судьба неорганических и органических видов мышьяка в фильтрах свалок и биогазах». Environ. Sci. Technol . 41 (13): 4536–4541. DOI : 10.1021 / es0628506 . PMID 17695893 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Хури, JT; и другие. (7 апреля 2008 г.). «Анализ летучих соединений мышьяка в свалочном газе». Запахи и выбросы в атмосферу 2008 . Феникс, Аризона: Федерация водной среды.
- ^ Фредерик Челленджер (1955). «Биологическое метилирование». Q. Rev. Chem. Soc . 9 (3): 255–286. DOI : 10.1039 / QR9550900255 .
- ^ Ronald Bentley & Thomas G. Chasteen (2002). «Микробное метилирование металлоидов: мышьяка, сурьмы и висмута» . Обзоры микробиологии и молекулярной биологии . 66 (2): 250–271. DOI : 10.1128 / MMBR.66.2.250-271.2002 . PMC 120786 . PMID 12040126 .
- ^ а б Уильям Р. Каллен; Рональд Бентли (2005). «Токсичность триметиларсина: городской миф». J. Environ. Монит . 7 (1): 11–15. DOI : 10.1039 / b413752n . PMID 15693178 .
- ^ Фредерик Челленджер; Констанс Хиггинботтом; Луи Эллис (1933). «Образование металлоорганических соединений микроорганизмами. Часть I. Триметиларсин и диметилэтиларсин». J. Chem. Soc. : 95–101. DOI : 10.1039 / JR9330000095 .
- ^ Эндрюс, Пол; и другие. (2003). «Диметиларсин и триметиларсин - сильнодействующие генотоксины in vitro». Chem. Res. Toxicol . 16 (8): 994–1003. DOI : 10.1021 / tx034063h . PMID 12924927 .
- ^ Ирвин, Т. Рик; и другие. (1995). «Пренатальная токсичность in vitro триметиларсина, оксида триметиларсина и сульфида триметиларсина». Прикладная металлоорганическая химия . 9 (4): 315–321. DOI : 10.1002 / aoc.590090404 .
- ^ Хироши Ямаути; Тошиказу Кайсе; Кейко Такахаши; Юкио Ямамура (1990). «Токсичность и метаболизм триметиларсина у мышей и хомяков». Фундаментальная и прикладная токсикология . 14 (2): 399–407. DOI : 10.1016 / 0272-0590 (90) 90219-A . PMID 2318361 .
Внешние ссылки [ править ]
- Индекс по молекулярной формуле
- Информация об опасных химических веществах по классам
- Микробное метилирование металлоидов: мышьяка, сурьмы и висмута
- Мышьяк Curiosa и человечество