| Имена | |||
|---|---|---|---|
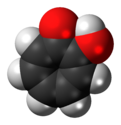
| Название ИЮПАК 2-гидрокси-2,4,6-циклогептатриен-1-он | |||
| Другие имена 2-гидрокситропон; Пурпурокатехол | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.007.799 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
| MeSH | D014334 | ||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 7 Н 6 О 2 | |||
| Молярная масса | 122,12 г / моль | ||
| Температура плавления | От 50 до 52 ° C (от 122 до 126 ° F, от 323 до 325 K) | ||
| Точка кипения | От 80 до 84 ° C (от 176 до 183 ° F, от 353 до 357 K) (0,1 мм рт. Ст.) | ||
| Кислотность (p K a ) | 6,89 (и -0,5 для конъюгированной кислоты) | ||
| -61 · 10 −6 см 3 / моль | |||
| Опасности | |||
| S-фразы (устаревшие) | S22 S24 / 25 | ||
| точка возгорания | 112 ° С (234 ° F, 385 К) | ||
| Родственные соединения | |||
Родственные соединения | Хинокитиол (4-изопропил-трополон) | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Трополон - это органическое соединение с формулой C 7 H 5 (OH) O. Это бледно-желтое твердое вещество, растворимое в органических растворителях. Соединение представляет интерес для химиков-исследователей из-за его необычной электронной структуры и его роли в качестве предшественника лиганда. Хотя его обычно не получают из тропона , его можно рассматривать как его производное с гидроксильной группой во 2-положении.
Синтез и реакции [ править ]
Описано множество методов синтеза трополона. [2] Один из них связанно бромирования 1,2-cycloheptanedione с N - бромсукцинимид с последующим дегидрогалогенированием при повышенных температурах, в то время как другое использование ацилоины конденсации этилового эфира из пимелиновой кислоты ацилоины снова с последующим окислением с помощью брома . [3]
Соединение легко подвергается O-алкилированию с образованием производных циклогептатриенила, которые, в свою очередь, являются универсальными синтетическими промежуточными продуктами. [4] С катионами металлов он подвергается депротонированию с образованием хелатных комплексов, например Cu (O 2 C 7 H 5 ) 2 . [3]
Естественное явление [ править ]
Было выделено около 200 природных производных трополона, в основном из растений и грибов . [5] трополона соединения и их производные включают dolabrins, dolabrinols, thujaplicins , thujaplicinols, stipitatic кислоту , stipitatonic кислоту, nootkatin, nootkatinol, puberulic кислоту, puberulonic кислоту, sepedonin, 4-acetyltropolone, pygmaein, isopygmaein, procein, chanootin, benzotropolones (такие а purpurogallin , crocipodin, goupiolone а и в), теафлавин и его производные, bromotropolones, tropoisoquinolines и tropoloisoquinolines (таких как grandirubrine, imerubrine, isoimerubrine, pareitropone, pareirubrine а и в), колхицин, колхикон и другие. [6] Трополон возникает через поликетидный путь, который дает фенольный промежуточный продукт, который подвергается расширению кольца. [4]
Они особенно встречаются у определенных видов растений, таких как семейства Cupressaceae и Liliaceae . [5] Трополоны в основном содержатся в сердцевине, листьях и коре растений, поэтому эфирные масла богаты различными типами трополонов. Первые природные производные трополона были изучены и очищены в середине 1930-х - начале 1940-х годов. [7] Thuja plicata , Thujopsis dolabrata , Chamaecyparis obtusa , Chamaecyparis taiwanensis и Juniperus thurifera были в списке деревьев, по которым были идентифицированы первые трополоны. Первыми синтетическими трополонами были туяплицины, полученные отРальф Рафаэль . [8]
Биологические эффекты [ править ]
Это ингибитор полифенолоксидазы винограда [9] [10] и тирозиназы грибов . [11]
Производные трополона [ править ]
| Учебный класс | Примеры | Основные природные источники [6] [5] [12] [13] | Направления исследований [5] [14] [6] [15] [16] | Запатентовано в продуктах [5] [17] |
|---|---|---|---|---|
| Простые трополоны | Трополоне | Pseudomonas lindbergii , Pseudomonas plantarii. | Антибактериальные, противогрибковые, инсектицидные, пестицидные, ингибиторы роста растений, противовоспалительные, антиоксидантные, нейрозащитные, антипротеазные, против потемнения (антитирозиназы и полифенолоксидазы), противоопухолевые, хелатирующие | - |
| Долабринс | β-долабрин, α-долабринол | Caragana pygmaea , Cupressus goveniana , Cupressus abramsiana , Thujopsis dolabrata. | Антибактериальные, противогрибковые, инсектицидные, пестицидные, ингибирование роста растений, ингибирование протеаз | Средство от насекомых, дезодорант |
| Туяплицины | α-туяплицин, β-туяплицин ( хинокитиол ), γ-туяплицин, туяплицинол | Кипарисовик туполистный , туя складчатая , туевик dolabrata , можжевельник древесный , Кедр Атласский , кипарис мексиканский , кипарисовик лавсона , Chamaecyparis taiwanensis , Chamaecyparis thyoides , кипарис аризонский , Кипарис macnabiana , кипарис крупноплодный , Кипарис guadalupensis , можжевельник китайский , Можжевельник , Juniperus саЩогтса , можжевельник западный , Можжевельник oxycedrus ,Можжевельник сабина , Calocedrus decurrens , Calocedrus formosana , Platycladus orientalis , Thuja occidentalis , Thuja standishii , Tetraclinis articulata , Cattleya forbesii , Carya glabra | Противогрибковые, антибактериальные, антибактериальные (антитирозиназные), хелатирующие, инсектицидные, пестицидные, противомалярийные, противовирусные, противовоспалительные, ингибиторы роста растений, антипротеазные, противодиабетические, противоопухолевые, химиосенсибилизирующие, антиоксидантные, нейропротекторные, ветеринарные препараты | Средство от насекомых, дезодорант, зубная паста, спрей для полости рта, уход за кожей и волосами, консервант для древесины, пищевая добавка, упаковка для пищевых продуктов |
| Сесквитерпеновые трополоны | Нооткатин, нооткатинол, нооткатол, нооткатен, нооткатон , валенсен-13-ол, нооткастатин | Chamaecyparis nootkatensis , Грейпфрут | Противогрибковое, против потемнения (антитирозиназа), инсектицидное, фунгицидное, противоопухолевое | Репелленты от насекомых, ароматизаторы, парфюмерия |
| Пигмеи | Пигмеин, Изопигмеин | Caragana pygmaea , Cupressus goveniana , Cupressus abramsiana. | - | - |
| Бензотрополоны | Пурпурогаллин , крокиподин , гупиолон А и В | Виды Quercus , Leccinum crocipodium , Goupia glabra | Антибактериальные, ингибирующие рост растений, ингибирование протеаз, противоопухолевые, противомалярийные, антиоксидантные, противовирусные | Пищевая добавка |
| Теафлавины | Теафлавин , теафлавовая кислота, теафлават А и В | Camellia sinensis ,виды Quercus | Антибактериальные, противовоспалительные, антиоксидантные, противовирусные, противодиабетические, хемосенсибилизирующие | - |
| Тропоизохинолины и трополоизохинолины | Грандирубрин, имерубрин, изоимерубрин, парейтропон, пареирубрин А и В | Циссампелос парейра , Abuta grandifolia | Антилейкемический | - |
| Алкалоиды тропона | Колхицин , демеколцин | Colchicum autumnale , Gloriosa superba | Антимитотические, противовоспалительные, антиподагрические, селекционные | Фармацевтический препарат |
Ссылки [ править ]
- ^ Трополона в Sigma-Aldrich
- ^ Миннс, Ричард А. (1977). «Трополоне». Орг. Synth. 57 : 117. DOI : 10,15227 / orgsyn.057.0117 .
- ^ a b Паусон, Питер Л. (1955). «Тропоны и трополоны». Chem. Ред. 55 (1): 9–136. DOI : 10.1021 / cr50001a002 .
- ^ а б Пьетра, Ф. (1973). «Семичленные сопряженные карбо- и гетероциклические соединения и их гомоконъюгированные аналоги и комплексы металлов. Синтез, биосинтез, структура и реакционная способность». Химические обзоры . 73 (4): 293–364. DOI : 10.1021 / cr60284a002 .
- ↑ a b c d e Чжао, Цзянь Чжао и Цзянь (30 сентября 2007 г.). «Тропоноиды растений: химия, биологическая активность и биосинтез». Современная лекарственная химия . DOI : 10.2174 / 092986707782023253 .
- ^ a b c Лю, На; Песня, Вангзе; Schienebeck, Casi M .; Чжан, Мин; Тан, Вэйпин (декабрь 2014 г.). «Синтез природных тропонов и трополонов» . Тетраэдр . 70 (49): 9281–9305. DOI : 10.1016 / j.tet.2014.07.065 . PMC 4228802 .
- ↑ Наканиши, Кодзи (июнь 2013 г.). "Автографы химиков 1953-1994 годов Тэцуо Нозоэ": эссе: "Автографы химиков 1953-1994 годов Тэцуо Нозоэ": эссе " . Химический отчет . 13 (3): 343–352. DOI : 10.1002 / tcr.201300007 .
- ^ Кук, JW; Рафаэль, РА; Скотт, AI (1951). «149. Трополоны. Часть II. Синтез α-, β- и γ-туяплицинов». J. Chem. Soc . 0 (0): 695–698. DOI : 10.1039 / JR9510000695 .
- ^ Зависящее от времени ингибирование полифенолоксидазы винограда трополоном. Эдельмира Валеро, Мануэла Гарсиа-Морено, Рамон Варон и Франсиско Гарсия-Кармона, J. Agric. Food Chem, 1991, том 39, стр 1043-1046,.. DOI : 10.1021 / jf00006a007
- ^ Чеджи, Рассел. Вторичные метаболиты западного красного кедра (Thuja plicata): их биотехнологическое применение и роль в придании естественной прочности . LAP Lambert Academic Publishing, 2010, ISBN 3-8383-4661-0 , ISBN 978-3-8383-4661-8
- ^ Ингибирование грибной тирозиназы трополоном. Varda Кан и Andrawis Andrawis, фитохимии, том 24, выпуск 5, 1985, страницы 905-908, DOI : 10.1016 / S0031-9422 (00) 83150-7
- ^ Karchesy, Джозеф Дж .; Келси, Рик Дж .; Гонсалес-Эрнандес, депутат (май 2018 г.). «Желтый кедр, Callitropsis (Chamaecyparis) nootkatensis, вторичные метаболиты, биологическая активность и химическая экология». Журнал химической экологии . 44 (5): 510–524. DOI : 10.1007 / s10886-018-0956-у .
- ^ Токсикологические чрезвычайные ситуации Goldfrank в . Нельсон, Льюис, 1963- (одиннадцатое изд.). Нью-Йорк. ISBN 978-1-259-85961-8. OCLC 1020416505 .CS1 maint: другие ( ссылка )
- ^ Карлссон, Бленда; Erdtman, H .; Франк, А .; Харви, МЫ; Остлинг, Свен (1952). "Химия природного отряда Cupressales. VIII. Составляющие сердцевины Chamaecyparis nootkatensis - карвакрол, нооткатин и хаминовая кислота" . Acta Chemica Scandinavica . 6 : 690–696. DOI : 10.3891 / acta.chem.scand.06-0690 .
- ^ Дальбет, Никола; Лаутерио, Томас Дж .; Вулф, Генри Р. (октябрь 2014 г.). «Механизм действия колхицина при лечении подагры» . Клиническая терапия . 36 (10): 1465–1479. DOI : 10.1016 / j.clinthera.2014.07.017 .
- ^ Гриффитс AJF, Gelbart WM, Miller JH (1999). Современный генетический анализ: изменение числа хромосом . WH Freeman, Нью-Йорк.CS1 maint: использует параметр авторов ( ссылка )
- ↑ Агентство по охране окружающей среды США, OCSPP (10 августа 2020 г.). «Нооткатон теперь зарегистрирован EPA» . Агентство по охране окружающей среды США .