 | |
 | |
| Имена | |
|---|---|
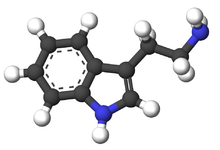
| Название ИЮПАК 2- (1 H- индол-3-ил) этанамин | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.000.464 |
PubChem CID | |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| C 10 H 12 N 2 | |
| Молярная масса | 160,220 г · моль -1 |
| Внешность | от белого до оранжевого кристаллического порошка [1] |
| Температура плавления | 113-116˚C [1] |
| Точка кипения | 137 ° C (279 ° F, 410 K) (0,15 мм рт. Ст.) [1] |
| незначительная растворимость в воде [1] | |
| Опасности | |
| точка возгорания | 185˚C [1] |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Триптамин является индоламиновым метаболитом незаменимой аминокислоты триптофана . [2] [3] Химическая структура определяется индолом ─ конденсированным бензольным и пиррольным кольцами и 2-аминоэтильной группой у третьего атома углерода. [2] Структура триптамина является общей чертой некоторых аминергических нейромодуляторов, включая мелатонин , серотонин , буфотенин и психоделические производные, такие как диметилтриптамин (DMT), псилоцибин , псилоцин и другие . [2][4] [5] [6] Было показано, что триптамин активирует следовые амино-ассоциированные рецепторы, экспрессируемые в головном мозге млекопитающих, и регулирует активность дофаминергической , серотонинергической и глутаматергической систем. [7] [8] В кишечнике человека симбиотические бактерии превращают пищевой триптофан в триптамин, который активируетрецепторы 5-HT 4 и регулирует перистальтику желудочно-кишечного тракта. [3] [9] [10] Для лечения мигрени были разработаны несколько препаратов на основе триптамина., в то время как рецепторы, связанные со следами аминов, исследуются как потенциальная мишень для лечения нервно-психических расстройств. [11] [12] [13]
Для получения списка производных триптамина см .: Список замещенных триптаминов .
Естественные явления [ править ]
Для получения списка растений, грибов и животных, содержащих триптамины, см. Список психоактивных растений и Список встречающихся в природе триптаминов .
Мозг млекопитающих [ править ]
Эндогенные уровни триптамина в головном мозге млекопитающих составляют менее 100 нг на грамм ткани. [14] [15] Однако повышенные уровни следов аминов наблюдались при нервно-психических расстройствах, таких как биполярная депрессия и шизофрения . [16]
Микробиом кишечника млекопитающих [ править ]
Триптамина относительно много в кишечнике и кале людей и грызунов. [17] [18] Комменсальные бактерии, в том числе Ruminococcus gnavus и Clostridium sporogenes в желудочно-кишечном тракте, обладают ферментом триптофан- декарбоксилазой , который способствует превращению пищевого триптофана в триптамин. [17] Триптамин является лигандом кишечных эпителиальных рецепторов серотонина типа 4 (5-HT 4 ) и регулирует баланс электролитов в желудочно-кишечном тракте через секрецию толстой кишки. [18]
Метаболизм триптамина [ править ]
Биосинтез [ править ]
Чтобы получить триптамин in vivo, триптофандекарбоксилаза удаляет группу карбоновой кислоты на α-углероде триптофана . [19] Синтетические модификации триптамина могут производить серотонин и мелатонин, однако это не основной путь синтеза эндогенных нейротрансмиттеров. [20]
Катаболизм [ править ]
Моноаминоксидазы A и B являются основными ферментами, участвующими в метаболизме триптамина с образованием индол-3-ацетальдегида , однако неясно, какая изоформа специфична для разложения триптамина. [21]
Механизмы действия и биологические эффекты [ править ]
Нейромодуляция [ править ]
Триптамин может слабо активировать рецептор, связанный со следами аминов, TAAR1 (hTAAR1 у человека). [22] [23] [24] В ограниченных исследованиях триптамин рассматривался как следовой нейромодулятор, способный регулировать активность ответов нейрональных клеток без связывания со связанными постсинаптическими рецепторами. [24] [25]
hTAAR1 [ править ]
hTAAR1 - это стимулирующий рецептор, связанный с G-белком (GPCR), который слабо экспрессируется во внутриклеточном компартменте как пре-, так и постсинаптических нейронов. [26] Триптамин и другие агонисты hTAAR1 может увеличить возбуждение нейронов путем ингибирования рециркуляции нейромедиаторов через цАМФ -зависимой фосфорилирования из обратного захвата моноаминов транспортера . [27] [25] Этот механизм увеличивает количество нейротрансмиттера в синаптической щели, что впоследствии увеличивает связывание постсинаптических рецепторов и активацию нейронов. [25] И наоборот, когда hTAAR1 совместно локализован с G-белком, внутренне выпрямляющие калиевые каналы(GIRKs), активация рецептора снижает нейрональную активность, облегчая гиперполяризацию мембраны за счет оттока ионов калия. [25] Баланс между ингибирующей и возбуждающей активностью активации hTAAR1 подчеркивает роль триптамина в регуляции нервной активности. [28]
Активация hTAAR1 изучается как новый метод лечения депрессии, зависимости и шизофрении. [29] hTAAR1 в первую очередь экспрессируется в структурах мозга, связанных с дофаминовыми системами, такими как вентральная тегментальная область (VTA) и серотониновые системы в ядрах дорсального шва (DRN). [29] Кроме того, ген hTAAR1 локализован в 6q23.2 хромосомы человека, который является локусом восприимчивости к расстройствам настроения и шизофрении. [30] Активация TAAR1 предполагает потенциальное новое лечение нервно-психических расстройств, поскольку агонисты TAAR1 обладают антидепрессивной активностью, повышением когнитивных функций , снижением стресса и эффектами против зависимости.[28] [30]
Желудочно-кишечная моторика [ править ]
Триптамин, продуцируемый мутуалистическими бактериями в кишечнике человека, активирует GPCR серотонина, повсеместно экспрессируемые вдоль эпителия толстой кишки. [31] При связывании триптамина активированный рецептор 5-HT 4 претерпевает конформационное изменение, которое позволяет его альфа-субъединице G s обменивать GDP на GTP и высвобождать его из рецептора 5-HT 4 и субъединицы βγ. [31] ГТФ-G связаны с активирует аденилатциклазу , которая катализирует превращение АТФ в циклического аденозинмонофосфата (цАМФ). [31]цАМФ открывает каналы для ионов хлора и калия, чтобы управлять секрецией электролитов в толстой кишке и способствовать перистальтике кишечника. [32] [33]
Фармакокинетика [ править ]
| Активация TAAR1 (EC 50 ) и сродство связывания (K i ) триптаминов [34] | ||||||
|---|---|---|---|---|---|---|
| Триптамин | Человеческий TAAR1 | Мышь TAAR1 | Крыса ТААР | |||
| 50 по К.Э. | K я | 50 по К.Э. | K я | 50 по К.Э. | K я | |
| Триптамин | 21 год | Нет данных | 2,7 | 1.4 | 0,41 | 0,13 |
| Серотонин | > 50 | Нет данных | > 50 | Нет данных | 5.2 | Нет данных |
| Псилоцин | > 30 | Нет данных | 2,7 | 17 | 0,92 | 1.4 |
| ДМТ | > 10 | Нет данных | 1.2 | 3.3 | 1.5 | 22 |
| Значения EC 50 и K i выражены в микромолях (мкМ). 50 EC отражает сумму триптамина, необходимого для вызова 50% максимального ответа TAAR1. Чем меньше значение K i , тем сильнее триптамин связывается с рецептором. | ||||||
Терапевтические препараты на основе триптамина [ править ]
| Препарат, средство, медикамент | Механизм | Уход | Эффект | Структура |
|---|---|---|---|---|
| Суматриптан [35] | 5-HT 1B и 5-HT 1D агонист | Мигрени | Вазоконстрикция кровеносных сосудов головного мозга | Суматриптан |
| Ризатриптан [35] | 5-HT 1B и 5-HT 1D агонист | Мигрени | Вазоконстрикция кровеносных сосудов головного мозга | Ризатриптан |
| Золмитриптан [35] | 5-HT 1B и 5-HT 1D агонист | Мигрени | Вазоконстрикция кровеносных сосудов головного мозга | Золмитриптан |
| Алмотриптан [35] | 5-HT 1B и 5-HT 1D агонист | Мигрени | Вазоконстрикция кровеносных сосудов головного мозга | Алмотриптан |
| Элетриптан [35] | 5-HT 1B и 5-HT 1D агонист | Мигрени | Вазоконстрикция кровеносных сосудов головного мозга | Элетриптан |
| Фроватриптан [35] | 5-HT 1B и 5-HT 1D агонист | Мигрени | Вазоконстрикция кровеносных сосудов головного мозга | Фроватриптан |
| Наратриптан [35] | 5-HT 1B и 5-HT 1D агонист | Мигрени | Вазоконстрикция кровеносных сосудов головного мозга | Наратриптан |
См. Также [ править ]
- Триптофан
- Замещенные триптамины
- Следы аминов
- Агонист рецепторов серотонина
- Человеческий следовой аминосвязанный рецептор 1
- Нейромодуляция
Ссылки [ править ]
- ^ a b c d e http://www.chemicalbook.com/ProductChemicalPropertiesCB8192006_EN.htm [ требуется полная ссылка ]
- ^ а б в PubChem. «Триптамин» . pubchem.ncbi.nlm.nih.gov . Проверено 1 декабря 2020 .
- ^ a b Дженкинс, Триша А .; Нгуен, Джейсон CD; Polglaze, Kate E .; Бертран, Пол П. (2016-01-20). «Влияние триптофана и серотонина на настроение и познание с возможной ролью оси кишечник-мозг» . Питательные вещества . 8 (1): 56. DOI : 10,3390 / nu8010056 . ISSN 2072-6643 . PMC 4728667 . PMID 26805875 .
- ^ Тылш, Филип; Паленичек, Томаш; Горачек, Иржи (01.03.2014). «Псилоцибин - Обобщение знаний и новые перспективы» . Европейская нейропсихофармакология . 24 (3): 342–356. DOI : 10.1016 / j.euroneuro.2013.12.006 . ISSN 0924-977X . PMID 24444771 . S2CID 10758314 .
- ^ Титтарелли, Роберта; Маннокки, Джулио; Пантано, Фламиния; Ромоло, Франческо Саверио (2015). «Рекреационное использование, анализ и токсичность триптаминов» . Современная нейрофармакология . 13 (1): 26–46. DOI : 10.2174 / 1570159X13666141210222409 . ISSN 1570-159X . PMC 4462041 . PMID 26074742 .
- ^ "Феномен Аяуаски" . КАРТЫ . Проверено 3 октября 2020 .
- ^ Хан, Мухаммад Захид; Наваз, Вакас (01.10.2016). «Новые роли человеческих следовых аминов и человеческих следовых амино-ассоциированных рецепторов (hTAAR) в центральной нервной системе» . Биомедицина и фармакотерапия . 83 : 439–449. DOI : 10.1016 / j.biopha.2016.07.002 . ISSN 0753-3322 . PMID 27424325 .
- ^ Берри, Марк Д .; Гайнетдинов, Рауль Р .; Hoener, Marius C .; Шахид, Мохаммед (01.12.2017). «Фармакология человеческих следовых амино-ассоциированных рецепторов: терапевтические возможности и проблемы» . Фармакология и терапия . 180 : 161–180. DOI : 10.1016 / j.pharmthera.2017.07.002 . ISSN 0163-7258 . PMID 28723415 . S2CID 207366162 .
- ^ Бхаттарай, Йогеш; Уильямс, Брианна Б .; Battaglioli, Eric J .; Whitaker, Weston R .; Тилль, Лиза; Гровер, Мадхусудан; Linden, Дэвид Р .; Акиба, Ясутада; Кандималла, Каруня К .; Zachos, Nicholas C .; Кауниц, Джонатан Д. (13.06.2018). «Триптамин, продуцируемый кишечной микробиотой, активирует эпителиальный рецептор, связанный с G-белком, для увеличения секреции толстой кишки» . Клеточный хозяин и микроб . 23 (6): 775–785.e5. DOI : 10.1016 / j.chom.2018.05.004 . ISSN 1931-3128 . PMC 6055526 . PMID 29902441 .
- ^ Поле, Майкл (2003). «Кишечный ионный транспорт и патофизиология диареи» . Журнал клинических исследований . 111 (7): 931–943. DOI : 10.1172 / JCI200318326 . ISSN 0021-9738 . PMC 152597 . PMID 12671039 .
- ^ "Агонисты серотониновых рецепторов (триптаны)" , LiverTox: Клиническая и исследовательская информация о лекарственном поражении печени , Bethesda (MD): Национальный институт диабета, болезней пищеварения и почек, 2012, PMID 31644023 , получено 15 октября 2020 г.
- ^ «Новое соединение, связанное с психоделическим ибогаином, может лечить зависимость, депрессию» . Калифорнийский университет в Дэвисе . 2020-12-09 . Проверено 11 декабря 2020 .
- ^ ServiceDec. 9, Роберт Ф .; 2020; Ут, 11:45 (09.12.2020). «Химики модернизируют психоделик для лечения депрессии и зависимости у грызунов» . Наука | AAAS . Проверено 11 декабря 2020 .CS1 maint: числовые имена: список авторов ( ссылка )
- ^ Титтарелли, Роберта; Маннокки, Джулио; Пантано, Фламиния; Ромоло, Франческо Саверио (2015). «Рекреационное использование, анализ и токсичность триптаминов» . Современная нейрофармакология . 13 (1): 26–46. DOI : 10.2174 / 1570159X13666141210222409 . ISSN 1570-159X . PMC 4462041 . PMID 26074742 .
- ^ Берри, Марк Д .; Гайнетдинов, Рауль Р .; Hoener, Marius C .; Шахид, Мохаммед (01.12.2017). «Фармакология человеческих следовых амино-ассоциированных рецепторов: терапевтические возможности и проблемы» . Фармакология и терапия . 180 : 161–180. DOI : 10.1016 / j.pharmthera.2017.07.002 . ISSN 0163-7258 . PMID 28723415 . S2CID 207366162 .
- ^ Миллер, Грегори М. (2011). «Возникающая роль следовых аминов ассоциированного рецептора 1 в функциональной регуляции переносчиков моноаминов и дофаминергической активности» . Журнал нейрохимии . 116 (2): 164–176. DOI : 10.1111 / j.1471-4159.2010.07109.x . ISSN 0022-3042 . PMC 3005101 . PMID 21073468 .
- ^ a b Дженкинс, Триша А .; Нгуен, Джейсон CD; Polglaze, Kate E .; Бертран, Пол П. (2016-01-20). «Влияние триптофана и серотонина на настроение и познание с возможной ролью оси кишечник-мозг» . Питательные вещества . 8 (1): 56. DOI : 10,3390 / nu8010056 . ISSN 2072-6643 . PMC 4728667 . PMID 26805875 .
- ^ а б Бхаттарай, Йогеш; Уильямс, Брианна Б .; Battaglioli, Eric J .; Whitaker, Weston R .; Тилль, Лиза; Гровер, Мадхусудан; Linden, Дэвид Р .; Акиба, Ясутада; Кандималла, Каруня К .; Zachos, Nicholas C .; Кауниц, Джонатан Д. (13.06.2018). «Триптамин, продуцируемый кишечной микробиотой, активирует эпителиальный рецептор, связанный с G-белком, для увеличения секреции толстой кишки» . Клеточный хозяин и микроб . 23 (6): 775–785.e5. DOI : 10.1016 / j.chom.2018.05.004 . ISSN 1931-3128 . PMC 6055526 . PMID 29902441 .
- ^ Титтарелли, Роберта; Маннокки, Джулио; Пантано, Фламиния; Ромоло, Франческо Саверио (2015). «Рекреационное использование, анализ и токсичность триптаминов» . Современная нейрофармакология . 13 (1): 26–46. DOI : 10.2174 / 1570159X13666141210222409 . ISSN 1570-159X . PMC 4462041 . PMID 26074742 .
- ^ «Синтез и метаболизм серотонина» . Сигма Олдрич . 2020.
- ^ "MetaCyc L-триптофан деградации VI (через триптамин)" . biocyc.org . Проверено 11 декабря 2020 .
- ^ Ю, Ай-Мин; Granvil, Camille P .; Haining, Роберт Л .; Krausz, Kristopher W .; Корчеро, Хавьер; Кюпфер, Адриан; Idle, Джеффри Р .; Гонсалес, Фрэнк Дж. (01.02.2003). «Относительный вклад изоферментов моноаминоксидазы и цитохрома P450 в метаболическое дезаминирование следовых аминов триптамина» . Журнал фармакологии и экспериментальной терапии . 304 (2): 539–546. DOI : 10,1124 / jpet.102.043786 . ISSN 0022-3565 . PMID 12538805 . S2CID 18279145 .
- ^ Хан, Мухаммад Захид; Наваз, Вакас (01.10.2016). «Новые роли человеческих следовых аминов и человеческих следовых амино-ассоциированных рецепторов (hTAAR) в центральной нервной системе» . Биомедицина и фармакотерапия . 83 : 439–449. DOI : 10.1016 / j.biopha.2016.07.002 . ISSN 0753-3322 . PMID 27424325 .
- ^ a b Zucchi, R; Кьеллини, G; Сканлан, ТС; Гранди, ДК (2006). «Следы аминосвязанных рецепторов и их лигандов» . Британский журнал фармакологии . 149 (8): 967–978. DOI : 10.1038 / sj.bjp.0706948 . ISSN 0007-1188 . PMC 2014643 . PMID 17088868 .
- ^ a b c d Миллер, Грегори М. (2011). «Возникающая роль следовых аминов ассоциированного рецептора 1 в функциональной регуляции переносчиков моноаминов и дофаминергической активности» . Журнал нейрохимии . 116 (2): 164–176. DOI : 10.1111 / j.1471-4159.2010.07109.x . ISSN 0022-3042 . PMC 3005101 . PMID 21073468 .
- ^ Берри, Марк Д .; Гайнетдинов, Рауль Р .; Hoener, Marius C .; Шахид, Мохаммед (01.12.2017). «Фармакология человеческих следовых амино-ассоциированных рецепторов: терапевтические возможности и проблемы» . Фармакология и терапия . 180 : 161–180. DOI : 10.1016 / j.pharmthera.2017.07.002 . ISSN 0163-7258 . PMID 28723415 . S2CID 207366162 .
- ^ Цзин, Ли; Ли, Цзюнь-Сюй (2015-08-15). «Следы амино-ассоциированного рецептора 1: многообещающая мишень для лечения зависимости от психостимуляторов» . Европейский журнал фармакологии . 761 : 345–352. DOI : 10.1016 / j.ejphar.2015.06.019 . ISSN 0014-2999 . PMC 4532615 . PMID 26092759 .
- ^ a b Гранди, Дэвид К .; Миллер, Грегори М .; Ли, Цзюнь-Сюй (01.02.2016). « » TAARgeting Addiction «Аламо Медведи Свидетель на другой революции» . Наркотическая и алкогольная зависимость . 159 : 9–16. DOI : 10.1016 / j.drugalcdep.2015.11.014 . ISSN 0376-8716 . PMC 4724540 . PMID 26644139 .
- ^ а б Берри, Марк Д .; Гайнетдинов, Рауль Р .; Hoener, Marius C .; Шахид, Мохаммед (01.12.2017). «Фармакология человеческих следовых амино-ассоциированных рецепторов: терапевтические возможности и проблемы» . Фармакология и терапия . 180 : 161–180. DOI : 10.1016 / j.pharmthera.2017.07.002 . ISSN 0163-7258 . PMID 28723415 . S2CID 207366162 .
- ^ a b Гайнетдинов, Рауль Р .; Hoener, Marius C .; Берри, Марк Д. (2018-07-01). «Следовые амины и их рецепторы» . Фармакологические обзоры . 70 (3): 549–620. DOI : 10,1124 / pr.117.015305 . ISSN 0031-6997 . PMID 29941461 . S2CID 49411553 .
- ^ a b c Бхаттарай, Йогеш; Уильямс, Брианна Б .; Battaglioli, Eric J .; Whitaker, Weston R .; Тилль, Лиза; Гровер, Мадхусудан; Linden, Дэвид Р .; Акиба, Ясутада; Кандималла, Каруня К .; Zachos, Nicholas C .; Кауниц, Джонатан Д. (13.06.2018). «Триптамин, продуцируемый кишечной микробиотой, активирует эпителиальный рецептор, связанный с G-белком, для увеличения секреции толстой кишки» . Клеточный хозяин и микроб . 23 (6): 775–785.e5. DOI : 10.1016 / j.chom.2018.05.004 . ISSN 1931-3128 . PMC 6055526 . PMID 29902441 .
- ^ Поле, Майкл (2003). «Кишечный ионный транспорт и патофизиология диареи» . Журнал клинических исследований . 111 (7): 931–943. DOI : 10.1172 / JCI200318326 . ISSN 0021-9738 . PMC 152597 . PMID 12671039 .
- ^ "Microbiome-Lax может облегчить запор" . GEN - Новости генной инженерии и биотехнологии . 2018-06-15 . Проверено 11 декабря 2020 .
- ^ Гайнетдинов, Рауль Р .; Hoener, Marius C .; Берри, Марк Д. (2018-07-01). «Следовые амины и их рецепторы» . Фармакологические обзоры . 70 (3): 549–620. DOI : 10,1124 / pr.117.015305 . ISSN 0031-6997 . PMID 29941461 . S2CID 49411553 .
- ^ a b c d e f g «Агонисты серотониновых рецепторов (триптаны)» , LiverTox: Клиническая и исследовательская информация о лекарственном поражении печени , Bethesda (MD): Национальный институт диабета, болезней органов пищеварения и почек, 2012, PMID 31644023 , получено 2020-10-15
Внешние ссылки [ править ]
- Часто задаваемые вопросы о триптамине
- Триптаминовые галлюциногены и сознание
- Триптаминд Психоактивные вещества , справочный сайт о триптамине и других психоактивных веществах.
- Вход триптамина (Т) в TiHKAL • информация