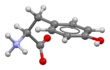
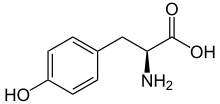
 Скелетная формула из L -тирозина | |||
 L- тирозин при физиологическом pH | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК ( S ) -Тирозин | |||
| Другие имена L -2-амино-3- (4-гидроксифенил) пропановая кислота | |||
| Идентификаторы | |||
| |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.419 | ||
PubChem CID | |||
| UNII | |||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 9 H 11 N O 3 | |||
| Молярная масса | 181,191 г · моль -1 | ||
| 0,0453 г / 100 мл | |||
| -105,3 · 10 −6 см 3 / моль | |||
| Опасности | |||
| Паспорт безопасности | См .: страницу данных | ||
| NFPA 704 (огненный алмаз) | |||
| Страница дополнительных данных | |||
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. | ||
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ | ||
Спектральные данные | УФ , ИК , ЯМР , МС | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
L- тирозин или тирозин (символ Tyr или Y ) [2] или 4-гидроксифенилаланин - одна из 20 стандартных аминокислот , которые используются клетками для синтеза белков . Это заменимая аминокислота с полярной боковой группой . Слово «тирозин» происходит от греческого tyrós , что означает сыр , поскольку он был впервые обнаружен в 1846 году немецким химиком Юстусом фон Либихом в белке казеина из сыра. [3] [4] Это называетсятирозил, если его называют функциональной группой или боковой цепью. Хотя тирозин обычно классифицируется как гидрофобная аминокислота, он более гидрофильный, чем фенилаланин . [5] Он кодируется с помощью кодонов UAC и СХУ в матричной РНК .
Функции [ править ]
Помимо того , что тирозин является протеиногенной аминокислотой , он играет особую роль благодаря фенольной функциональности. Он встречается в белках, которые являются частью процессов передачи сигнала, и функционирует как приемник фосфатных групп, которые передаются посредством протеинкиназ . Фосфорилирование гидроксильной группы может изменять активность целевого белка или может образовывать часть сигнального каскада через связывание с доменом SH2.
Остаток тирозина также играет важную роль в фотосинтезе . В хлоропластах ( фотосистема II ) он действует как донор электронов при восстановлении окисленного хлорофилла . В этом процессе он теряет атом водорода своей фенольной ОН-группы. Этот радикал впоследствии восстанавливается в фотосистеме II четырьмя остовными кластерами марганца.
Диетические требования и источники [ править ]
Диетический номер всасывание (рекомендуется диетическое пособие, RDA) для фенилаланина и тирозин составляет 42 мг на килограмм веса тела. [6] Для человека весом 70 кг это 2,31 г (фенилаланин + тирозин).
Тирозин, которые также могут быть синтезированы в организме из фенилаланина , содержатся во многих высоком белке пищевых продуктов , такие как курица , индейка , рыба , молоко , йогурт , творог , сыр , арахис , миндаль , семена тыквы , семена кунжута , сои продукты и фасоль лима , а также авокадо и бананы . [7] Например, яичный белок содержит около 250 мг на яйцо, [8]в то время как постная говядина / баранина / свинина / лосось / курица / индейка содержит около 1 г на порцию в 3 унции (85 г). [8]
Биосинтез [ править ]
У растений и большинства микроорганизмов tyr продуцируется через префенат , промежуточный продукт на пути шикимата . Префенат подвергается окислительному декарбоксилированию с сохранением гидроксильной группы с образованием п- гидроксифенилпирувата, который трансаминируется с использованием глутамата в качестве источника азота с образованием тирозина и α-кетоглутарата .
Млекопитающие синтезируют тирозин из незаменимой аминокислоты фенилаланина ( phe ), получаемой с пищей. Превращение phe в tyr катализируется ферментом фенилаланингидроксилазой , монооксигеназой. Этот фермент катализирует реакцию, вызывающую присоединение гидроксильной группы к концу 6-углеродного ароматического кольца фенилаланина , так что оно становится тирозином.
Метаболизм [ править ]
Фосфорилирование и сульфатирование [ править ]
Некоторые из остатков тирозина могут быть помечены (по гидроксильной группе) фосфатной группой ( фосфорилированы ) протеинкиназами . В своей фосфорилированной форме тирозин называется фосфотирозином . Фосфорилирование тирозина считается одним из ключевых шагов в передаче сигнала и регуляции ферментативной активности. Фосфотирозин можно обнаружить с помощью специфических антител . Остатки тирозина также можно модифицировать путем добавления сульфатной группы, процесс, известный как сульфатирование тирозина . [9] Сульфатирование тирозинакатализируется тирозилпротеинсульфотрансферазой (TPST). Подобно упомянутым выше антителам к фосфотирозину, недавно были описаны антитела, которые специфически обнаруживают сульфотирозин. [10]
Предшественник нейротрансмиттеров и гормонов [ править ]
В дофаминергических клетках головного мозга тирозин превращается в L-DOPA под действием фермента тирозингидроксилазы (TH). TH - это фермент, ограничивающий скорость, участвующий в синтезе нейромедиатора дофамина . Затем дофамин может быть преобразован в другие катехоламины , такие как норадреналин (норадреналин) и адреналин (адреналин).
В щитовидной железе гормоны трийодтиронин (Т 3 ) и тироксин (Т 4 ) в коллоиде в щитовидной железе , также вытекает из тирозина.
Биосинтетические пути катехоламинов и следовых аминов в мозге человека [11] [12] [13] |
Предшественник алкалоидов [ править ]
Латекс опийного мака Papaver somniferum , как было показано, превращает тирозин в алкалоид морфин, и был установлен биосинтетический путь от тирозина до морфина с использованием радиоактивно меченного углеродом тирозина для отслеживания пути синтеза in vivo. . [ необходима цитата ]
Предшественник природных фенолов [ править ]
Тирозинаммиаклиаза (TAL) - это фермент, участвующий в пути биосинтеза природных фенолов. Он превращает L-тирозин в п-кумаровую кислоту .
Предшественник пигментов [ править ]
Тирозин также является предшественником пигмента меланина .
Роль в синтезе коэнзима Q10 [ править ]
Тирозин (или его предшественник фенилаланин) необходим для синтеза бензохиноновой структуры, которая является частью кофермента Q10 .
Деградация [ править ]
Разложение L-тирозина (син. Пара- гидроксифенилаланин) начинается с α-кетоглутарат-зависимого трансаминирования через тирозинтрансаминазу до пара- гидроксифенилпирувата . Позиционное описание пара , сокращенно p , означает, что гидроксильная группа и боковая цепь фенильного кольца расположены напротив друг друга (см. Иллюстрацию ниже).
Следующая стадия окисления катализируется пара- гидроксифенилпируватдиоксигеназой и отщеплением гомогентизата CO 2 (2,5-дигидроксифенил-1-ацетат). [14] Чтобы разделить ароматическое кольцо гомогентизата, необходима дополнительная диоксигеназа, гомогентизат-1,2-диоксигеназа . Таким образом, за счет включения еще одной молекулы O 2 образуется малейлацетоацетат .
Fumarylacetoacetate создается maleylacetoacetate цис - транс - -isomerase через вращения карбоксильной группы , созданной из гидроксильной группы путем окисления. Эта цис-транс- изомераза содержит глутатион в качестве кофермента . Наконец, фумарилацетоацетат расщепляется ферментом фумарилацетоацетатгидролазой за счет добавления молекулы воды.
Таким образом высвобождаются фумарат (также метаболит цикла лимонной кислоты) и ацетоацетат (3-кетобутироат). Ацетоацетат представляет собой кетоновое тело , которое активируется сукцинил-КоА, после чего оно может быть преобразовано в ацетил-КоА , который, в свою очередь, может окисляться циклом лимонной кислоты или использоваться для синтеза жирных кислот .
Флоретиновая кислота также является метаболитом тирозина в моче крыс. [15]
Орто- и метатирозин [ править ]
Известны три структурных изомера L-тирозина. Помимо обычной аминокислоты L-тирозина, которая является пара-изомером ( пара- тир, п- тир или 4-гидроксифенилаланин), существуют два дополнительных региоизомера, а именно мета- тирозин (также известный как 3-гидроксифенилаланин , L- м- тирозин и м- тир) и орто- тирозин ( о- тир или 2-гидроксифенилаланин), встречающиеся в природе. М -Tyr и о -Tyr изомеры, которые являются редкими, возникает в результате неферментативных свободных радикаловгидроксилирование фенилаланина в условиях окислительного стресса . [16] [17]
м-тирозин и аналоги (редкие в природе , но доступных синтетический) показали применение в болезни Паркинсона , болезни Альцгеймера и артрите . [18]
Медицинское использование [ править ]
Тирозин является предшественником нейротрансмиттеров и увеличивает уровни нейромедиаторов в плазме (особенно дофамина и норэпинефрина) [19], но практически не влияет на настроение у нормальных людей. [20] [21] [22] Тем не менее, ряд исследований показал, что тирозин полезен в условиях стресса, холода, усталости (у мышей), [23] длительной работы и лишения сна, [24] [25] с снижение уровня гормона стресса [26] снижение вызванной стрессом потери веса, наблюдаемое в испытаниях на животных [23], а также улучшение когнитивных и физических показателей [21] [27] [28] видели в человеческих испытаниях.
Тирозин, по-видимому, не оказывает значительного влияния на когнитивные или физические способности в нормальных условиях [29] [30], но помогает лучше поддерживать рабочую память при многозадачности. [31]
Промышленный синтез [ править ]
L-тирозин и его производные ( L-DOPA , меланин , фенилпропаноиды и др.) Используются в фармацевтических препаратах , пищевых добавках и пищевых добавках . Ранее для производства L-тирозина использовались два метода. Первый включает извлечение нужной аминокислоты из гидролизатов белка с использованием химического подхода. Второй использует ферментативный синтез фенольных соединений, пирувата и аммиака за счет использования тирозинфеноллиазы . [32] Достижения в области генной инженерии и появление промышленной ферментациипереключили синтез L-тирозина на использование искусственно созданных штаммов E. coli . [33] [34]
См. Также [ править ]
- Альбинизм
- Алькаптонурия
- Беталаин
- Йодированные производные тирозина
- Поли реакция
- Тирамин
- Сульфатирование тирозина
- Тирозинемия
Ссылки [ править ]
- ^ a b Фрей MN, Koetzle TF, Lehmann MS, Hamilton WC (1973). «Прецизионное определение структуры белков и нуклеиновых кислот с помощью дифракции нейтронов. X. Сравнение кристаллической и молекулярной структур L-тирозина и L-тирозина гидрохлорида». J. Chem. Phys. 58 (6): 2547–2556. Bibcode : 1973JChPh..58.2547F . DOI : 10.1063 / 1.1679537 .
- ^ «Номенклатура и символика аминокислот и пептидов» . Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983. Архивировано 9 октября 2008 года . Проверено 5 марта 2018 .
- ^ «Тирозин» . Колумбийская электронная энциклопедия, 6-е изд . Infoplease.com - Издательство Колумбийского университета. 2007 . Проверено 20 апреля 2008 .
- Перейти ↑ Harper D (2001). «Тирозин» . Интернет-словарь этимологии . Проверено 20 апреля 2008 .
- ^ «Аминокислоты - Тирозин» . www.biology.arizona.edu . Проверено 31 января 2018 .
- ^ Pencharz PB, Hsu JW, Болл RO (июнь 2007). «Потребность в ароматических аминокислотах у здоровых людей» . Журнал питания . 137 (6 Дополнение 1): 1576S – 1578S, обсуждение 1597S-1598S. DOI : 10.1093 / JN / 137.6.1576S . PMID 17513429 .
- ^ «Тирозин» . Медицинский центр Университета Мэриленда . Проверено 17 марта 2011 .
- ^ a b Топ-10 продуктов с самым высоким содержанием тирозина
- ^ Hoffhines AJ, Damoc E, мосты KG, Лири JA Мур KL (декабрь 2006). «Обнаружение и очистка тирозин-сульфатированных белков с использованием нового моноклонального антитела против сульфтирозина» . Журнал биологической химии . 281 (49): 37877–87. DOI : 10.1074 / jbc.M609398200 . PMC 1764208 . PMID 17046811 .
- ^ Канан Y, Гамильтон RA, Sherry DM, Al-Ubaidi MR (декабрь 2012). «В центре внимания молекулы: сульфотирозин» . Экспериментальные исследования глаза . 105 : 85–6. дои : 10.1016 / j.exer.2012.02.014 . PMC 3629733 . PMID 22406006 .
- ^ Broadley KJ (март 2010). «Сосудистые эффекты следовых аминов и амфетаминов». Фармакология и терапия . 125 (3): 363–375. DOI : 10.1016 / j.pharmthera.2009.11.005 . PMID 19948186 .
- ^ Lindemann L, Hoener MC (май 2005). «Возрождение следовых аминов, вдохновленное новым семейством GPCR». Направления фармакологических наук . 26 (5): 274–281. DOI : 10.1016 / j.tips.2005.03.007 . PMID 15860375 .
- Перейти ↑ Wang X, Li J, Dong G, Yue J (февраль 2014 г.). «Эндогенные субстраты CYP2D мозга». Европейский журнал фармакологии . 724 : 211–218. DOI : 10.1016 / j.ejphar.2013.12.025 . PMID 24374199 .
- ↑ Zea-Rey AV, Cruz-Camino H, Vazquez-Cantu DL, Gutiérrez-García VM, Santos-Guzmán J, Cantú-Reyna C (27 ноября 2017 г.). «Заболеваемость преходящей неонатальной тирозинемией среди населения Мексики» . Журнал врожденных ошибок метаболизма и скрининга . 5 : 232640981774423. дои : 10,1177 / 2326409817744230 .
- ^ Бут Н., Масри MS, Robbins DJ, Эмерсон OH, Jones FT, деяниях F (1960). «Метаболизм тирозина фенольной кислоты в моче» . Журнал биологической химии . 235 (9): 2649–2652. DOI : 10.1016 / S0021-9258 (19) 76930-0 .
- ^ Мольнар Г.А., Вагнер З., Марко Л., Ко Сеги Т., Мохас М., Кочиш Б. и др. (Ноябрь 2005 г.). «Выведение орто-тирозина с мочой при сахарном диабете и почечной недостаточности: данные о продукции гидроксильных радикалов». Kidney International . 68 (5): 2281–7. DOI : 10.1111 / j.1523-1755.2005.00687.x . PMID 16221230 .
- ^ Молнар Г.А., Nemes В, Биро Z, Ludány А, Вагнер Z, Уиттманн I (декабрь 2005). «Накопление гидроксильных маркеров свободных радикалов мета, орто-тирозина и ДОФА в катарактальных линзах сопровождается более низким содержанием белка и фенилаланина в водорастворимой фазе». Свободно-радикальные исследования . 39 (12): 1359–66. DOI : 10.1080 / 10715760500307107 . PMID 16298866 . S2CID 31154432 .
- ^ Хамфри CE, Furegati М, Laumen К, La Vecchia л, Leutert Т, Мюллер-Hartwieg JC, Vogtle М (2007). «Оптимизированный синтез Lm-тирозина, пригодный для химического увеличения масштаба». Исследования и разработки в области органических процессов . 11 (6): 1069–1075. DOI : 10.1021 / op700093y .
- ^ Rasmussen DD, Ishizuka B, Куигли ME, Yen SS (октябрь 1983). «Влияние приема тирозина и триптофана на концентрацию катехоламинов в плазме и 3,4-дигидроксифенилуксусной кислоты». Журнал клинической эндокринологии и метаболизма . 57 (4): 760–3. DOI : 10,1210 / jcem-57-4-760 . PMID 6885965 .
- ^ Leathwood PD, Pollet P (1982). «Изменения настроения, вызванные диетой у нормальных людей». Журнал психиатрических исследований . 17 (2): 147–54. DOI : 10.1016 / 0022-3956 (82) 90016-4 . PMID 6764931 .
- ^ a b Deijen JB, Orlebeke JF (1994). «Влияние тирозина на когнитивные функции и артериальное давление при стрессе». Бюллетень исследований мозга . 33 (3): 319–23. DOI : 10.1016 / 0361-9230 (94) 90200-3 . PMID 8293316 . S2CID 33823121 .
- ^ Либерман HR, Corkin S, Весна BJ, Wurtman RJ, Growdon JH (август 1985). «Влияние диетических предшественников нейромедиаторов на поведение человека». Американский журнал клинического питания . 42 (2): 366–70. DOI : 10.1093 / ajcn / 42.2.366 . PMID 4025206 .
- ↑ a b Hao S, Avraham Y, Bonne O, Berry EM (февраль 2001 г.). «Потеря веса тела, вызванная разделением, нарушение поведения чередования и вегетативный тонус: эффекты тирозина». Фармакология, биохимия и поведение . 68 (2): 273–81. DOI : 10.1016 / S0091-3057 (00) 00448-2 . PMID 11267632 . S2CID 46405659 .
- ^ Мэджилл Р.А., Уотерс В.Ф., Брей Г.А., Волауфова Дж., Смит С.Р., Либерман Х.Р. и др. (Август 2003 г.). «Влияние тирозина, фентермина, кофеина D-амфетамина и плацебо на когнитивные и двигательные нарушения во время депривации сна». Пищевая неврология . 6 (4): 237–46. DOI : 10.1080 / 1028415031000120552 . PMID 12887140 . S2CID 21300076 .
- ^ Neri DF, Wiegmann D, Стани RR, Shappell SA, McCardie A, McKay DL (апрель 1995). «Влияние тирозина на когнитивные способности во время длительного бодрствования». Авиационная, космическая и экологическая медицина . 66 (4): 313–9. PMID 7794222 .
- ^ Reinstein DK, Lehnert H, Wurtman RJ (декабрь 1985). «Диетический тирозин подавляет повышение уровня кортикостерона в плазме после острого стресса у крыс». Науки о жизни . 37 (23): 2157–63. DOI : 10.1016 / 0024-3205 (85) 90566-1 . PMID 4068899 .
- ^ Deijen JB, Wientjes CJ, Vullinghs HF, Cloin PA, Langefeld JJ (январь 1999). «Тирозин улучшает когнитивные способности и снижает кровяное давление у курсантов после недели курса боевой подготовки». Бюллетень исследований мозга . 48 (2): 203–9. DOI : 10.1016 / S0361-9230 (98) 00163-4 . PMID 10230711 . S2CID 27927524 .
- ^ Махони CR, Кастеллани J, Kramer FM, Young A, Либерман HR (ноябрь 2007). «Добавки тирозина смягчают ухудшение рабочей памяти во время воздействия холода» . Физиология и поведение . 92 (4): 575–82. DOI : 10.1016 / j.physbeh.2007.05.003 . PMID 17585971 . S2CID 207372821 .
- ^ Chinevere TD, Sawyer RD, Creer AR, Conlee RK, Parcell AC (ноябрь 2002 г.). «Влияние приема L-тирозина и углеводов на выполнение упражнений на выносливость». Журнал прикладной физиологии . 93 (5): 1590–7. DOI : 10.1152 / japplphysiol.00625.2001 . PMID 12381742 .
- ^ Strüder HK, Холлман W, Валик P, Donike M, Gotzmann A, Weber K (апрель 1998). «Влияние пароксетина, аминокислот с разветвленной цепью и тирозина на реакции нейроэндокринной системы и утомляемость у людей». Гормоны и метаболические исследования = Hormon- und Stoffwechselforschung = Hormones et Metabolisme . 30 (4): 188–94. DOI : 10,1055 / с-2007-978864 . PMID 9623632 .
- ^ Томас JR, Локвуд PA, Singh A, Deuster PA (ноябрь 1999). «Тирозин улучшает рабочую память в многозадачной среде». Фармакология, биохимия и поведение . 64 (3): 495–500. DOI : 10.1016 / S0091-3057 (99) 00094-5 . PMID 10548261 . S2CID 24717770 .
- ^ Литке-Eversloh T, Сантос CN, Стефэнопулос G (декабрь 2007). «Перспективы биотехнологического производства L-тирозина и его применения». Прикладная микробиология и биотехнология . 77 (4): 751–62. DOI : 10.1007 / s00253-007-1243 у- . PMID 17968539 . S2CID 23088822 .
- ^ Чавес-Бежар М, Бэез-Виверос Дж, Мартинес А, Боливар F, G Госсет (2012). «Биотехнологическое производство L-тирозина и производных соединений». Биохимия процессов . 47 (7): 1017–1026. DOI : 10.1016 / j.procbio.2012.04.005 .
- ^ Литке-Eversloh T, Сантос CN, Стефэнопулос G (декабрь 2007). «Перспективы биотехнологического производства L-тирозина и его применения». Прикладная микробиология и биотехнология . 77 (4): 751–62. DOI : 10.1007 / s00253-007-1243 у- . PMID 17968539 . S2CID 23088822 .
Внешние ссылки [ править ]
- Тирозин MS Spectrum
- Метаболизм тирозина
- Биосинтез фенилаланина и тирозина
- Биосинтез фенилаланина, тирозина и триптофана
- Тирозин в базе данных ChemIDplus