 | |
 | |
| Имена | |
|---|---|
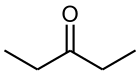
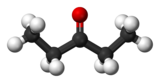
| Предпочтительное название IUPAC Пентан-3-он | |
| Другие названия Диэтилкетон, диэтилкетон, 3-пентанон, диметилацетон, пропион, метацетон, метацетон, этилкетон | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| Сокращения | DEK |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.002.265 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1156 |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| С 5 Н 10 О | |
| Молярная масса | 86,134 г · моль -1 |
| Появление | Бесцветная жидкость [1] |
| Запах | Ацетоноподобный [2] |
| Плотность | 0,81 г / см 3 при 20 ° C [2] |
| Температура плавления | -39 ° С (-38 ° F, 234 К) [2] |
| Точка кипения | 102 ° С (216 ° F, 375 К) [2] |
| 35 г / л [2] | |
| Давление газа | 35 мм рт. Ст. [1] |
| -58,14 · 10 −6 см 3 / моль | |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасность |
Положения об опасности GHS | H225 , H335 , H336 |
Меры предосторожности GHS | P210 , P233 , P240 , P241 , P242 , P243 , P261 , P271 , P280 , P303 + 361 + 353 , P304 + 340 , P312 , P370 + 378 , P403 + 233 , P403 + 235 , P405 , P501 |
| точка возгорания | 12,78 ° С (55,00 ° F, 285,93 К) |
самовоспламенения температуру | 425 ° С (797 ° F, 698 К) |
| Пределы взрываемости | 1,6% -6,4% [1] |
| NIOSH (пределы воздействия на здоровье в США): | |
PEL (Допустимо) | нет [1] |
REL (рекомендуется) | TWA 200 частей на миллион (705 мг / м 3 ) [1] |
IDLH (Непосредственная опасность) | ND [1] |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
3-пентанон (также известный как диэтилкетон ) представляет собой простой, симметричной диалкил кетон. Это бесцветный жидкий кетон с запахом ацетона . Он растворим примерно в 25 частях воды, но смешивается с органическими растворителями.
Использует [ редактировать ]
Он в основном используется в качестве растворителя в краске и предшественник витамина Е . [3]
Синтез [ править ]
Путь кетонового декарбоксилирования [ править ]
3-пентанон производятся кетоновым декарбоксилированием из пропановой кислоты с использованием катализаторов на основе оксидов металлов:
- 2 CH 3 CH 2 CO 2 H → (CH 3 CH 2 ) 2 CO + CO 2 + H 2 O
в лаборатории реакцию можно проводить в трубчатой печи . [4]
Путь карбонилирования [ править ]
Его также можно получить путем объединения этилена , CO и H 2 . [3] Когда реакция катализируется октакарбонилом дикобальта , в качестве источника водорода можно использовать воду. Предлагаемый промежуточный продукт представляет собой этилен-пропиониловые частицы [CH 3 C (O) Co (CO) 3 (этилен)], которые претерпевают мигрирующую вставку с образованием [CH 3 COCH 2 CH 2 Co (CO) 3 ]. Требуемый водород образуется в результате реакции конверсии воды . Подробнее см. [5]Если реакция водного сдвига не происходит, реакция дает полимер, содержащий чередующиеся звенья моноксида углерода и этилена. Такие алифатические поликетоны обычно получают с использованием палладиевых катализаторов. [6]
Безопасность [ править ]
Значение TLV для 3-пентанона составляет 200 частей на миллион (705 мг / м 3 ). [3] 3-пентанон может быть опасен при попадании на кожу или в глаза и может вызвать раздражение кожи и покраснение, слезотечение и зуд в глазах. Это химическое вещество также может вызвать повреждение нервной системы или органов при проглатывании. Хотя 3-пентанон считается стабильным, он легко воспламеняется при воздействии пламени, искр или другого источника тепла. В целях безопасности его следует хранить в шкафу для легковоспламеняющихся материалов вдали от источников тепла или источников возгорания, предпочтительно в прохладном, хорошо вентилируемом помещении. [7]
См. Также [ править ]
- 2-пентанон
- Метилизопропилкетон
Ссылки [ править ]
- ^ a b c d e f Карманный справочник NIOSH по химической опасности. «# 0212» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ a b c d e Запись в базе данных веществ GESTIS Института безопасности и гигиены труда
- ^ a b c Хардо Сигель, Манфред Эггерсдорфер «Кетоны» в Энциклопедии промышленной химии Ульмана , Wiley-VCH, 2002, Wiley-VCH, Wienheim. DOI : 10.1002 / 14356007.a15_077
- ^ Фернисс, Брайан; Ханнафорд, Энтони; Смит, Питер и Тэтчелл, Остин (1996). Учебник практической органической химии Фогеля (5-е изд.). Лондон: Longman Science & Technical. п. 613 . ISBN 9780582462366.
- ^ Мурата К .; Мацуда А. (1981). «Применение гомогенной реакции конверсии воды в газ III. Дальнейшее исследование гидрокарбонилирования - высокоселективного образования диэтилкетона из этилена, CO и H 2 O» . Бюллетень химического общества Японии . 54 (7): 2089–2092. DOI : 10.1246 / bcsj.54.2089 .
- ^ Дж. Лю; BT Heaton; Дж. А. Игго и Р. Уайман (2004). «Полное определение стадий инициации, распространения и завершения цикла карбометокси для карбоалкоксилирования этена с помощью Pd-дифосфановых катализаторов». Энгью. Chem. Int. Эд. 43 : 90–94. DOI : 10.1002 / anie.200352369 .
- ^ Химические вещества и лабораторное оборудование, Паспорт безопасности материала для 3-пентанона Архивировано 02января 2010 г.в Wayback Machine , ScienceLab.com, обновлено 11.06.2008