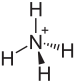| |||
 | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Гидросульфат аммония | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.332 | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
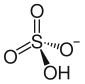
| (NH 4 ) HSO 4 | |||
| Молярная масса | 115,11 г / моль | ||
| Появление | Белое твердое вещество | ||
| Плотность | 1,78 г / см 3 | ||
| Температура плавления | 147 ° С (297 ° F, 420 К) | ||
| Очень растворим | |||
| Растворимость в других растворителях | Растворим в метаноле, не растворим в ацетоне | ||
| Опасности | |||
| Паспорт безопасности | Внешний паспорт безопасности материала | ||
| NFPA 704 (огненный алмаз) | |||
| Родственные соединения | |||
Другие анионы | Тиосульфат аммония Сульфит аммония Сульфат аммония Персульфат аммония | ||
Другие катионы | Бисульфат натрия Бисульфат калия | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Бисульфат аммония , также известный как гидросульфат аммония , представляет собой белое кристаллическое твердое вещество с формулой (NH 4 ) HSO 4 . Это продукт полунейтрализации серной кислоты аммиаком .
Производство [ править ]
Обычно он собирается как побочный продукт «ацетонциангидрина» в товарный химический метилметакрилат . [1]
Его также можно получить гидролизом сульфаминовой кислоты в водном растворе, в результате чего получают соль высокой чистоты:
- H 3 NSO 3 + H 2 O → [NH 4 ] + [HSO 4 ] -
Он также возникает при термическом разложении сульфата аммония :
- (NH 4 ) 2 SO 4 → (NH 4 ) HSO 4 + NH 3
Приложения [ править ]
В дальнейшем его можно нейтрализовать аммиаком с образованием сульфата аммония, ценного удобрения . Его можно использовать как более слабую альтернативу серной кислоте, хотя бисульфат натрия встречается гораздо чаще.
Естественное явление [ править ]
Родственное соединение формулы (NH 4 ) 3 H (SO 4 ) 2 встречается как редкий минерал летовицит , известный из окружающей среды угольных пожаров. [2] [3]
Ссылки [ править ]
- ^ Уильям Бауэр младший «Метакриловая кислота и производные» в Энциклопедии промышленной химии Ульмана 2002, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a16_441 .
- ^ https://www.mindat.org/min-2382.html
- ^ https://www.ima-mineralogy.org/Minlist.htm