 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК ацетат железа (III) | |
| Другие названия основной ацетат железа (III), оксиацетат железа (III), ацетат железа (III) | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ChemSpider | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C 14 H 27 Fe 3 O 18 | |
| Молярная масса | 650,9 г / моль |
| Появление | коричневато-красный аморфный порошок |
| Растворимость | растворим в этаноле [2] |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
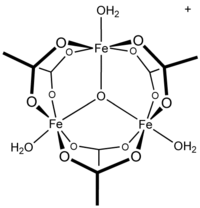
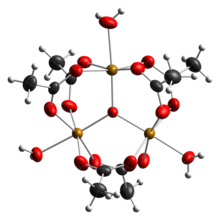
Ацетат железа - это ацетатная соль координационного комплекса [Fe 3 O (OAc) 6 (H 2 O) 3 ] + (OAc - представляет собой CH 3 CO 2 - ). Обычно соль известна как «основной ацетат железа». [3] Образование красно-коричневого комплекса когда-то использовалось в качестве теста на ионы трехвалентного железа . [4]
Структура и синтез [ править ]
Основной ацетат железа образуется при обработке водных растворов источников железа (III) ацетатными солями. [5] Типичным предшественником является свежеосажденный оксид / гидроксид железа, не содержащий галогенидов. [6]
Ранние исследования показали, что катион трехъядерный. [7] Центры Fe эквивалентны, каждый октаэдрический , связанный с шестью кислородными лигандами, включая трехкомпонентный оксид в центре равностороннего треугольника. [8] Соединение было ранним примером молекулярного комплекса железа с оксидным лигандом. Катион имеет идеализированную симметрию D 3h .
Реакции [ править ]
Концевые аквалиганды на триметаллическом каркасе могут быть замещены другими лигандами, такими как пиридин и диметилформамид . Известно множество различных солей по обмену аниона, например [Fe 3 (μ 3 -O) (OAc) 6 (H 2 O) 3 ] Cl. Восстановление катиона дает нейтральную производную со смешанной валентностью, которая содержит один центр железа и два центра железа. [3] Известны смешанные виды металлов, такие как [Fe 2 CoO (OAc) 6 (H 2 O) 3 ]. [9]
Родственные соединения [ править ]
Хром (III), рутений (III), ванадий (III) и родий (III) образуют аналогичные соединения. [10] Ацетат железа (III) (без оксолиганда) был заявлен как соединение красного цвета в результате реакции ацетата серебра и хлорида железа (III) . [11]
Использует [ редактировать ]
Материалы, полученные путем нагревания железа, уксусной кислоты и воздуха, которые можно описать как основные ацетаты железа, используются в качестве красителей и протравы . [3]
Ацетат железа часто наносят щеткой на необработанную древесину, чтобы придать ей вид состаренной древесины.
См. Также [ править ]
- Железо (II) ацетат
- Кобальта (II) ацетат
- Родия (II) ацетат
- Ацетат марганца (III)
- Хром (III) ацетат
Ссылки [ править ]
- ^ Лиде, Дэвид Р., изд. (2006). CRC Справочник по химии и физике (87-е изд.). Бока-Ратон, Флорида: CRC Press . С. 4–63. ISBN 0-8493-0487-3.
- ^ "Ацетат железа (III)" . EndMemo . Проверено 18 апреля 2015 года .
- ^ а б в Дж., Берджесс; МВ, Твигг (2005). Р. Брюс, Кинг; J., Wiley (ред.). Энциклопедия неорганической химии (2-е изд.). Нью-Йорк: Вили. ISBN 978-0-470-86078-6.
- ^ Х., Брирли; Ф., Ибботсон (1902). Анализ материалов металлургических заводов . Лондон; Нью-Йорк: Лонгманс, Грин. Архивировано из оригинала 18 апреля 2015 года.
- ^ W., Саймон (март 2007 г.). Руководство по химии . п. 474. ISBN 1406733350.
- ^ Х. Люкс (1963). «Ацетат основного железа (III)». В Георге Брауэре (ред.). Справочник по препаративной неорганической химии . п. 1508.
- ^ Weinland, R .; Динкелакер, П. (июль 1909 г.). "Uber Salze einer Hexaacetato (formiato) -trichrombase. II" (PDF) . Berichte der Deutschen Chemischen Gesellschaft . 42 (3): 2997–3018. DOI : 10.1002 / cber.19090420318 .
- ^ Фиггис, Б.Н.; Робертсон, Великобритания (13 февраля 1965 г.). "Кристалл-молекулярная структура и магнитные свойства Cr 3 (CH 3 . СОО) 6 OCl.5H 2 O". Природа . 205 (4972): 694–695. DOI : 10.1038 / 205694a0 . В статье описана изоструктура соединений хрома и железа.
- ^ Блейк, Энтони Б .; Явари, Ахмад; Hatfield, William E .; Сетулекшми, CN (1985). «Магнитные и спектроскопические свойства некоторых гетеротриядерных основных ацетатов хрома (III), железа (III) и ионов двухвалентных металлов». Журнал химического общества, Dalton Сделки (12): 2509. DOI : 10.1039 / DT9850002509 .
- ^ Холлеман, Арнольд Фредерик; Виберг, Эгон (2001), Виберг, Нильс (ред.), Неорганическая химия , перевод Иглсона, Мэри; Брюэр, Уильям, Сан-Диего / Берлин: Academic Press / De Gruyter, ISBN 0-12-352651-5
- ^ Пол, Ram C .; Нарула, Рамеш Ч .; Васишт, Шам К. (декабрь 1978 г.). «Ацетаты железа (III)». Химия переходных металлов . 3 (1): 35–38. DOI : 10.1007 / BF01393501 .
| AcOH | Он | |||||||||||||||||||
| LiOAc | Be (OAc) 2 BeAcOH | B (OAc) 3 | AcOAc ROAc | NH 4 OAc | AcOOH | FAc | Ne | |||||||||||||
| NaOAc | Mg (OAc) 2 | Al (OAc) 3 АЛСОЛ Al (OAc) 2 OH Al 2 SO 4 (OAc) 4 | Si | п | S | ClAc | Ar | |||||||||||||
| KOAc | Ca (OAc) 2 | Sc (OAc) 3 | Ti (OAc) 4 | VO (OAc) 3 | Cr (OAc) 2 Cr (OAc) 3 | Mn (OAc) 2 Mn (OAc) 3 | Fe (OAc) 2 Fe (OAc) 3 | Co (OAc) 2 | Ni (OAc) 2 | Cu (OAc) 2 | Zn (OAc) 2 | Ga (OAc) 3 | Ge | As (OAc) 3 | Se | BrAc | Kr | |||
| RbOAc | Sr (OAc) 2 | Y (OAc) 3 | Zr (OAc) 4 | Nb | Мо (OAc) 2 | Tc | Ru 2 (OAc) 4 Cl Ru (OAc) 3 | Rh 2 (OAc) 4 | Pd (OAc) 2 | AgOAc | Cd (OAc) 2 | В | Sn (OAc) 2 Sn (OAc) 4 | Sb (OAc) 3 | Te | IAc | Xe | |||
| CsOAc | Ba (OAc) 2 | * | Лу (OAc) 3 | Hf | Та | W | Re | Операционные системы | Ir | Pt (OAc) 2 | Au | Hg 2 (OAc) 2 , Hg (OAc) 2 | TlOAc Tl (OAc) 3 | Pb (OAc) 2 Pb (OAc) 4 | Bi (OAc) 3 | По | В | Rn | ||
| Пт | Ра | ** | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Ур. | Ц | Og | ||
| * | La (OAc) 3 | Ce (OAc) x | Pr | Nd | Вечера | Sm (OAc) 3 | Eu (OAc) 3 | Gd (OAc) 3 | Tb | Dy (OAc) 3 | Хо (OAc) 3 | Э | Тм | Yb (OAc) 3 | ||||||
| ** | Ac | Чт | Па | UO 2 (OAc) 2 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | ||||||