Биомаркер рака относится к веществу или процессу , который является показателем наличия рака в организме. Биомаркером может быть молекулой , секретируемый в опухоли или в ответ конкретного организма на наличие рака. Генетические , [1] эпигенетические , [2] протеомные , [3] гликомические , [4] и визуализирующие биомаркеры могут использоваться для диагностики рака, прогноза и эпидемиологии. В идеале такие биомаркеры можно анализировать в биологических жидкостях, собранных неинвазивным способом, таких как кровь или сыворотка. [5]
Несмотря на то, что существует множество проблем, связанных с переводом исследований биомаркеров в клиническую практику; некоторое количество биомаркеров на основе генов и белков уже использовалось при лечении пациентов; в том числе AFP ( рак печени ), BCR-ABL ( хронический миелоидный лейкоз ), BRCA1 / BRCA2 ( рак груди / яичников ), BRAF V600E ( меланома / колоректальный рак ), CA-125 (рак яичников), CA19.9 ( рак поджелудочной железы). ), CEA(Колоректальный рак), EGFR ( немелкоклеточная карцинома легкого ), HER-2 (рак молочной железы), KIT ( желудочно-кишечная стромальная опухоль ), PSA (специфический антиген простаты ) ( рак простаты ), S100 (меланома) и многие другие . [6] [7] [8] [9] [10] [11] [12] [13] [14] [15] Сами мутантные белки, обнаруживаемые с помощью мониторинга выборочных реакций (SRM) » , как сообщается, являются наиболее специфическими биомаркерами. для рака, потому что они могут возникнуть только из существующей опухоли. [16]Около 40% случаев рака можно вылечить, если выявить их на ранней стадии при обследовании. [17]
Определения биомаркеров рака [ править ]
Организации и публикации различаются по определению биомаркера . Во многих областях медицины биомаркеры ограничиваются белками, которые можно идентифицировать или измерить в крови или моче . Однако этот термин часто используется для обозначения любых молекулярных, биохимических, физиологических или анатомических свойств, которые можно количественно определить или измерить.
Национальный институт рака (NCI) , в частности, определяет биомаркер в виде: «биологическая молекула найдена в крови, других жидкостях организма, или тканях , что является признаком нормального или аномального процесса или состояния или заболевания. Биомаркер можно использовать, чтобы увидеть, насколько хорошо организм реагирует на лечение заболевания или состояния. Также называется молекулярным маркером и сигнатурной молекулой » [18].
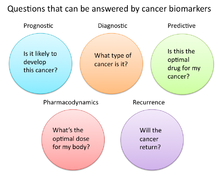
В исследованиях рака и медицине биомаркеры используются тремя основными способами: [19]
- Чтобы помочь диагностировать состояния, как в случае выявления рака на ранней стадии (Диагностика)
- Чтобы спрогнозировать, насколько агрессивным является состояние, например, в случае определения способности пациента жить без лечения (Прогноз)
- Чтобы предсказать, насколько хорошо пациент ответит на лечение (Прогнозирующий)
Роль биомаркеров в исследованиях рака и медицине [ править ]
Использование биомаркеров в медицине рака [ править ]
Оценка риска [ править ]
Биомаркеры рака, особенно те, которые связаны с генетическими мутациями или эпигенетическими изменениями, часто предлагают количественный способ определить, когда люди предрасположены к определенным типам рака. Известные примеры потенциально предсказывающих биомаркеров рака включают мутации генов KRAS , p53 , EGFR , erbB2 для рака толстой кишки , пищевода , печени и поджелудочной железы; мутации генов BRCA1 и BRCA2 для груди и яичников рака; аномальное метилированиеиз генов - супрессоров опухолей р16 , CDKN2B и p14ARF для рака мозга ; гиперметилирование MYOD1 , CDH1 и CDH13 при раке шейки матки ; и гиперметилирование p16 , p14 и RB1 при раке полости рта . [20]
Диагноз [ править ]
Биомаркеры рака также могут быть полезны при постановке конкретного диагноза. Это особенно актуально, когда необходимо определить, первичного или метастатического происхождения опухоль . Чтобы сделать это различие, исследователи могут сравнивать хромосомные изменения, обнаруженные в клетках, расположенных в первичном очаге опухоли, с изменениями, обнаруженными во вторичном очаге. Если изменения совпадают, вторичная опухоль может быть идентифицирована как метастатическая; тогда как, если изменения различаются, вторичная опухоль может быть идентифицирована как отдельная первичная опухоль. [21] Например, у людей с опухолями наблюдается высокий уровень циркулирующей опухолевой ДНК (ктДНК) из-за опухолевых клеток, прошедших апоптоз. [22]Этот онкомаркер можно обнаружить в крови, слюне или моче. [17] Возможность определения эффективного биомаркера для ранней диагностики рака недавно была поставлена под сомнение в свете высокой молекулярной гетерогенности опухолей, наблюдаемой в исследованиях секвенирования следующего поколения. [23]
Прогноз и прогнозы лечения [ править ]
Еще одно применение биомаркеров в медицине рака - это прогноз заболевания , который имеет место после того, как у человека был диагностирован рак. Здесь биомаркеры могут быть полезны для определения агрессивности выявленного рака, а также его вероятности ответа на данное лечение. Частично это связано с тем, что опухоли, демонстрирующие определенные биомаркеры, могут реагировать на лечение, связанное с экспрессией или присутствием этого биомаркера. Примеры таких прогностических биомаркеров включают повышенные уровни ингибитора металлопептидазы 1 (TIMP1) , маркера, связанного с более агрессивными формами множественной миеломы , [24] повышенный уровень рецептора эстрогена (ER) и / или рецептора прогестерона (PR).экспрессия, маркеры, связанные с лучшей общей выживаемостью у пациентов с раком груди; [25] [26] Амплификация гена HER2 / neu , маркер, указывающий на рак груди, вероятно, будет отвечать на лечение трастузумабом ; [27] [28] мутация в экзоне 11 протоонкогена c-KIT , маркера, указывающего на желудочно-кишечную стромальную опухоль (GIST) , вероятно, будет отвечать на лечение иматинибом ; [29] [30] и мутации в тирозинкиназном домене EGFR1 , маркера, указывающего на немелкоклеточный рак легкого (НМРЛ).вероятно ответит на лечение гефитинибом или эрлотинибом . [31] [32]
Фармакодинамика и фармакокинетика [ править ]
Биомаркеры рака также можно использовать для определения наиболее эффективного режима лечения рака конкретного человека. [33] Из-за различий в генетическом составе каждого человека некоторые люди метаболизируют или изменяют химическую структуру лекарств по-разному. В некоторых случаях снижение метаболизма некоторых лекарств может создать опасные условия, при которых в организме накапливается высокий уровень этого лекарства. Таким образом, при принятии решения о дозировке лекарств при лечении рака может помочь скрининг на такие биомаркеры. Примером может служить ген, кодирующий фермент тиопуринметилтрансферазу (TPMPT) . [34] Лица с мутациями в гене TPMT неспособны метаболизировать большое количество лекарственного средства от лейкемии , меркаптопурина., что потенциально может привести к фатальному падению количества лейкоцитов у таких пациентов. Таким образом, пациентам с мутациями TPMT рекомендуется назначать более низкую дозу меркаптопурина из соображений безопасности. [35]
Мониторинг реакции на лечение [ править ]
Биомаркеры рака также показали свою полезность в мониторинге эффективности лечения с течением времени. В этой конкретной области проводится много исследований, поскольку успешные биомаркеры могут обеспечить значительное снижение затрат на лечение пациентов, так как современные тесты на основе изображений, такие как КТ и МРТ для мониторинга состояния опухоли, являются очень дорогостоящими. [36]
Одним из примечательных биомаркеров, привлекающих значительное внимание, является белковый биомаркер S100 -beta при мониторинге реакции злокачественной меланомы . В таких меланомах меланоциты , клетки, вырабатывающие пигмент в нашей коже, производят белок S100-бета в высоких концентрациях, зависящих от количества раковых клеток. Таким образом, ответ на лечение связан со снижением уровня S100-бета в крови таких людей. [37] [38]
Точно так же дополнительные лабораторные исследования показали, что опухолевые клетки, подвергающиеся апоптозу, могут высвобождать клеточные компоненты, такие как цитохром с , нуклеосомы , расщепленный цитокератин-18 и E-кадгерин . Исследования показали, что эти и другие макромолекулы могут находиться в обращении во время лечения рака, обеспечивая потенциальный источник клинических показателей для мониторинга лечения. [36]
Повторение [ править ]
Биомаркеры рака также могут быть полезны для прогнозирования или мониторинга рецидивов рака . Oncotype DX® анализ рака молочной железы является одним из таких испытаний используются для прогнозирования вероятности рецидива рака молочной железы. Этот тест предназначен для женщин с ранней стадией (стадия I или II ) инвазивным раком груди с отрицательными лимфатическими узлами, положительным по рецепторам эстрогена (ER +), которым будет проводиться гормональная терапия . Oncotype DX рассматривает панель из 21 гена в клетках, взятых во время биопсии опухоли . Результаты теста представлены в виде шкалы рецидивов, которая указывает на вероятность рецидива через 10 лет. [39] [40]
Использование биомаркеров в исследованиях рака [ править ]
Разработка мишеней для лекарств [ править ]
В дополнение к их использованию в медицине рака, биомаркеры часто используются в процессе разработки лекарств от рака. Например, в 1960-х годах исследователи обнаружили, что у большинства пациентов с хроническим миелогенным лейкозом имеется особая генетическая аномалия на хромосомах 9 и 22, названная филадельфийской хромосомой . Когда эти две хромосомы объединяются, они создают вызывающий рак ген, известный как BCR-ABL . У таких пациентов этот ген действует как основная начальная точка всех физиологических проявлений лейкемии. В течение многих лет BCR-ABL просто использовался в качестве биомаркера для стратификации определенного подтипа лейкемии. Однако в конечном итоге разработчики лекарств смогли разработать иматиниб., мощное лекарство, которое эффективно ингибирует этот белок и значительно снижает продукцию клеток, содержащих филадельфийскую хромосому. [41] [42]
Суррогатные конечные точки [ править ]
Еще одна многообещающая область применения биомаркеров - суррогатные конечные точки . В этом приложении биомаркеры выступают в качестве замены эффектов лекарственного средства на прогрессирование рака и выживаемость. В идеале использование проверенных биомаркеров избавит пациентов от необходимости проходить биопсию опухоли и длительные клинические испытания, чтобы определить, подействует ли новый препарат. В текущем стандарте лечения метрика для определения эффективности лекарства состоит в том, чтобы проверить, снизило ли оно прогрессирование рака у людей и, в конечном итоге, продлит ли оно выживаемость. Однако успешные суррогаты биомаркеров могут значительно сэкономить время, усилия и деньги, если некачественные препараты можно будет исключить из процесса разработки до того, как они попадут на клинические испытания.
Некоторые идеальные характеристики биомаркеров суррогатных конечных точек включают: [43] [44]
- Биомаркер должен участвовать в процессе, вызывающем рак.
- Изменения биомаркера должны коррелировать с изменениями заболевания.
- Уровни биомаркеров должны быть достаточно высокими, чтобы их можно было легко и надежно измерить.
- Уровни или наличие биомаркера должны легко различать нормальную, злокачественную и предраковую ткань.
- Эффективное лечение рака должно изменить уровень биомаркера.
- Уровень биомаркера не должен изменяться спонтанно или в ответ на другие факторы, не связанные с успешным лечением рака.
В частности, две области, которые привлекают внимание в качестве суррогатных маркеров, включают циркулирующие опухолевые клетки (ЦКО) [45] [46] и циркулирующие миРНК . [47] [48] Оба этих маркера связаны с количеством опухолевых клеток, присутствующих в крови, и, как таковые, можно надеяться, что они станут суррогатом для прогрессирования опухоли и метастазирования . Однако существенные препятствия на пути их принятия включают сложность обогащения, идентификации и измерения уровней CTC и miRNA в крови. Для их внедрения в клиническую практику, вероятно, потребуются новые технологии и исследования. [49] [50] [51]
Типы биомаркеров рака [ править ]
Биомаркеры молекулярного рака [ править ]
| Тип опухоли | Биомаркер |
|---|---|
| Грудь | ER / PR (рецептор эстрогена / рецептор прогестерона) [52] [53] |
| HER-2 / neu [52] [53] | |
| Колоректальный | EGFR [52] [53] |
| КРАС [52] [54] | |
| UGT1A1 [52] [54] | |
| Желудочный | HER-2 / neu [52] |
| СУТЬ | c-KIT [52] [55] |
| Лейкемия / лимфома | CD20 [52] [56] |
| CD30 [52] [57] | |
| FIP1L1 - PDGFRalpha [52] [58] | |
| PDGFR [52] [59] | |
| Филадельфийская хромосома ( BCR / ABL ) [52] [60] [61] | |
| PML / RAR-альфа [52] [62] | |
| TPMT [52] [63] | |
| UGT1A1 [52] [64] | |
| Легкое | EML4 / ALK [52] [65] [66] |
| EGFR [52] [53] | |
| КРАС [52] [53] | |
| Меланома | BRAF [52] [66] |
| Поджелудочная железа | Повышенный уровень лейцина , изолейцина и валина [67] |
| Яичники | СА-125 [68] |
Другие примеры биомаркеров:
- Подавители опухолей, утраченные при раке
- Примеры: BRCA1 , BRCA2.
- РНК
- Примеры: мРНК , микроРНК [69]
- Белки, содержащиеся в жидкостях или тканях организма.
- Примеры: простатоспецифический антиген и СА-125.
- Антитела к раковым антигенам
- Примеры: полиомавирус клеток Меркеля [70]
- ДНК
- Примеры: Циркулирующая опухолевая ДНК ( цДНК ) [17]
Биомаркеры рака без специфики [ править ]
Не все биомаркеры рака должны быть специфичными для разных типов рака. Некоторые биомаркеры, обнаруженные в системе кровообращения, можно использовать для определения аномального роста клеток, присутствующих в организме. Все эти типы биомаркеров можно определить с помощью диагностических анализов крови, что является одной из основных причин, по которой нужно регулярно проходить тестирование на здоровье. Регулярно проходя анализы, многие проблемы со здоровьем, такие как рак, можно обнаружить на ранней стадии, что предотвратит многие смерти.
Было показано, что соотношение нейтрофилов и лимфоцитов является неспецифическим детерминантом для многих видов рака. Это соотношение фокусируется на активности двух компонентов иммунной системы, которые участвуют в воспалительной реакции, которая, как было показано, выше при наличии злокачественных опухолей. [71] Кроме того, основной фактор роста фибробластов ( bFGF ) - это белок, который участвует в пролиферации клеток. К сожалению, было показано, что при наличии опухолей он очень активен, что привело к выводу, что он может способствовать более быстрому размножению злокачественных клеток. [72] Исследования показали, что антитела против bFGF можно использовать для лечения опухолей различного происхождения. [72] Кроме того, инсулиноподобный фактор роста(IGF-R) участвует в пролиферации и росте клеток. Возможно, он участвует в подавлении апоптоза, запрограммированной гибели клеток из-за какого-либо дефекта. [73] Из-за этого уровни IGF-R могут быть увеличены при наличии рака груди, простаты, легких и толстой кишки. [74]
| Биомаркер | Описание | Используемый биосенсор |
|---|---|---|
| NLR (отношение нейтрофилов к лимфоцитам) | Повышается при воспалении, вызванном раком [75] | Нет |
| Базовый фактор роста фибробластов (bFGF) | Этот уровень увеличивается при наличии опухоли, способствует быстрому размножению опухолевых клеток [76] | Электрохимический [77] |
| Инсулиноподобный фактор роста (IGF-R) | Высокая активность в раковых клетках, способствует размножению [78] | Датчик спектроскопии электрохимического импеданса [ необходима ссылка ] |
См. Также [ править ]
- Онкомаркер
Ссылки [ править ]
- ^ Кальцоне, Кэтлин А. (2012). «Генетические биомаркеры риска рака». Семинары по онкологическому сестринскому делу . 28 (2): 122–128. DOI : 10.1016 / j.soncn.2012.03.007 . PMID 22542320 .
- ^ Герцег, Зденко; Эно, Пьер (01.06.2007). «Генетические и эпигенетические изменения как биомаркеры для обнаружения, диагностики и прогноза рака» . Молекулярная онкология . 1 (1): 26–41. DOI : 10.1016 / j.molonc.2007.01.004 . ISSN 1878-0261 . PMC 5543860 . PMID 19383285 .
- ^ Ли, Данни; Чан, Дэниел В. (2014-04-01). «Протеомные биомаркеры рака от открытия до утверждения: усилия стоят того» . Экспертный обзор протеомики . 11 (2): 135–136. DOI : 10.1586 / 14789450.2014.897614 . ISSN 1478-9450 . PMC 4079106 . PMID 24646122 .
- ^ Aizpurua-Olaizola, O .; Тораньо, Х. Састре; Фалькон-Перес, JM; Уильямс, С .; Reichardt, N .; Бунс, Г.-Дж. (2018). «Масс-спектрометрия для открытия гликановых биомаркеров». Тенденции TrAC в аналитической химии . 100 : 7–14. DOI : 10.1016 / j.trac.2017.12.015 .
- ^ Мишра, Алок; Верма, Мукеш (2010). «Биомаркеры рака: готовы ли мы к прайм-тайму?» . Раки . 2 (1): 190–208. DOI : 10,3390 / cancers2010190 . PMC 3827599 . PMID 24281040 .
- ^ Рея, Жанна; Росс Дж. Молинаро (март 2011 г.). «Биомаркеры рака: выжить в пути от скамейки к постели» . Наблюдатель в медицинской лаборатории. Архивировано из оригинального 14 октября 2013 года . Проверено 26 апреля 2013 года . CS1 maint: обескураженный параметр ( ссылка )
- ^ Бене, Тара; Копур, М. Ситки (1 января 2012 г.). «Биомаркеры гепатоцеллюлярной карциномы» . Международный журнал гепатологии . 2012 : 859076. дои : 10,1155 / 2012/859076 . PMC 3357951 . PMID 22655201 .
- ^ Мусолино, А; Белла, Массачусетс; Бортеси, Б; Michiara, M; Нальди, N; Zanelli, P; Капеллетти, М; Pezzuolo, D; Camisa, R; Сави, М; Нери, ТМ; Ардиццони, А (июнь 2007 г.). «Мутации BRCA, молекулярные маркеры и клинические переменные при раннем начале рака груди: популяционное исследование». Грудь . 16 (3): 280–92. DOI : 10.1016 / j.breast.2006.12.003 . hdl : 11381/1629553 . PMID 17257844 .
- ^ Dienstmann, R; Табернеро, Дж. (Март 2011 г.). «BRAF как мишень для лечения рака». Противораковые средства в медицинской химии . 11 (3): 285–95. DOI : 10.2174 / 187152011795347469 . PMID 21426297 .
- ^ Лампарелла, N; Барохия, А; Альмокадем, С (2013). Влияние генетических маркеров на лечение немелкоклеточного рака легкого . Успехи экспериментальной медицины и биологии . 779 . С. 145–64. DOI : 10.1007 / 978-1-4614-6176-0_6 . ISBN 978-1-4614-6175-3. PMID 23288638 .
- ^ Орфанос, G; Контоуракис, П. (2012). «Ориентация на рецептор HER2 при метастатическом раке молочной железы» . Гематология / Онкология и терапия стволовыми клетками . 5 (3): 127–37. DOI : 10.5144 / 1658-3876.2012.127 . PMID 23095788 .
- ^ DePrimo, SE; Хуанг, X .; Blackstein, ME; Гарретт, CR; Хармон, CS; Schoffski, P .; Шах, MH; Verweij, J .; Баум, СМ; Деметри, Г.Д. (8 сентября 2009 г.). «Уровни циркулирующего растворимого KIT служат биомаркером для клинических результатов у пациентов с желудочно-кишечными стромальными опухолями, получающих сунитиниб после неэффективности иматиниба» . Клинические исследования рака . 15 (18): 5869–5877. DOI : 10.1158 / 1078-0432.CCR-08-2480 . PMC 3500590 . PMID 19737953 .
- ^ Бантис, А; Grammaticos, P (сентябрь – декабрь 2012 г.). «Простатический специфический антиген и сканирование костей в диагностике и последующем наблюдении рака простаты. Можно ли повысить диагностическое значение ПСА?». Греческий журнал ядерной медицины . 15 (3): 241–6. PMID 23227460 .
- ^ Kruijff, S; Хукстра, HJ (апрель 2012 г.). «Текущее состояние S-100B как биомаркера меланомы». Европейский журнал хирургической онкологии . 38 (4): 281–5. DOI : 10.1016 / j.ejso.2011.12.005 . PMID 22240030 .
- ^ Людвиг, JA; Вайнштейн, Дж. Н. (ноябрь 2005 г.). «Биомаркеры в стадии рака, прогнозе и выборе лечения» . Обзоры природы Рак . 5 (11): 845–56. DOI : 10.1038 / nrc1739 . PMID 16239904 .
- ^ Ван, Цин; Рагхотама Чаркади (декабрь 2010 г.). «Мутантные белки как биомаркеры рака» . Труды Национальной академии наук . 108 (6): 2444–2449. Bibcode : 2011PNAS..108.2444W . DOI : 10.1073 / pnas.1019203108 . PMC 3038743 . PMID 21248225 .
- ^ a b c Ли, Сюаньин; Е, Менша; Чжан, Вэйин; Тан, Дуэт; Яффрезич-Рено, Николь; Ян, Сюй; Го, Чжэньчжун (01.02.2019). «Жидкая биопсия циркулирующей опухолевой ДНК и биосенсорные приложения» . Биосенсоры и биоэлектроника . 126 : 596–607. DOI : 10.1016 / j.bios.2018.11.037 . ISSN 0956-5663 . PMID 30502682 .
- ^ «биомаркер» . Словарь терминов по раку NCI . Национальный институт рака. 2011-02-02.
- ^ «Биомаркеры рака: Вводное руководство для адвокатов» (PDF) . Сеть пропаганды исследований. 2010. Архивировано из оригинального (PDF) 29.10.2013 . Проверено 26 апреля 2013 года . CS1 maint: обескураженный параметр ( ссылка )
- ^ Верма, М; Манн, Ю (октябрь 2006 г.). «Генетические и эпигенетические биомаркеры в диагностике рака и выявлении групп высокого риска» . Критические обзоры в онкологии / гематологии . 60 (1): 9–18. DOI : 10.1016 / j.critrevonc.2006.04.002 . PMID 16829121 .
- ^ Леонг, PP; Резаи, Б; Кох, WM; Рид, А; Eisele, D; Ли, диджей; Сидранский, Д; Джен, Дж; Westra, WH (1 июля 1998 г.). «Отличие вторых первичных опухолей от метастазов в легких у пациентов с плоскоклеточным раком головы и шеи» . Журнал Национального института рака . 90 (13): 972–7. DOI : 10.1093 / JNCI / 90.13.972 . PMID 9665144 .
- ^ Лапин, Мортен; Олтедал, Сату; Тьенсволл, Кьерсти; Буль, Тове; Smaaland, Руна; Гарресори, Хериш; Явле, Милинд; Гленен, Нильс Идар; Абельсет, Бенте Кристин; Гилье, Бьёрнар; Нордгард, Оддмунд (6 ноября 2018 г.). «Размер фрагмента и уровень внеклеточной ДНК обеспечивают прогностическую информацию у пациентов с распространенным раком поджелудочной железы» . Журнал трансляционной медицины . 16 (1): 300. DOI : 10,1186 / s12967-018-1677-2 . ISSN 1479-5876 . PMC 6218961 . PMID 30400802 .
- ^ Драгани, TA; Матарезе, V; Коломбо, Ф (2020). «Биомаркеры для ранней диагностики рака: перспективы успеха через призму опухолевой генетики». BioEssays . 42 (4): e1900122. DOI : 10.1002 / bies.201900122 . PMID 32128843 .
- ^ Terpos Е, Dimopoulos М.А., Шривастава В, и др. (Март 2010 г.). «Высокие уровни сывороточного ТИМП-1 коррелируют с запущенным заболеванием и предсказывают плохую выживаемость у пациентов с множественной миеломой, леченных новыми препаратами». Исследование лейкемии . 34 (3): 399–402. DOI : 10.1016 / j.leukres.2009.08.035 . PMID 19781774 .
- ^ Куукасъярви, Т; Кононен, Дж; Helin, H; Холли, К; Изола, Дж. (Сентябрь 1996 г.). «Потеря рецептора эстрогена при рецидивирующем раке груди связана с плохим ответом на эндокринную терапию». Журнал клинической онкологии . 14 (9): 2584–9. DOI : 10.1200 / jco.1996.14.9.2584 . PMID 8823339 .
- ^ Харрис, L; Fritsche, H; Mennel, R; Нортон, L; Равдин, П; Таубе, S; Сомерфилд, MR; Hayes, DF; Bast RC, Jr; Американское общество клинической онкологии (20 ноября 2007 г.). «Американское общество клинической онкологии, обновление 2007 г. рекомендаций по использованию онкомаркеров при раке груди». Журнал клинической онкологии . 25 (33): 5287–312. DOI : 10.1200 / JCO.2007.14.2364 . PMID 17954709 .
- ^ Kröger, N; Milde-Langosch, K; Ритдорф, S; Schmoor, C; Шумахер, М; Зандер, АР; Лёнинг, Т. (1 января 2006 г.). «Прогностические и прогностические эффекты иммуногистохимических факторов у пациентов с первичным раком молочной железы высокого риска» . Клинические исследования рака . 12 (1): 159–68. DOI : 10.1158 / 1078-0432.CCR-05-1340 . PMID 16397038 .
- ^ Vrbic, S; Пейчич, я; Филипович, S; Кочич, Б; Врбич, М. (январь – март 2013 г.). «Текущая и будущая терапия против HER2 при раке груди». Журнал Балканского союза онкологов . 18 (1): 4–16. PMID 23613383 .
- ^ Yoo, C; Рю, MH; Ryoo, BY; Бек, MY; Канг, YK (17 апреля 2013 г.). «Эффективность, безопасность и фармакокинетика увеличения дозы иматиниба до 800 мг / день у пациентов с распространенными опухолями стромы желудочно-кишечного тракта». Новые исследуемые препараты . 31 (5): 1367–74. DOI : 10.1007 / s10637-013-9961-8 . PMID 23591629 .
- ^ Деметри, GD; van Oosterom, AT; Гарретт, CR; Blackstein, ME; Шах, MH; Verweij, J; McArthur, G; Джадсон, Ирландия; Генрих, MC; Morgan, JA; Desai, J; Флетчер, CD; Джордж, S; Bello, CL; Хуанг, X; Баум, СМ; Casali, PG (14 октября 2006 г.). «Эффективность и безопасность сунитиниба у пациентов с запущенной стромальной опухолью желудочно-кишечного тракта после неэффективности иматиниба: рандомизированное контролируемое исследование». Ланцет . 368 (9544): 1329–38. DOI : 10.1016 / S0140-6736 (06) 69446-4 . PMID 17046465 .
- ^ Herbst, RS; Prager, D; Hermann, R; Ференбахер, Л; Джонсон, BE; Сандлер, А; Крис, MG; Тран, HT; Klein, P; Ли, Х; Ramies, D; Джонсон, DH; Миллер, Вирджиния; Исследовательская группа TRIBUTE (1 сентября 2005 г.). «TRIBUTE: испытание фазы III гидрохлорида эрлотиниба (OSI-774) в сочетании с химиотерапией карбоплатином и паклитакселом при запущенном немелкоклеточном раке легкого». Журнал клинической онкологии . 23 (25): 5892–9. DOI : 10.1200 / JCO.2005.02.840 . PMID 16043829 .
- ^ Линч, TJ; Белл, DW; Sordella, R; Гурубхагаватула, S; Окимото, РА; Бранниган, BW; Harris, PL; Хазерлат, С.М. Супко, Ю.Г.; Халуска, Ф.Г .; Луи, DN; Кристиани, округ Колумбия; Сеттлман, Дж; Габер, Д.А. (20 мая 2004 г.). «Активирующие мутации в рецепторе эпидермального фактора роста, лежащие в основе реакции немелкоклеточного рака легкого на гефитиниб» (PDF) . Медицинский журнал Новой Англии . 350 (21): 2129–39. DOI : 10.1056 / NEJMoa040938 . PMID 15118073 .
- ^ Sawyers CL (апрель 2008). «Проблема биомаркера рака». Природа . 452 (7187): 548–52. Bibcode : 2008Natur.452..548S . DOI : 10,1038 / природа06913 . PMID 18385728 .
- ^ Карась-Кузелицкий, N; Млинарич-Раскан, I (август 2009 г.). «Индивидуализация тиопуриновой терапии: тиопурин-S-метилтрансфераза и не только». Фармакогеномика . 10 (8): 1309–22. DOI : 10,2217 / pgs.09.78 . PMID 19663675 .
- ^ Реллинг М.В., Хэнкок М.Л., Ривера Г.К. и др. (Декабрь 1999 г.). «Непереносимость меркаптопуриновой терапии и гетерозиготность по локусу гена тиопурин-S-метилтрансферазы» . Журнал Национального института рака . 91 (23): 2001–8. DOI : 10.1093 / JNCI / 91.23.2001 . PMID 10580024 .
- ^ a b Шнайдер, Джон; Манприт К. Сидху; Синтия Дусе; Ноэми Кисс; Роберт Л. Осфельдт; Дональд Чалфин (2012). «Экономика онкологических биомаркеров» . Персонализированная медицина . 9 (8): 829–837. DOI : 10,2217 / pme.12.87 . PMID 29776231 .
- ^ Хенце, G; Даммер, Р. Joller-Jemelka, HI; Böni, R; Бург, Г. (1997). «Сыворотка S100 - маркер для мониторинга болезни при метастатической меланоме». Дерматология . 194 (3): 208–12. DOI : 10.1159 / 000246103 . PMID 9187834 .
- ^ Harpio, R; Эйнарссон, Р. (июль 2004 г.). «Белки S100 как биомаркеры рака с акцентом на S100B при злокачественной меланоме». Клиническая биохимия . 37 (7): 512–8. DOI : 10.1016 / j.clinbiochem.2004.05.012 . PMID 15234232 .
- ^ Ламонд, Северо-Запад; Skedgel, C; Юнис, Т. (апрель 2013 г.). «Является ли оценка рецидива 21 гена экономически эффективным методом при эндокринно-чувствительном раке молочной железы без лимфоузлов?». Экспертный обзор фармакоэкономических исследований и результатов исследований . 13 (2): 243–50. DOI : 10.1586 / erp.13.4 . PMID 23570435 .
- ^ Бирощак, младший; Шварц, GF; Палаццо, JP; Плата, AD; Brill, KL; Джаслоу, RJ; Ли, SY (май 2013 г.). «Влияние Oncotype DX на решения о лечении при ER-положительном, отрицательном по узлу раке молочной железы с гистологической корреляцией». Журнал груди . 19 (3): 269–75. DOI : 10.1111 / tbj.12099 . PMID 23614365 .
- ^ Moen, MD; McKeage, K; Плоскер, Г.Л .; Сиддики, Массачусетс (2007). «Иматиниб: обзор его использования при хроническом миелоидном лейкозе». Наркотики . 67 (2): 299–320. DOI : 10.2165 / 00003495-200767020-00010 . PMID 17284091 .
- ^ Лимоник, Майкл; Алиса Парк (28 мая 2001 г.). «Новая надежда рака» . Журнал Time . Проверено 26 апреля 2013 года . CS1 maint: обескураженный параметр ( ссылка )
- ^ Цена, C; Макдоннелл, Д. (февраль 1991 г.). «Влияние фильтрации ниобия и постоянного потенциала на сенситометрические отклики стоматологических рентгенографических пленок». Челюстно-лицевая радиология . 20 (1): 11–6. DOI : 10,1259 / dmfr.20.1.1884846 . PMID 1884846 .
- ^ Коэн, Виктор; Фадло Хури (2003). «Прогресс в химиопрофилактике рака легких» (PDF) . Борьба с раком . 10 (4): 315–324. DOI : 10.1177 / 107327480301000406 . PMID 12915810 . Проверено 26 апреля 2013 года . CS1 maint: обескураженный параметр ( ссылка )[ постоянная мертвая ссылка ]
- ^ Лу, CY; Цай, HL; Uen, YH; Ху, HM; Чен, CW; Cheng, TL; Lin, SR; Ван, JY (5 марта 2013 г.). «Циркулирующие опухолевые клетки как суррогатный маркер для определения клинического исхода химиотерапии mFOLFOX у пациентов с раком толстой кишки III стадии» . Британский журнал рака . 108 (4): 791–7. DOI : 10.1038 / bjc.2012.595 . PMC 3590657 . PMID 23422758 .
- ^ Balic, M; Уильямс, А; Lin, H; Датар, Р; Кот, RJ (2013). «Циркулирующие опухолевые клетки: от скамейки к постели» . Ежегодный обзор медицины . 64 : 31–44. DOI : 10.1146 / annurev-med-050311-163404 . PMC 3809995 . PMID 23092385 .
- ^ Мадхаван, D; Цукник, М; Wallwiener, M; Цук, К; Modugno, C; Шарпфф, М; Schott, S; Хайль, Дж; Турчинович А; Ян, Р; Беннер, А; Ритдорф, S; Трамп, А; Sohn, C; Пантел, К; Schneeweiss, A; Burwinkel, B (1 ноября 2012 г.). «Циркулирующие миРНК как суррогатные маркеры циркулирующих опухолевых клеток и прогностические маркеры при метастатическом раке молочной железы» . Клинические исследования рака . 18 (21): 5972–82. DOI : 10.1158 / 1078-0432.CCR-12-1407 . PMID 22952344 .
- ^ Редова, М; Сана, Дж; Слаби, О (март 2013). «Циркулирующие миРНК как новые биомаркеры крови для солидного рака». Будущая онкология . 9 (3): 387–402. DOI : 10.2217 / fon.12.192 . PMID 23469974 .
- ^ Joosse, SA; Пантель, К. (1 января 2013 г.). «Биологические проблемы при обнаружении циркулирующих опухолевых клеток» . Исследования рака . 73 (1): 8–11. DOI : 10.1158 / 0008-5472.CAN-12-3422 . PMID 23271724 .
- ^ Hou, HW; Варкиани, Мэн; Khoo, BL; Li, ZR; Су, РА; Tan, DS; Lim, WT; Хан, Дж; Бхагат, AA; Лим, CT (2013). «Выделение и извлечение циркулирующих опухолевых клеток с помощью центробежных сил» . Научные отчеты . 3 : 1259. Bibcode : 2013NatSR ... 3E1259H . DOI : 10.1038 / srep01259 . PMC 3569917 . PMID 23405273 .
- ^ Дхондт, Берт; Де Блезер, Элиза; Клэйс, Том; Бюленс, Сара; Люмен, Николаас; Вандесомпеле, Джо; Бекерс, Аннелин; Фонтейн, Валери; Ван дер Экен, Ким; Де Брюйкер, Орели; Поль, Жером; Грамм, Пьер; Ост, Пит (21 декабря 2018 г.). «Открытие и проверка сигнатуры сывороточной микроРНК для характеристики олиго- и полиметастатического рака простаты: пока не готовы» . Всемирный журнал урологии . 37 (12): 2557–2564. DOI : 10.1007 / s00345-018-2609-8 . hdl : 1854 / LU-8586484 . PMID 30578441 .
- ^ a b c d e f g h i j k l m n o p q r s «Таблица фармакогеномных биомаркеров на этикетках лекарств» . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США.
- ^ a b c d e "Информационный бюллетень по опухолевым маркерам" (PDF) . Американское онкологическое общество.
- ^ a b Хайнц-Йозеф Ленц (18 сентября 2012 г.). Биомаркеры в онкологии: прогноз и прогноз . Springer Science & Business Media. п. 263. ISBN. 978-1-4419-9754-8.
- Перейти ↑ Gonzalez RS, Carlson G, Page AJ, Cohen C (июль 2011). «Маркеры стромальных опухолей желудочно-кишечного тракта при меланомах кожи: взаимосвязь с прогностическими факторами и исходом» . Американский журнал клинической патологии . 136 (1): 74–80. DOI : 10.1309 / AJCP9KHD7DCHWLMO . PMID 21685034 .
- ^ Tam CS, Otero-Palacios J, Abruzzo LV, et al. (Апрель 2008 г.). «Экспрессия CD20 хронического лимфоцитарного лейкоза зависит от генетического подтипа: исследование количественной проточной цитометрии и флуоресцентной гибридизации in-situ у 510 пациентов» . Британский журнал гематологии . 141 (1): 36–40. DOI : 10.1111 / j.1365-2141.2008.07012.x . PMID 18324964 .
- ^ Zhang M, Yao Z, Patel H, et al. (Май 2007 г.). «Эффективная терапия мышиных моделей лейкемии и лимфомы человека радиоактивно меченным анти-CD30 антителом, HeFi-1» . Труды Национальной академии наук Соединенных Штатов Америки . 104 (20): 8444–8. Bibcode : 2007PNAS..104.8444Z . DOI : 10.1073 / pnas.0702496104 . PMC 1895969 . PMID 17488826 .
- ↑ Yamada Y, Sanchez-Aguilera A, Brandt EB, et al. (Сентябрь 2008 г.). «FIP1L1 / PDGFRalpha взаимодействует с SCF, чтобы вызвать системный мастоцитоз на мышиной модели хронического эозинофильного лейкоза / гиперэозинофильного синдрома» . Кровь . 112 (6): 2500–7. DOI : 10.1182 / кровь-2007-11-126268 . PMID 18539901 .
- ^ Nimer SD (май 2008). «Миелодиспластические синдромы» . Кровь . 111 (10): 4841–51. DOI : 10.1182 / кровь-2007-08-078139 . PMID 18467609 . S2CID 6802096 .
- ^ Оттманн О., Домбрет Х, Мартинелли Г. и др. (Октябрь 2007 г.). «Дазатиниб вызывает быстрые гематологические и цитогенетические реакции у взрослых пациентов с острым лимфобластным лейкозом, положительным по филадельфийской хромосоме, с устойчивостью или непереносимостью иматиниба: промежуточные результаты исследования фазы 2» . Кровь . 110 (7): 2309–15. DOI : 10.1182 / кровь-2007-02-073528 . PMID 17496201 .
- ^ Булос Н., Малдер Х.Л., Калабрезе CR и др. (Март 2011 г.). «Химиотерапевтические агенты предотвращают появление устойчивых к дазатинибу мутаций киназы BCR-ABL в точной мышиной модели острого лимфобластного лейкоза с положительной хромосомой в Филадельфии» . Кровь . 117 (13): 3585–95. DOI : 10.1182 / кровь-2010-08-301267 . PMC 3072880 . PMID 21263154 .
- ^ О'Коннелл PA, Madureira PA, Берман JN, Ливски RS, Waisman DM (апрель 2011). «Регулирование S100A10 онкобелком PML-RAR-α» . Кровь . 117 (15): 4095–105. DOI : 10.1182 / кровь-2010-07-298851 . PMID 21310922 .
- ^ Duffy MJ, Crown J (ноябрь 2008). «Индивидуальный подход к лечению рака: как могут помочь биомаркеры» . Клиническая химия . 54 (11): 1770–9. DOI : 10,1373 / clinchem.2008.110056 . PMID 18801934 .
- ^ Ribrag V, Koscielny S, Casasnovas O и др. (Апрель 2009 г.). «Фармакогенетическое исследование лимфом Ходжкина показывает влияние полиморфизма UGT1A1 на прогноз пациентов» . Кровь . 113 (14): 3307–13. DOI : 10.1182 / кровь-2008-03-148874 . PMID 18768784 .
- ↑ Li Y, Ye X, Liu J, Zha J, Pei L (январь 2011 г.). «Оценка слитых белков EML4-ALK при немелкоклеточном раке легкого с использованием низкомолекулярных ингибиторов» . Неоплазия . 13 (1): 1–11. DOI : 10.1593 / neo.101120 . PMC 3022423 . PMID 21245935 .
- ^ a b Pao W, Girard N (февраль 2011 г.). «Новые мутации драйвера при немелкоклеточном раке легкого». Ланцет Онкология . 12 (2): 175–80. DOI : 10.1016 / S1470-2045 (10) 70087-5 . PMID 21277552 .
- ^ Hewes, Arlington (2 октября 2014). «Перспективный метод выявления рака поджелудочной железы за годы до традиционной диагностики» . Singularity HUB . Проверено 22 апреля 2016 .
- ^ Гупта, Дигант; Лис, Кристофер Г. (2009-10-09). «Роль CA125 в прогнозировании выживаемости при раке яичников - обзор эпидемиологической литературы» . Журнал исследований яичников . 2 (1): 13. DOI : 10,1186 / 1757-2215-2-13 . ISSN 1757-2215 . PMC 2764643 . PMID 19818123 .
- ^ Bartels CL, Tsongalis GJ (апрель 2009). «МикроРНК: новые биомаркеры рака человека» . Клиническая химия . 55 (4): 623–31. DOI : 10,1373 / clinchem.2008.112805 . PMID 19246618 .
- ^ Полсон, Келли G .; Льюис, Кристофер В .; Редман, Мэри В .; Саймонсон, Уильям Т .; Лисберг, Аарон; Риттер, Дебора; Моришима, Тихиро; Хатчинсон, Кэтлин; Мудгистратова, Лола; Блом, Астрид; Айер, Джаясри; Мошири, Ата С .; Tarabadkar, Erica S .; Картер, Джозеф Дж .; Бхатия, Шайлендер; Кавасуми, Масаоки; Galloway, Denise A .; Wener, Mark H .; Нгием, Пол (2017). «Вирусные онкопротеиновые антитела как маркер рецидива карциномы из клеток Меркеля: проспективное валидационное исследование» . Рак . 123 (8): 1464–1474. DOI : 10.1002 / cncr.30475 . PMC 5384867 . PMID 27925665 .
- ^ Проктор, MJ; Макмиллан, округ Колумбия; Моррисон, DS; Флетчер, CD; Хорган, PG; Кларк, SJ (24 июля 2012 г.). «Производное соотношение нейтрофилов к лимфоцитам предсказывает выживаемость больных раком» . Британский журнал рака . 107 (4): 695–699. DOI : 10.1038 / bjc.2012.292 . ISSN 0007-0920 . PMC 3419948 . PMID 22828611 .
- ^ a b Лю, человек; Син, Лу-Ци (2017-06-07). «Базовый фактор роста фибробластов как потенциальный биомаркер для диагностики метастазов злокачественных опухолей у женщин» . Письма онкологии . 14 (2): 1561–1567. DOI : 10.3892 / ol.2017.6335 . ISSN 1792-1074 . PMC 5529833 . PMID 28789380 .
- ^ Фюрстенбергер, Грегор; Сенн, Ханс-Йорг (май 2002 г.). «Инсулиноподобные факторы роста и рак». Ланцетная онкология . 3 (5): 298–302. DOI : 10.1016 / s1470-2045 (02) 00731-3 . ISSN 1470-2045 . PMID 12067807 .
- ^ Ю, Герберт; Рохан, Томас (2000-09-20). «Роль семейства инсулиноподобных факторов роста в развитии и прогрессировании рака» . JNCI: Журнал Национального института рака . 92 (18): 1472–1489. DOI : 10.1093 / JNCI / 92.18.1472 . ISSN 0027-8874 . PMID 10995803 .
- ^ Вано, Янн-Александр; Удар, Стефан; Автор, Мари-Аньес; Тету, Полина; Тибо, Констанция; Абудагга, приветствую! Скотте, Флориан; Элаиди, Реза (2018-04-06). «Оптимальный предел для соотношения нейтрофилов и лимфоцитов: факт или вымысел? Проспективное когортное исследование у пациентов с метастатическим раком» . PLOS ONE . 13 (4): e0195042. Bibcode : 2018PLoSO..1395042V . DOI : 10.1371 / journal.pone.0195042 . ISSN 1932-6203 . PMC 5889159 . PMID 29624591 .
- ^ Лю, человек; Син, Лу-Ци (2017-08-01). «Базовый фактор роста фибробластов как потенциальный биомаркер для диагностики метастазов злокачественных опухолей у женщин» . Письма онкологии . 14 (2): 1561–1567. DOI : 10.3892 / ol.2017.6335 . ISSN 1792-1074 . PMC 5529833 . PMID 28789380 .
- ^ Торренте-Родригес, Ребека М .; Руис-Вальдепеньяс Монтьель, Виктор; Кампузано, Сусана; Педреро, Мария; Фарчадо, Мерьем; Варгас, Ева; Мануэль де Вильена, Ф. Хавьер; Гарранцо-Асенсио, Мария; Бардерас, Родриго; Пингаррон, Хосе М. (4 апреля 2017 г.). «Электрохимический датчик для быстрого определения рецептора 4 фактора роста фибробластов в сырых лизатах раковых клеток» . PLOS ONE . 12 (4): e0175056. Bibcode : 2017PLoSO..1275056T . DOI : 10.1371 / journal.pone.0175056 . ISSN 1932-6203 . PMC 5380347 . PMID 28376106 .
- ^ Дендулури, Сахитья К .; Идову, Олумуива; Ван, Чжунлян; Ляо, Чжань; Ян, Чжэнцзянь; Мохаммед, Марьям К .; Е, Цзиксин; Вэй, Цян; Ван, Цзин; Чжао, Лянгун; Луу, Хюэ Х. (март 2015 г.). «Передача сигналов инсулиноподобного фактора роста (IGF) при онкогенезе и развитии лекарственной устойчивости рака» . Гены и болезни . 2 (1): 13–25. DOI : 10.1016 / j.gendis.2014.10.004 . ISSN 2352-3042 . PMC 4431759 . PMID 25984556 .