| Имена | |||
|---|---|---|---|
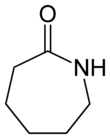
| Имена ИЮПАК Азепан-2-он (предпочтительное название IUPAC) Гексано-6-лактам (разрешенная альтернатива) | |||
| Другие названия ε-Капролактам 1-Аза-2-циклогептанон 2-Азациклогептанон Капрон PK4 Изооксим циклогексанона Экстром 6N Гексагидро-2-азепинон Гексагидро-2H-азепин-2-он (9CI) Гексанолактам Аминокапроновый лактам | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 106934 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.013 | ||
| Номер ЕС |
| ||
| 101802 | |||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 6 H 11 N O | |||
| Молярная масса | 113,160 г · моль -1 | ||
| Появление | Белое твердое вещество | ||
| Плотность | 1,01 г / см 3 | ||
| Температура плавления | 69,2 ° С (156,6 ° F, 342,3 К) | ||
| Точка кипения | 270,8 ° C (519,4 ° F, 544,0 К) при 1013,25 гПа | ||
| 866,89 г / л (22 ° С) | |||
| Давление газа | 0,00000008 мм рт. Ст. (20 ° C) [1] | ||
| Опасности | |||
| Пиктограммы GHS |  | ||
| Сигнальное слово GHS | Предупреждение | ||
| H302 , H315 , H319 , H332 , H335 | |||
| Р261 , Р264 , Р270 , Р271 , Р280 , Р301 + 312 , P302 + 352 , Р304 + 312 , Р304 + 340 , P305 + 351 + 338 , P312 , P321 , P330 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , P405 , P501 | |||
| точка возгорания | 125 ° С (257 ° F, 398 К) | ||
| Пределы взрываемости | 1,4% -8,0% [1] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | нет [1] | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Капролактам ( CPL ) представляет собой органическое соединение с формулой (CH 2 ) 5 C (O) NH. Это бесцветное твердое вещество представляет собой лактам (циклический амид ) капроновой кислоты . Мировой спрос на это соединение составляет примерно пять миллионов тонн в год, и подавляющее большинство из них используется для производства нитей, волокон и пластиков из нейлона 6 . [2]
Синтез и производство [ править ]
Капролактам был впервые описан в конце 1800-х годов, когда он был получен циклизацией ε- аминокапроновой кислоты , продукта гидролиза капролактама. По оценкам, мировой спрос на капролактам в 2015 году достигнет пяти миллионов тонн в год. 90% производимого капролактама используется для производства волокон и волокна, 10% - для пластмасс, а небольшое количество используется в качестве промежуточного химического продукта. [2] Из-за его коммерческого значения было разработано множество методов производства капролактама. Было подсчитано, что 90% всего капролактама синтезируется из циклогексанона ( 1 ), который сначала превращается в его оксим ( 2 ). Обработка этого оксима кислотой вызываетПерегруппировка Бекмана с образованием капролактама ( 3 ): [2]
Непосредственным продуктом кислотной перегруппировки является бисульфатная соль капролактама. Эта соль нейтрализуется аммиаком для высвобождения свободного лактама и совместного образования сульфата аммония . При оптимизации производственной практики большое внимание уделяется минимизации производства солей аммония. [2]
Другой крупный промышленный путь включает образование оксима из циклогексана с использованием нитрозилхлорида , и на этот метод приходится 10% мирового производства. [2] Преимущество этого метода в том, что циклогексан дешевле, чем циклогексанон .
Другие пути получения капролактама включают деполимеризацию отработанного нейлона 6 и реакцию капролактона с аммиаком. [2] В лабораторных условиях сообщалось о реакции циклогексанона с азойной кислотой с образованием капролактама в реакции Шмидта . [3]
Использует [ редактировать ]
Почти весь производимый капролактам идет на производство нейлона 6 . Превращение влечет за собой полимеризацию с раскрытием цикла :
Нейлон 6 широко используется в волокнах и пластмассах .
Анионная полимеризация in situ используется для производства литого нейлона, где преобразование ε-капролактама в нейлон 6 происходит внутри формы. В связи с обработкой бесконечных волокон часто используется термин трансферное формование из термопластической смолы (T-RTM).
Капролактам также используется в синтезе нескольких фармацевтических препаратов, включая пентилентетразол , мептазинол и лаурокапрам .
Безопасность [ править ]
Капролактам является раздражителем и умеренно токсичен , его LD 50 составляет 1,1 г / кг (крыса, перорально). В 1991 году он был включен в список опасных загрязнителей воздуха Законом США о чистом воздухе 1990 года . Впоследствии он был исключен из списка в 1996 году по просьбе производителей. [4] В воде капролактам гидролизуется до аминокапроновой кислоты , которая используется в медицине.
В настоящее время не существует официального установленного предела допустимого воздействия для рабочих, работающих с капролактамом в США. Рекомендуемый предел воздействия устанавливаются в 1 мг / м 3 в течение восьми часов рабочей смены для капролактама пыли и паров. Предел кратковременного воздействия устанавливается на уровне 3 мг / м 3 для капролактама пыли и паров. [5]
Ссылки [ править ]
- ^ a b c Карманный справочник NIOSH по химической опасности. «# 0097» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Б с д е ф Josef Ritz; Хьюго Фукс; Хайнц Кечка; Уильям С. Моран. «Капролактам». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a05_031.pub2 .
- ^ Эрик Дж. Канторовски; Марк Дж. Курт (2000). «Расширение до семичленных колец». Тетраэдр . 56 (26): 4317–4353. DOI : 10.1016 / S0040-4020 (00) 00218-0 .
- ^ EPA - Модификации к 112 (b) 1 Опасные загрязнители воздуха
- ^ NIOSH Карманный справочник по химической опасности , CDC , извлеченной ноября +8, 2013