 | |
| Идентификаторы | |
|---|---|
3D модель ( JSmol ) | |
| |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Карборановые кислоты H (CXB
11Y
5Z
6) (X, Y, Z = H, Alk, F, Cl, Br, CF 3 ) представляют собой класс суперкислот , [1] некоторые из которых, по оценкам, как минимум в миллион раз сильнее, чем 100% чистая серная кислота в их значения функции кислотности Гаммета ( H 0 ≤ –18) и рассчитанные значения p K a значительно ниже –20, что делает их одними из самых сильных известных кислот Бренстеда. [2] [3] [4] Наиболее хорошо изученным примером является высокохлорированное производное H (CHB
11Cl
11) . Кислотность H (CHB
11Cl
11) Было установлено , что значительно превышать трифторметансульфокислоты , CF
3ТАК
3Н , и bistriflimide , (CF
3ТАК
2)
2NH , соединения, ранее считавшиеся сильнейшими из выделяемых кислот.
Их высокая кислотность связана с обширной делокализацией их сопряженных оснований, карборанат-анионов (CXB 11 Y 5 Z 6 - ), которые обычно дополнительно стабилизируются электроотрицательными группами, такими как Cl, F и CF 3 . Из-за отсутствия окислительных свойств и исключительно низкой нуклеофильности и высокой стабильности их сопряженных оснований они являются единственными суперкислотами, которые, как известно, протонируют фуллерен C 60, не разлагая его. [5] [6] Кроме того, они образуют стабильные выделяемые соли с протонированным бензолом , C 6 H 7 +, исходное соединение промежуточных продуктов Веланда, встречающихся в реакциях электрофильного ароматического замещения .
Фторированная карборановая кислота, H (CHB
11F
11) , даже сильнее, чем хлорированная карборановая кислота. Он способен протонировать бутан с образованием трет- бутильного катиона при комнатной температуре и является единственной известной кислотой, которая протонирует диоксид углерода с образованием мостикового катиона [H (CO
2)
2]+
, что делает его, возможно, самой сильной из известных кислот. В частности, CO 2 не подвергается заметному протонированию при обработке смешанными суперкислотами HF-SbF 5 или HSO 3 F-SbF 5 . [7] [8] [9] [10]
Как класс, карборановые кислоты образуют наиболее кислотную группу четко определенных выделяемых веществ, известных, гораздо более кислых, чем ранее известные однокомпонентные сильные кислоты, такие как трифликовая кислота или хлорная кислота . В некоторых случаях, подобно почти пергалогенированным производным, упомянутым выше, их кислотность конкурирует (и, возможно, превышает) кислотность традиционных смешанных суперкислот Льюиса-Бренстеда, таких как магическая кислота и фторантимоновая кислота . (Однако прямое сравнение до сих пор было невозможно из-за отсутствия меры кислотности, подходящей для обоих классов кислот: значения p K a плохо определены для химически сложных смешанных кислот, в то время как H 0 значения не могут быть измерены для очень высокоплавких карбановых кислот).
Кислотность [ править ]
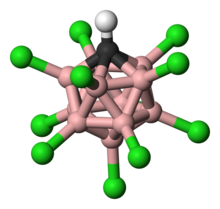
11Cl
11) было показано, что он является мономерным в газовой фазе, причем кислотный протон (показан красным ) связан с Cl (12) и вторично связан с Cl (7). Мономерная форма является метастабильной при конденсации, но в конечном итоге полимеризуется с образованием структуры с кислотным протонным мостиком между карборановыми звеньями. [11] ( Примечание : линии между атомами углерода и бора карборанового ядра показывают связность, но не должны интерпретироваться как одинарные связи. Порядок связи меньше единицы из-за недостатка электронов.)
Сила кислоты Бренстеда-Лоури соответствует ее способности выделять ионы водорода. Одной из распространенных мер силы кислоты для концентрированных суперкислотных жидких сред является функция кислотности Гаммета, H 0 . Основываясь на своей способности количественно протонировать бензол, хлорированная карборановая кислота H (CHB
11Cl
11) был консервативно оценен как имеющий значение H 0 на уровне -18 или ниже, что привело к общепринятому утверждению, что карборановые кислоты по крайней мере в миллион раз сильнее, чем 100% -ная серная кислота ( H 0 = -12). [12] [13] Однако, поскольку значение H 0 измеряет протонирующую способность жидкой среды, кристаллическая и тугоплавкая природа этих кислот препятствует прямому измерению этого параметра. С точки зрения p K a , несколько иной показатель кислотности, определяемый как способность данного растворенного вещества подвергаться ионизации в растворителе, карборановые кислоты, по оценкам, имеют p K a.значения ниже -20, даже без электроноакцепторных заместителей на атомах бора (например, H (CHB
11ЧАС
11), по оценкам, имеет ap K a, равное -24), [14] с (пока неизвестным) полностью фторированным аналогом H (CHB
11F
11) с расчетным p K a, равным -46. [4] Известная кислота H (CHB
11F
11) с одним фтором меньше, как ожидается, будет лишь немного слабее (p K a <-40).
В газовой фазе H (CHB
11F
11) имеет расчетную кислотность 216 ккал / моль по сравнению с экспериментально определенной кислотностью 241 ккал / моль (в разумном соответствии с расчетным значением 230 ккал / моль) для H (CHB
11Cl
11) . Напротив, HSbF 6 (упрощенная модель для протонодонорных частиц во фторированной антимоновой кислоте ) имеет расчетную кислотность в газовой фазе 255 ккал / моль, в то время как предыдущим экспериментально определенным рекордсменом был (C 4 F 9 SO 2 ) 2 NH, a конгенер бистрифлимида , 291 ккал / моль. Таким образом, H (CHB
11F
11) , вероятно, является наиболее кислотным веществом, синтезированным до сих пор в массе, с точки зрения его кислотности в газовой фазе. Ввиду его уникальной реакционной способности, он также является сильным претендентом на звание самого кислого вещества в конденсированной фазе (см. Выше). Были предсказаны некоторые еще более сильнокислые производные с кислотностью газовой фазы <200 ккал / моль. [15] [16]
Карборановые кислоты отличаются от классических суперкислот тем, что они являются однокомпонентными веществами. Напротив, классические суперкислоты часто представляют собой смеси кислоты Бренстеда и кислоты Льюиса (например, HF / SbF 5 ). [17] Несмотря на то, что борные карбоновые кислоты являются самой сильной кислотой, они описываются как «мягкие», чисто протонирующие слабоосновные вещества без дальнейших побочных реакций. [18] В то время как обычные суперкислоты разлагают фуллерены из-за их сильно окисляющего кислотного компонента Льюиса, карборановая кислота обладает способностью протонировать фуллерены при комнатной температуре с образованием выделяемой соли. [19] [20]Кроме того, анион, образующийся в результате переноса протона, почти полностью инертен. Это свойство делает карборановые кислоты единственными веществами, сравнимыми по кислотности со смешанными суперкислотами, которые также можно хранить в стеклянной бутылке, поскольку различные вещества, дающие фтор (которые атакуют стекло), отсутствуют или не образуются. [21] [19]
История [ править ]
Карборановая кислота была впервые обнаружена и синтезирована профессором Кристофером Ридом и его коллегами в 2004 году в Калифорнийском университете в Риверсайде. [20] До открытия карборановой кислоты давний рекорд «сильнейших кислот как отдельных выделяемых соединений» держали две суперкислоты, фторсульфоновая кислота и трифторметансульфоновая кислота, с p K a s -14 и -16 соответственно. [22] Исходная молекула, из которой происходит карборановая кислота, икосаэдрический карборанат-анион, ГХБ.
11ЧАС-
11, был впервые синтезирован в DuPont в 1967 году Уолтером Нотом. Исследования свойств этой молекулы были приостановлены до середины 1980-х годов, когда чешская группа ученых-борников Плешек, Штибр и Гержманек усовершенствовали процесс галогенирования молекул карборана. Эти открытия сыграли важную роль в разработке современной процедуры синтеза карборановой кислоты. [19] [22] Процесс состоит из обработки Cs + [HCB 11 H 11 ] - с SO
2Cl
2кипячение с обратным холодильником в сухом аргоне для полного хлорирования молекулы с образованием карборановой кислоты, но было показано, что это полностью хлорируется только при определенных условиях. [23] [19] [24]
В 2010 году Рид опубликовал руководство, в котором подробно описаны процедуры синтеза карборановых кислот и их производных. [25] Тем не менее, синтез карборановых кислот остается длительным и трудным и требует хорошо обслуживаемого перчаточного бокса и специального оборудования. Исходным материалом является коммерчески доступный декаборан (14) , высокотоксичное вещество. Наиболее изучена карборановая кислота H (CHB
11Cl
11) готовится за 13 шагов. Последние несколько этапов особенно чувствительны и требуют перчаточного бокса при <1 ppm H 2 O без каких-либо паров слабощелочного растворителя, поскольку такие слабые основания, как бензол или дихлорметан, будут реагировать с электрофилами на основе карборана и кислотами Бренстеда. Заключительным этапом синтеза является метатезис карборанатной соли μ-гидридодисилилия с избыточной жидкостью, безводным хлористым водородом, предположительно за счет образования прочных связей Si – Cl и H – H в летучих побочных продуктах:
- [Et 3 Si – H – SiEt 3 ] + [HCB 11 Cl 11 ] - + 2HCl → H (CHB
11Cl
11) + 2Et 3 SiCl + H 2
- [Et 3 Si – H – SiEt 3 ] + [HCB 11 Cl 11 ] - + 2HCl → H (CHB
Продукт был выделен испарением побочных продуктов и охарактеризован его инфракрасным (ν CH = 3023 см -1 ) и ядерным магнитным резонансом (δ 4,55 (с, 1H, CH), 20,4 (с, 1H, H + ) в жидкости. SO 2 ) спектры (обратите внимание на чрезвычайно слабопольный химический сдвиг кислотного протона). [25] Хотя реакции, используемые в синтезе, аналогичны, получение чистого образца более кислого H (CHB
11F
11) оказалось еще сложнее, требуя чрезвычайно строгих процедур для исключения следов слабоосновных примесей. [7]
Структура [ править ]
Карборановая кислота состоит из 11 атомов бора; каждый атом бора связан с атомом хлора. Атомы хлора служат для повышения кислотности и действуют как щит от атак извне из-за стерических препятствий, которые они создают вокруг кластера. Кластер, состоящий из 11 боров, 11 хлора и одного атома углерода, спарен с атомом водорода, связанным с атомом углерода. Атомам бора и углерода позволяют образовывать шесть связей из-за способности бора образовывать трехцентровые двухэлектронные связи. [22]
- Бор обладает способностью образовывать «связь трех центров и двух электронов». Здесь представлены резонансные структуры связи 3c-2e в диборане.
Хотя структура карборановой кислоты сильно отличается от обычных кислот, обе распределяют заряд и стабильность одинаковым образом. Карборанат-анион распределяет свой заряд, делокализуя электроны по 12 атомам клетки. [26] Это было показано в исследовании дифракции рентгеновских лучей на монокристалле, показавшем укороченную длину связи в гетероциклической части кольца, что свидетельствует об электронной делокализации. [27]
Хлорированный карбаклозо- додекаборат-анион ГХБ
11Cl-
11 представляет собой исключительно стабильный анион с тем, что ранее было описано как «замещающе инертные» вершины B – Cl.
Дескриптор closo указывает, что молекула формально является производной ( заменой B-на-C + ) из борана стехиометрии и заряда [B n H n ] 2– ( n = 12 для известных карборановых кислот). [28] Кубовидная структура, образованная 11 атомами бора и 1 атомом углерода, позволяет электронам быть сильно делокализованными через трехмерную клетку (специальная стабилизация карборановой системы была названа «σ-ароматичностью») и требует высокой энергии. разрушение борной кластерной части молекулы - вот что придает аниону его замечательную стабильность. [28]Поскольку анион чрезвычайно стабилен, он не будет вести себя как нуклеофил по отношению к протонированному субстрату, в то время как сама кислота полностью не окисляет, в отличие от кислотных компонентов Льюиса многих суперкислот, таких как пентафторид сурьмы. Следовательно, чувствительные молекулы, такие как C 60, могут протонироваться без разложения. [29] [30]
Использование [ править ]
Существует множество предлагаемых применений карборановых кислот на основе бора. Например, они были предложены в качестве катализаторов крекинга углеводородов и изомеризации н- алканов с образованием разветвленных изоалканов (например, «изооктана»). Карборановые кислоты могут также использоваться в качестве сильных селективных кислот Бренстеда для тонкого химического синтеза, где низкая нуклеофильность противоаниона может быть преимуществом. В механистической органической химии они могут быть использованы для изучения реакционноспособных катионных интермедиатов. [31] В неорганическом синтезе их беспрецедентная кислотность может позволить изолировать экзотические виды, такие как соли протонированного ксенона. [21] [22] [32]
Ссылки [ править ]
- ^ Обратите внимание, что на изображении кислотный протон не связан с карбораном, но это не отображаемый противоион.
- ^ Олах, Джорджия; Пракаш, ГКС; Sommer, J .; Мольнар, А. (2009). Суперкислотная химия (2-е изд.). Вайли. п. 41. ISBN 978-0-471-59668-4.
- ^ То есть, если бы он был жидким, протонирующая способность чистого образца карборановой суперкислоты, измеренная по активности H + , была бы в миллион раз выше, чем у 100% -ной серной кислоты .
- ^ a b Липпинг, Лаури; Лейто, Иво; Коппель, Ивар; Кроссинг, Инго; Химмель, Даниэль; Коппель, Ильмар А. (2015-01-14). «Сверхкислотность кислот Бренстеда на основе клозо-додекабората: исследование DFT». Журнал физической химии . 119 (4): 735–743. Bibcode : 2015JPCA..119..735L . DOI : 10.1021 / jp506485x . PMID 25513897 .
- ^ Юхас, М .; Hoffmann, S .; Стоянов, Е .; Kim, K.-C .; Рид, Калифорния (2004). «Самая сильная выделяемая кислота» . Angewandte Chemie International Edition . 43 (40): 5352–5355. DOI : 10.1002 / anie.200460005 . PMID 15468064 .
- Перейти ↑ Reed, CA (2005). «Карборановые кислоты. Новые« сильные, но мягкие »кислоты для органической и неорганической химии» (PDF) . Химические коммуникации . 2005 (13): 1669–1677. DOI : 10.1039 / b415425h . PMID 15791295 .
- ^ а б Нава Мэтью (2013). «Самая сильная кислота Бренстеда: протонирование алканов H (CHB11F11) при комнатной температуре» . Angewandte Chemie International Edition . 53 (4): 1131–1134. DOI : 10.1002 / anie.201308586 . PMC 4993161 . PMID 24339386 .
- ^ Рид CA (2013). «Мифы о протоне. Природа H + в конденсированных средах» . В соотв. Chem. Res . 46 (11): 2567–75. DOI : 10.1021 / ar400064q . PMC 3833890 . PMID 23875729 .
- ^ Рид CA (2013). «Мифы о протоне. Природа H + в конденсированных средах» . В соотв. Chem. Res . 46 (11): 2567–75. DOI : 10.1021 / ar400064q . PMC 3833890 . PMID 23875729 .
- ^ Каммингс, Стивен; Гратчян, Грант П .; Рид, Кристофер А. (22 января 2016 г.). «Самая сильная кислота: протонирование углекислого газа» . Angewandte Chemie International Edition . 55 (4): 1382–1386. DOI : 10.1002 / anie.201509425 . ISSN 1521-3773 . PMID 26663640 .
- ^ Стоянов, Евгений С .; Hoffmann, Stephan P .; Юхас, Марк; Рид, Кристофер А. (март 2006 г.). «Структура сильнейшей кислоты Бренстеда: карборановая кислота H (CHB11Cl11)» (PDF) . Журнал Американского химического общества . 128 (10): 3160–3161. DOI : 10.1021 / ja058581l . ISSN 0002-7863 . PMID 16522093 .
- ↑ Рид, Калифорния (октябрь 2011 г.). «Самая сильная кислота». Chem. Новая Зеландия . 75 : 174–179. DOI : 10.1002 / chin.201210266 . S2CID 6226748 .
- ^ Олах, Джорджия; Пракаш, ГКС; Sommer, J .; Мольнар, А. (2009). Суперкислотная химия (2-е изд.). Вайли. п. 41. ISBN 978-0-471-59668-4 .
- ^ Значения p K a рассчитаны для 1,2-дихлорэтана в качестве растворителя, причем p K a пикриновой кислоты для удобства «привязан» к 0. Поскольку водный p K a пикриновой кислоты равен 0,4, эти расчетные значения дают приблизительную оценку p K a карборанов в воде.
- ^ Мейер, Мэтью М .; Ван, Сюэ-Бинь; Рид, Кристофер А .; Ван, Лай-Шэн; Касс, Стивен Р. (23 декабря 2009 г.). «Исследование слабого для оценки сильного: экспериментальное определение энергии связи электронов карборановых анионов и кислотности карборановых кислот в газовой фазе» . Журнал Американского химического общества . 131 (50): 18050–18051. DOI : 10.1021 / ja908964h . ISSN 1520-5126 . PMID 19950932 .
- ^ Липпинг, Лаури; Лейто, Иво; Коппель, Ивар; Коппель, Ильмар А. (19 ноября 2009 г.). "Сверхкислотность по Бренстеду в газовой фазе некоторых производных монокарба-клозо-боратов: вычислительное исследование". Журнал физической химии . 113 (46): 12972–12978. Bibcode : 2009JPCA..11312972L . DOI : 10.1021 / jp905449k . ISSN 1089-5639 . PMID 19807147 .
- ^ Рид, Кристофер. «Карборановые кислоты. Новые« сильные, но мягкие »кислоты для органической и иногронной химии». Предварительная статья (февраль 2005 г.). Проверено 13 февраля 2015 г.
- ^ Рид, Кристофер А. «Самая сильная кислота». Химия в Новой Зеландии (октябрь 2011 г.): 174-179. По состоянию на 13 февраля 2015 г.
- ^ a b c d Juhasz M .; Hoffmann S .; Стоянов Э .; Ким К.-С .; Рид CA (2004). «Самая сильная выделяемая кислота» . Angewandte Chemie International Edition . 43 (40): 5352–5355. DOI : 10.1002 / anie.200460005 . PMID 15468064 .
- ^ а б Рид CA (2005). «Карборановые кислоты. Новые« сильные, но мягкие »кислоты для органической и неорганической химии» . Химические сообщения (Представленная рукопись). 2005 (13): 1669–1677. Doi : 10.1039 / b415425h . PMID 15791295 .
- ^ a b Хопкин, М. (2004, 1 ноября). Создана сильнейшая кислота в мире. Получено 3 марта 2015 г. с http://www.nature.com/news/2004/041115/full/news041115-5.html.
- ^ a b c d Сато Кентаро, «Самая сильная кислота в мире». Музей органической химии. Доступ 13 февраля 2015 г.
- ^ "Обратное дело". Химические коммуникации . 46 (48): 9259. 28 декабря 2010 г. DOI : 10.1039 / C0CC90142C . ISSN 1364-548X .
- ^ Gu, W., McCulloch, Билли J, Reibenspies, Иосиф, и Озеров, Олег Васильевич (2010, 1 февраля). Chemical Communications Получено 5 марта 2015 г. с http://pubs.rsc.org/en/content/articlepdf/2010/cc/c001555e.
- ^ a b Рид, Кристофер А. (19 января 2010 г.). «Реагенты H +, CH3 + и R3Si + -карборан: когда трифлаты не работают» . Счета химических исследований . 43 (1): 121–128. DOI : 10.1021 / ar900159e . ISSN 0001-4842 . PMC 2808449 . PMID 19736934 .
- ^ Эль-Хеллани А .; Лавалло В. (2014). «Слияние N-гетероциклических карбенов с карборан-анионами». Энгью. Chem. Int. Эд . 53 (17): 4489–4493. DOI : 10.1002 / anie.201402445 . PMID 24664969 .
- ^ Аллен Л. Чан; Хавьер Фахардо младший; Джеймс Х. Райт, II; Мэтью Эсэй; Винсент Лавалло (2013). «Наблюдение активации B – Cl аниона HCB11Cl11 – при комнатной температуре и выделение стабильного анионного карборанилфосфазида». Неорганическая химия . 52 (21): 12308–12310. DOI : 10.1021 / ic402436w . PMID 24138749 .
- ^ a b Рид Кристофер А (1998). «Карбораны: новый класс слабо координирующих анионов для сильных электрофилов, окислителей и суперкислот». Счета химических исследований . 31 (3): 133–139. DOI : 10.1021 / ar970230r .
- ^ Рамирес-Контрерас Родриго (2012). «Удобное C-алкилирование аниона [HCB11Cl11] -карборана». Dalton Trans . 41 (26): 7842–7844. DOI : 10.1039 / C2DT12431A . PMID 22705934 .
- ^ Кин, Сэм. Исчезающая ложка: и другие правдивые сказки о безумии, любви и истории мира из Периодической таблицы элементов. Нью-Йорк: Back Bay Books, 2011. Печать.
- ^ Лавкин Крис. «Сильный, но нежный, без кислоты». Калифорнийский университет, Риверсайд. (Ноябрь 2004 г.). По состоянию на 13 февраля 2015 г.
- ↑ Стайлз, Д. (1 сентября 2007 г.). «Колонка: Скамья-обезьяна» . Проверено 3 марта 2015 года .
Внешние ссылки [ править ]
- Группа Рид
- Паспорт безопасности материала
