Было предложено разделить эту статью на статьи под названием « Глюкоза» (химия) и « Глюкоза» (биохимия) . ( Обсудить ) ( май 2021 ) |
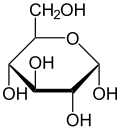 Проекция Хауорта α- d- глюкопиранозы | |
 Фишер проекция из д - глюкозы | |
| Имена | |
|---|---|
| Произношение | / Ɡ л ¯u к oʊ г / , / ɡ л ¯u к oʊ с / |
Название ИЮПАК
| |
| Предпочтительное название IUPAC PIN-коды не используются для натуральных продуктов. | |
Другие названия
| |
| Идентификаторы | |
| |
3D модель ( JSmol ) | |
| 3DMet | |
| Сокращения | Glc |
| 1281604 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| Номер ЕС |
|
| 83256 | |
| КЕГГ | |
| MeSH | Глюкоза |
PubChem CID | |
| Номер RTECS |
|
| UNII |
|
| |
| |
| Характеристики | |
| С 6 Н 12 О 6 | |
| Молярная масса | 180,156 г / моль |
| Появление | белый порошок |
| Плотность | 1,54 г / см 3 |
| Температура плавления | α- d- глюкоза: 146 ° C (295 ° F, 419 K) β- d- глюкоза: 150 ° C (302 ° F, 423 K) |
| 909 г / л (25 ° C (77 ° F)) | |
| −101,5 × 10 −6 см 3 / моль | |
| 8,6827 | |
| Термохимия | |
Теплоемкость ( C ) | 218,6 Дж / (К · моль) [1] |
Стандартная мольная энтропия ( S | 209,2 Дж / (К · моль) [1] |
Std энтальпия формации (Δ F H ⦵ 298 ) | −1271 кДж / моль [2] |
Теплота сгорания, высшее значение (HHV) | 2,805 кДж / моль (670 ккал / моль) |
| Фармакология | |
Код УВД | B05CX01 ( ВОЗ ) V04CA02 ( ВОЗ ), V06DC01 ( ВОЗ ) |
| Опасности | |
| Паспорт безопасности | ICSC 08655 |
| NFPA 704 (огненный алмаз) |  0 1 0 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Глюкоза - это простой сахар с молекулярной формулой C 6 H 12 O 6.. Глюкоза является наиболее распространенным моносахарид , [3] подкатегория углеводов . Глюкоза в основном производится растениями и большинством водорослей во время фотосинтеза из воды и углекислого газа с использованием энергии солнечного света, где она используется для производства целлюлозы в клеточных стенках , которая является наиболее распространенным углеводом. [4] В энергетическом обмене глюкоза является наиболее важным источником энергии для всех организмов . Глюкоза для метаболизма хранится в виде полимера в растениях в основном в виде крахмала и амилопектина., а у животных в виде гликогена . Глюкоза циркулирует в крови животных в виде сахара в крови . В природе форма глюкозы д -глюкозный, а л -глюкозного получают синтетический в сравнительно небольших количествах и имеет меньшее значение. Глюкоза представляет собой моносахарид, содержащий шесть атомов углерода и альдегидную группу, и поэтому является альдогексозой . Молекула глюкозы может существовать в форме с открытой цепью (ациклической), а также в кольцевой (циклической) форме. Глюкоза встречается в природе и в свободном состоянии содержится во фруктах и других частях растений. У животных глюкоза высвобождается в результате распада гликогена в процессе, известном как гликогенолиз .
Глюкоза, как раствор сахара для внутривенного введения , включена в Список основных лекарственных средств Всемирной организации здравоохранения - самые безопасные и эффективные лекарства, необходимые в системе здравоохранения . [5] Он также включен в список в сочетании с хлоридом натрия. [5]
Название глюкоза происходит от французского от греческого γλυκός («глюкос»), что означает «сладкий» в отношении сусла , сладкого первого отжима винограда при производстве вина . [6] [7] Суффикс « -оза » - это химический классификатор, обозначающий сахар.
История [ править ]
Глюкоза была впервые выделена из изюма в 1747 году немецким химиком Андреасом Маргграфом . [8] [9] Глюкоза была обнаружена в винограде Иоганном Тобиасом Ловицем в 1792 году и отличилась от тростникового сахара (сахарозы). Глюкоза - это термин, придуманный Жаном Батистом Дюма в 1838 году, который преобладал в химической литературе. Фридрих Август Кекуле предложил термин декстроза (от латинского dexter = право), потому что в водном растворе глюкозы плоскость линейно поляризованного света повернута вправо. Напротив, d- фруктоза (кетогексоза) и l-глюкоза повернуть линейно поляризованный свет влево. Раннее обозначение вращения плоскости линейно поляризованного света ( d и l- номенклатура) было позже оставлено в пользу d- и l- обозначений, которые относятся к абсолютной конфигурации асимметричного центра, наиболее удаленного от карбонильной группы. , и в соответствии с конфигурацией d- или l- глицеральдегида. [10] [11]
Поскольку глюкоза является основной необходимостью для многих организмов, правильное понимание ее химического состава и структуры во многом способствовало общему прогрессу в области органической химии . Это понимание произошло во многом благодаря исследованиям Эмиля Фишера , немецкого химика, получившего в 1902 году Нобелевскую премию по химии за свои открытия. [12] Синтез глюкозы установил структуру органического материала и, следовательно, стал первым окончательным подтверждением теорий химической кинетики и расположения химических связей в углеродсодержащих молекулах Якоба Хенрикуса ван 'т Гоффа . [13]Между 1891 и 1894 годами Фишер установил стереохимическую конфигурацию всех известных сахаров и правильно предсказал возможные изомеры , применяя теорию асимметричных атомов углерода Ван'т-Гоффа. Названия изначально относились к натуральным веществам. Их энантиомеры получили то же название с введением систематической номенклатуры с учетом абсолютной стереохимии (например, номенклатура Фишера, номенклатура d / l ).
За открытие метаболизма глюкозы Отто Мейерхоф получил Нобелевскую премию по физиологии и медицине в 1922 году. [14] Ганс фон Эйлер-Челпин был удостоен Нобелевской премии по химии вместе с Артуром Харденом в 1929 году за их «исследования ферментации глюкозы». сахар и их доля ферментов в этом процессе ». [15] [16] В 1947 году Бернардо Хусей (за открытие роли гипофиза в метаболизме глюкозы и производных углеводов), а также Карл и Герти Кори (за открытие превращения гликогена из глюкозы в ) получил Нобелевскую премию по физиологии и медицине.[17] [18] [19] В 1970 году Луис Лелуар был удостоен Нобелевской премии по химии за открытие сахарных нуклеотидов, полученных из глюкозы, в биосинтезе углеводов. [20]
Химические свойства [ править ]
Глюкоза образует белые или бесцветные твердые вещества, которые хорошо растворяются в воде и уксусной кислоте, но плохо растворяются в метаноле и этаноле . Они плавятся при 146 ° C (295 ° F) ( α ) и 150 ° C (302 ° F) ( β ) и разлагаются, начиная с 188 ° C (370 ° F), с выделением различных летучих продуктов, в конечном итоге оставляя остаток. из углерода . [21]
С шестью атомами углерода он классифицируется как гексоза , подкатегория моносахаридов. d- Глюкоза является одним из шестнадцати стереоизомеров альдогексозы . Д - изомер , д -глюкозный, также известная как декстроза , широко встречается в природе, но л -изомер, л -глюкозный , не делает. Глюкозу можно получить путем гидролиза углеводов, таких как молочный сахар ( лактоза ), тростниковый сахар ( сахароза ), мальтоза , целлюлоза , гликоген. и т.д. Декстроза обычно коммерчески производится из кукурузного крахмала в США и Японии, из картофельного и пшеничного крахмала в Европе и из крахмала тапиоки в тропических регионах. [22] В производственном процессе используется гидролиз посредством пропаривания под давлением при контролируемом pH в струе с последующей ферментативной деполимеризацией. [23] Несвязанная глюкоза - один из основных ингредиентов меда . Все формы глюкозы бесцветны и легко растворяются в воде, уксусной кислоте и некоторых других растворителях. Они плохо растворяются в метаноле и этаноле .
Структура и номенклатура [ править ]
Глюкоза обычно присутствует в твердой форме в виде моногидрата с замкнутым пирановым кольцом (гидрат декстрозы). В водном растворе, с другой стороны, он имеет открытую цепь в небольшой степени и присутствует преимущественно в виде α- или β- пиранозы , которые взаимно преобразуются (см. Мутаротацию ). Из водных растворов можно кристаллизовать три известные формы: α-глюкопиранозу, β-глюкопиранозу и гидрат β-глюкопиранозы. [24] Глюкоза является строительным блоком дисахаридов лактозы и сахарозы (тростниковый или свекольный сахар), олигосахаридов, таких как рафиноза, и полисахаридов, таких как крахмал иамилопектин , гликоген или целлюлоза . Температура стеклования глюкозы составляет 31 ° C, а постоянная Гордона – Тейлора (экспериментально определенная константа для предсказания температуры стеклования для различных массовых долей смеси двух веществ) [25] составляет 4,5. [26]
| Формы и прогнозы d- глюкозы в сравнении | ||
|---|---|---|
| Натта-проекция | Проекция Хаворта | |
α- d- глюкофураноза | β- d- глюкофураноза | |
α- d- глюкопираноза | β- d- глюкопираноза | |
| α- d- глюкопираноза в (1) Толленс / Фишер (2) проекция Хаворта (3) конформация стула (4) стереохимическая картина | ||
Форма с открытой цепочкой [ править ]
Глюкоза с открытой цепью составляет менее 0,02% молекул глюкозы в водном растворе. Остальное - одна из двух циклических форм полуацеталя. В своей форме с открытой цепью молекула глюкозы имеет открытую (в отличие от циклической ) неразветвленную основную цепь из шести атомов углерода, где C-1 является частью альдегидной группы H (C = O) -. Следовательно, глюкоза также классифицируется как альдоза или альдогексоза . Альдегидная группа превращает глюкозу в редуцирующий сахар, что дает положительную реакцию с тестом Фелинга .
Циклические формы [ править ]
.
Слева направо: Haworth проекции и мяч и пряника структуры альфа- и бета- аномерами из D -glucopyranose (верхний ряд) и D -glucofuranose (нижний ряд)
В растворах форма глюкозы с открытой цепью (« D -» или « L -») существует в равновесии с несколькими циклическими изомерами , каждый из которых содержит углеродное кольцо, замкнутое одним атомом кислорода. Однако в водном растворе более 99% молекул глюкозы существуют в форме пиранозы . Форма с открытой цепью ограничена примерно 0,25%, а формы фуранозы существуют в незначительных количествах. Термины «глюкоза» и « D- глюкоза» обычно также используются для этих циклических форм. Кольцо возникает из формы с открытой цепью в результате реакции внутримолекулярного нуклеофильного присоединения между альдегидной группой (при C-1) и гидроксильной группой C-4 или C-5,образуя полуацеталь связь, -C (OH) H-O-.
Реакция между C-1 и C-5 дает шестичленную гетероциклическую систему, называемую пиранозой, которая представляет собой моносахаридный сахар (отсюда «-оза»), содержащий дериватизированный скелет пирана . Реакция (гораздо реже) между C-1 и C-4 дает пятичленное кольцо фуранозы, названное в честь фурана циклического простого эфира . В любом случае к каждому атому углерода в кольце присоединены один водород и один гидроксил, за исключением последнего атома углерода (C-4 или C-5), где гидроксил заменен остатком открытой молекулы (которая представляет собой - (C ( CH 2 OH) HOH) -H или - (CHOH) -H соответственно).
Реакция замыкания кольца может дать два продукта, обозначенные «α-» и «β-». Когда молекула глюкопиранозы нарисована в проекции Хауорта , обозначение «α-» означает, что гидроксильная группа, присоединенная к C-1, и - Группа CH 2 OH в C-5 находится на противоположных сторонах плоскости кольца ( транс- расположение), в то время как «β-» означает, что они находятся на одной стороне плоскости ( цис- расположение). Следовательно, изомер с открытой цепью D- глюкоза дает четыре различных циклических изомера: α- D- глюкопираноза, β- D- глюкопираноза, α- D- глюкофураноза и β- D-глюкофураноза. Эти пять структур существуют в равновесии и взаимопревращаются, и взаимное превращение происходит намного быстрее при кислотном катализе .
Конформации кресла α- (слева) и β- (справа) D- глюкопиранозы
Другой изомер с открытой цепью L- глюкоза аналогичным образом дает четыре различных циклических формы L- глюкозы, каждая из которых является зеркальным отображением соответствующей D- глюкозы.
Кольцо глюкопиранозы (α или β) может принимать несколько неплоских форм, аналогичных конформациям «стул» и «лодочка» циклогексана . Точно так же кольцо глюкофуранозы может принимать несколько форм, аналогичных «конвертирующим» конформациям циклопентана .
В твердом состоянии наблюдаются только формы глюкопиранозы.
Некоторые производные глюкофуранозы, такие как 1,2- O- изопропилиден- D- глюкофураноза , стабильны и могут быть получены в чистом виде в виде кристаллических твердых веществ. [27] [28] Например, реакция α-D-глюкозы с пара- толилбороновой кислотой H
3С - ( С
6ЧАС
4) - В (ОН)
2восстанавливает нормальное пиранозное кольцо с образованием 4-кратного сложного эфира α-D-глюкофураноза-1,2∶3,5-бис ( п- толилборонат). [29]
Мутаротация [ править ]
Мутаротация состоит из временного обращения вспять реакции образования кольца, приводящего к форме с открытой цепью, с последующим преобразованием кольца. На этапе замыкания кольца может использоваться группа -ОН, отличная от той, которая была воссоздана на этапе раскрытия (таким образом, переключаясь между формами пиранозы и фуранозы), или новая полуацетальная группа, созданная на C-1, может иметь ту же или противоположную направленность, что и исходная. (таким образом переключаясь между формами α и β). Таким образом, хотя форма с открытой цепью практически не обнаруживается в растворе, она является важным компонентом равновесия.
Форма с открытой цепью термодинамически нестабильна и самопроизвольно изомеризуется в циклические формы. (Хотя реакция замыкания кольца теоретически может создать четырех- или трехатомные кольца, они будут сильно напряженными и не наблюдаются на практике.) В растворах при комнатной температуре четыре циклических изомера взаимопревращаются в течение нескольких часов, в процессе, называемом мутаротацией . [30] Начиная с любых пропорций, смесь сходится к стабильному соотношению α: β 36:64. Отношение было бы α: β 11:89, если бы не влияние аномерного эффекта . [31] Мутаротация происходит значительно медленнее при температурах, близких к 0 ° C (32 ° F).
Оптическая активность [ править ]
В воде или в твердой форме d - (+) - глюкоза является правовращающей , что означает, что она будет вращать направление поляризованного света по часовой стрелке, если смотреть на источник света. Эффект обусловлен хиральностью молекул, и действительно, зеркальный изомер, l - (-) - глюкоза, является левовращающим (вращает поляризованный свет против часовой стрелки) на ту же величину. Сила эффекта различна для каждого из пяти таутомеров .
Обратите внимание, что префикс d - не относится напрямую к оптическим свойствам соединения. Это указывает на то, что хиральный центр C-5 имеет такую же направленность, что и d- глицеральдегид (который был назван так, потому что он правовращающий). Тот факт, что d- глюкоза является правовращающей, является комбинированным действием ее четырех хиральных центров, а не только C-5; и действительно, некоторые из других d- альдогексозов являются левовращающими.
Превращение между двумя аномерами можно наблюдать в поляриметре, поскольку чистая α- d- глюкоза имеет удельный угол вращения + 112,2 ° · мл / (дм · г), чистая β- D-глюкоза + 17,5 ° · мл / ( дм · г). [32] Когда равновесие достигается через определенное время из-за мутаротации, угол поворота составляет + 52,7 ° · мл / (дм · г). [32] При добавлении кислоты или основания это превращение значительно ускоряется. Уравновешивание происходит через альдегидную форму с открытой цепью.
Изомеризация [ править ]
В разбавленном гидроксиде натрия или других разбавленных основаниях моносахариды манноза , глюкоза и фруктоза взаимно преобразуются (через преобразование Лобри де Брюна – Альберда – Ван Экенштейна ), так что образуется баланс между этими изомерами. Эта реакция протекает через ендиол :
Биохимические свойства [ править ]
| Метаболизм общих моносахаридов и некоторые биохимические реакции глюкозы. |
|---|
Глюкоза - самый распространенный моносахарид. Глюкоза также является наиболее широко используемой альдогексозой в большинстве живых организмов. Одним из возможных объяснений этого заключается в том, что глюкоза имеет меньшую тенденцию по сравнению с другими альдогексозами , чтобы неспецифический реагировать с аминными группами белков . [33] Эта реакция - гликирование - ухудшает или разрушает функцию многих белков, [33] например, гликированного гемоглобина . Низкая скорость гликирования глюкозы может быть объяснена тем, что она имеет более стабильную циклическую форму по сравнению с другими альдогексозами, что означает, что она тратит меньше времени, чем в ее реактивной форме с открытой цепью . [33]Причина того, что глюкоза имеет наиболее стабильную циклическую форму из всех альдогексоз, заключается в том, что ее гидроксильные группы (за исключением гидроксигруппы на аномерном атоме углерода d- глюкозы) находятся в экваториальном положении . Предположительно, глюкоза является наиболее распространенным природным моносахаридом, поскольку она менее гликирована белками, чем другие моносахариды. [33] [34] Другая гипотеза состоит в том, что глюкоза, будучи единственной D-альдогексозой, которая имеет все пять гидроксизаместителей в экваториальном положении в форме β-D-глюкозы, более доступна для химических реакций, [35] для например, для этерификации[36] илиобразование ацеталя . [37] По этой причине D-глюкоза также является наиболее предпочтительным строительным блоком природных полисахаридов (гликанов). Полисахариды, состоящие исключительно из глюкозы, называются глюканами .
Глюкоза вырабатывается растениями в процессе фотосинтеза с использованием солнечного света, воды и углекислого газа и может использоваться всеми живыми организмами в качестве источника энергии и углерода. Однако большая часть глюкозы встречается не в свободной форме, а в форме ее полимеров, то есть лактозы, сахарозы, крахмала и других веществ, являющихся запасами энергии, а также целлюлозы и хитина , которые являются компонентами клеточной стенки растений или грибов. и членистоногие соответственно. Эти полимеры разлагаются до глюкозы во время приема пищи животными, грибами и бактериями с помощью ферментов. Все животные также могут сами производить глюкозу из определенных предшественников по мере необходимости. Нервные клетки , клетки мозгового вещества иЭритроциты зависят от глюкозы для производства энергии. [38] У взрослых людей содержится около 18 г глюкозы, [39] из которых около 4 г присутствует в крови. [40] Примерно 180–220 г глюкозы вырабатывается в печени взрослого человека за 24 часа. [39]
Многие из долгосрочных осложнений диабета (например, слепота , почечная недостаточность и периферическая невропатия ), вероятно, связаны с гликированием белков или липидов . [41] Напротив, регулируемое ферментами добавление сахара к белку называется гликозилированием и необходимо для функционирования многих белков. [42]
Поглощение [ править ]
Проглоченная глюкоза изначально связывается с рецептором сладкого вкуса на языке человека. Этот комплекс белков T1R2 и T1R3 позволяет идентифицировать источники пищи, содержащие глюкозу. Глюкоза в основном поступает с пищей - около 300 г в день вырабатывается в результате преобразования пищи [43], но она также синтезируется из других метаболитов в клетках организма. У человека расщепление глюкозосодержащих полисахаридов частично происходит уже во время жевания с помощью амилазы , содержащейся в слюне , а также мальтазы , лактазы и сахарозы на краю кисти.тонкой кишки. Глюкоза является строительным материалом для многих углеводов и может быть отделена от них с помощью определенных ферментов. Глюкозидазы , подгруппа гликозидаз, сначала катализируют гидролиз длинноцепочечных глюкозосодержащих полисахаридов, удаляя концевую глюкозу. В свою очередь, дисахариды в основном разлагаются специфическими гликозидазами до глюкозы. Названия разрушающих ферментов часто происходят от конкретных поли- и дисахаридов; среди прочего, для разложения полисахаридных цепей используются амилазы (названные в честь амилозы, компонента крахмала), целлюлазы (названные в честь целлюлозы), хитиназы (названные в честь хитина) и другие. Кроме того, для расщепления дисахаридов используются мальтаза, лактаза, сахароза, трегалаза.и другие. У человека известно около 70 генов, кодирующих гликозидазы. Они выполняют функции переваривания и разложения гликогена, сфинголипидов , мукополисахаридов и поли (АДФ-рибозы) . Люди не производят целлюлазы, хитиназы и треалазы, в отличие от бактерий кишечной флоры .
Чтобы попасть внутрь или выйти из клеточных мембран клеток и мембран клеточных компартментов, глюкоза требует специальных транспортных белков из суперсемейства основных фасилитаторов . В тонком кишечнике (точнее, в тощей кишке ) [44] глюкоза поглощается эпителиальными клетками кишечника с помощью переносчиков глюкозы [45] через вторичный активный транспортный механизм, называемый симпортом ионов натрия и глюкозы через натрий / глюкозу. Котранспортер глюкозы 1 . [46] Дальнейший перенос происходит на базолатеральномчасть кишечных эпителиальных клеток через переносчик глюкозы GLUT2 , [46], а также их захват клетками печени , почечными клетками , клетками островков Лангерганса , нервными клетками, астроцитами и таницитами . [47] Глюкоза поступает в печень через портальную вену и хранится там в виде клеточного гликогена. [48] В клетке печени, она фосфорилируется с помощью глюкокиназы в положении 6 к глюкозо-6-фосфат , который не может покинуть клетку. С помощью глюкозо-6-фосфатазыглюкозо-6-фосфат при необходимости превращается обратно в глюкозу исключительно в печени, так что он доступен для поддержания достаточной концентрации глюкозы в крови. В других клетках захват происходит путем пассивного транспорта через один из 14 белков GLUT. [46] В других типах клеток фосфорилирование происходит через гексокиназу , после чего глюкоза больше не может диффундировать из клетки.
Переносчик глюкозы GLUT1 продуцируется большинством типов клеток и имеет особое значение для нервных клеток и β-клеток поджелудочной железы . [46] GLUT3 высоко экспрессируется в нервных клетках. [46] Глюкоза из кровотока поглощается GLUT4 из мышечных клеток ( скелетной мышцы [49] и сердечной мышцы ) и жировых клеток . [50] GLUT14 образуется исключительно в семенниках . [46] Избыточная глюкоза расщепляется и превращается в жирные кислоты, которые хранятся в виде триацилглицеридов . впочками глюкоза в моче абсорбируется через SGLT1 и SGLT2 в апикальных клеточных мембранах и передается через GLUT2 в базолатеральных клеточных мембранах. [51] Около 90% реабсорбции глюкозы почками происходит через SGLT2 и около 3% через SGLT1. [52]
Биосинтез [ править ]
У растений и некоторых прокариот глюкоза является продуктом фотосинтеза . [53] Глюкоза также образуется при расщеплении полимерных форм глюкозы, таких как гликоген (у животных и грибов ) или крахмал (у растений). Расщепление гликогена называется гликогенолизом , расщепление крахмала называется деградацией крахмала. [54]
Метаболический путь, который начинается с молекул, содержащих от двух до четырех атомов углерода (C), и заканчивается молекулой глюкозы, содержащей шесть атомов углерода, называется глюконеогенезом и происходит во всех живых организмах. Меньшие исходные материалы являются результатом других метаболических путей. В конечном итоге почти все биомолекулы образуются в результате ассимиляции углекислого газа растениями во время фотосинтеза. [55] Свободная энергия образования α- d- глюкозы составляет 917,2 килоджоулей на моль. [56] У людей глюконеогенез происходит в печени и почках, [57] но также и в других типах клеток. В печени хранится около 150 г гликогена, в скелетных мышцах - около 250 г. [58]Однако глюкоза, высвобождаемая в мышечных клетках при расщеплении гликогена, не может быть доставлена в кровоток, потому что глюкоза фосфорилируется гексокиназой, а глюкозо-6-фосфатаза не экспрессируется для удаления фосфатной группы. В отличие от глюкозы, для глюкозо-6-фосфата нет транспортного белка. Глюконеогенез позволяет организму накапливать глюкозу из других метаболитов, включая лактат или определенные аминокислоты, при этом потребляя энергию. Клетки почечных канальцев также могут производить глюкозу.
Разложение глюкозы [ править ]
Глюкозосодержащие соединения и изомерные формы перевариваются и усваиваются организмом в кишечнике, включая крахмал , гликоген , дисахариды и моносахариды .
Глюкоза хранится в основном в печени и мышцах в виде гликогена. Он распределяется и используется в тканях в виде свободной глюкозы.
У человека глюкоза метаболизируется путем гликолиза [59] и пентозофосфатного пути. [60] Гликолиз используется всеми живыми организмами, [61] [62] с небольшими вариациями, и все организмы вырабатывают энергию за счет распада моносахаридов. [61] В ходе дальнейшего метаболизма он может полностью разрушиться посредством окислительного декарбоксилирования , цикла Кребса (синоним цикла лимонной кислоты ) и дыхательной цепи.к воде и двуокиси углерода. Если для этого недостаточно кислорода, разложение глюкозы у животных происходит анаэробно до лактата посредством ферментации молочной кислоты и высвобождает меньше энергии. Мышечный лактат попадает в печень через кровоток у млекопитающих, где происходит глюконеогенез ( цикл Кори ). При большом количестве глюкозы метаболит ацетил-КоА из цикла Кребса также можно использовать для синтеза жирных кислот . [63] Глюкоза также используется для пополнения запасов гликогена в организме, которые в основном находятся в печени и скелетных мышцах. Эти процессы регулируются гормонально .
В других живых организмах могут происходить другие формы ферментации. Бактерия Escherichia coli может расти на питательных средах, содержащих глюкозу в качестве единственного источника углерода. [56] У некоторых бактерий и в модифицированной форме также у архей глюкоза разлагается по пути Энтнера-Дудорова . [64]
Использование глюкозы в качестве источника энергии в клетках осуществляется либо путем аэробного дыхания, либо анаэробного дыхания, либо путем ферментации. Первым этапом гликолиза является фосфорилирование глюкозы гексокиназой с образованием глюкозо-6-фосфата . Основная причина немедленного фосфорилирования глюкозы состоит в том, чтобы предотвратить ее диффузию из клетки, поскольку заряженная фосфатная группа препятствует легкому проникновению глюкозо-6-фосфата через клеточную мембрану . [65] Кроме того, добавление высокоэнергетической фосфатной группы активирует глюкозу для последующего разложения на более поздних стадиях гликолиза. В физиологических условиях эта начальная реакция необратима.
При анаэробном дыхании одна молекула глюкозы дает чистый прирост в две молекулы АТФ (четыре молекулы АТФ производятся во время гликолиза посредством фосфорилирования на уровне субстрата, но две необходимы ферментам, используемым во время процесса). [66] При аэробном дыхании молекула глюкозы намного более прибыльна, поскольку генерируется максимальное чистое производство 30 или 32 молекул АТФ (в зависимости от организма) посредством окислительного фосфорилирования. [67]
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи. [§ 1]
- ^ Интерактивную карту путей можно отредактировать на WikiPathways: " GlycolysisGluconeogenesis_WP534 " .
Опухолевые клетки часто растут сравнительно быстро и потребляют за счет гликолиза количество глюкозы выше среднего [68], что приводит к образованию лактата, конечного продукта ферментации у млекопитающих, даже в присутствии кислорода. Этот эффект называется эффектом Варбурга . Для увеличения поглощения глюкозы опухолями чрезмерно вырабатываются различные SGLT и GLUT. [69] [70]
В дрожжах этанол ферментируется при высоких концентрациях глюкозы даже в присутствии кислорода (который обычно приводит к дыханию, но не к брожению). Этот эффект называется эффектом Крэбтри .
Источник энергии [ править ]
Глюкоза - повсеместное топливо в биологии . Он используется в качестве источника энергии в организмах, от бактерий до людей, посредством аэробного дыхания , анаэробного дыхания (у бактерий) или ферментации . Глюкоза является ключевым источником энергии для человеческого организма, благодаря аэробному дыханию, обеспечивая около 3,75 килокалорий (16 килоджоулей ) пищевой энергии на грамм. [71] При расщеплении углеводов (например, крахмала) образуются моно- и дисахариды , большинство из которых представляет собой глюкозу. Посредством гликолиза, а затем в реакциях цикла лимонной кислоты иПри окислительном фосфорилировании глюкоза окисляется с образованием углекислого газа и воды , выделяя энергию в основном в форме АТФ . Реакция на инсулин и другие механизмы регулируют концентрацию глюкозы в крови. Физиологическая калорийность глюкозы, в зависимости от источника, составляет 16,2 килоджоулей на грамм [72] и 15,7 кДж / г (3,74 ккал / г) соответственно. [73]Высокая доступность углеводов из растительной биомассы привела к появлению множества методов в ходе эволюции, особенно у микроорганизмов, для использования энергии и запаса углерода глюкозы. Существуют различия в том, что конечный продукт больше не может использоваться для производства энергии. Присутствие отдельных генов и их генных продуктов, ферментов, определяет возможные реакции. Метаболический путь гликолиза используется почти всеми живыми существами. Существенным различием в использовании гликолиза является восстановление НАДФН в качестве восстановителя анаболизма , который в противном случае должен был бы генерироваться косвенно. [74]
Глюкоза и снабжение кислородом почти вся энергия для мозга , [75] поэтому его наличие влияния психологических процессов. Когда уровень глюкозы низкий , психологические процессы, требующие умственных усилий (например, самоконтроль , принятие решений), нарушаются. [76] [77] [78] [79] В головном мозге, который зависит от глюкозы и кислорода как основного источника энергии, концентрация глюкозы обычно составляет от 4 до 6 мМ (5 мМ равно 90 мг / дл), [ 39], но снижается до 2–3 мМ при голодании. [80] Путаница возникает ниже 1 мМ и кома - на более низких уровнях. [80]
Уровень глюкозы в крови называется сахаром в крови . Уровень сахара в крови регулируется связывающими глюкозу нервными клетками гипоталамуса . [81] Кроме того, глюкоза в головном мозге связывается с рецепторами глюкозы системы вознаграждения в прилежащем ядре . [81] Связывание глюкозы с рецептором сладкого на языке вызывает высвобождение различных гормонов энергетического метаболизма либо через глюкозу, либо через другие сахара, что приводит к увеличению клеточного поглощения и снижению уровня сахара в крови. [82] Искусственные подсластители не снижают уровень сахара в крови. [82]
Содержание сахара в крови здорового человека в состоянии кратковременного голодания, например, после ночного голодания, составляет примерно от 70 до 100 мг / дл крови (от 4 до 5,5 мМ). В плазме крови измеренные значения примерно на 10–15% выше. Кроме того, значения в артериальной крови выше, чем концентрации в венозной крови, поскольку глюкоза всасывается в ткань во время прохождения капиллярного русла . Также в капиллярной крови, которая часто используется для определения сахара в крови, значения иногда выше, чем в венозной крови. Содержание глюкозы в крови регулируется гормонами инсулином , инкретином и глюкагоном . [81][83] Инсулин снижает уровень глюкозы, глюкагон повышает его. [39] Кроме того, гормоны адреналин , тироксин , глюкокортикоиды , соматотропин и адренокортикотропин приводят к повышению уровня глюкозы. [39] Существует также гормонально-независимая регуляция, называемая ауторегуляцией глюкозы . [84] После приема пищи концентрация сахара в крови увеличивается. Значения более 180 мг / дл в венозной цельной крови являются патологическими и называются гипергликемией , значения ниже 40 мг / дл называются гипогликемией . [85]При необходимости глюкоза высвобождается в кровоток глюкозо-6-фосфатазой из глюкозо-6-фосфата, происходящего из гликогена печени и почек, тем самым регулируя гомеостаз концентрации глюкозы в крови. [57] [38] У жвачных животных концентрация глюкозы в крови ниже (60 мг / дл у крупного рогатого скота и 40 мг / дл у овец ), потому что углеводы больше преобразуются кишечной флорой в короткоцепочечные жирные кислоты . [86]
Некоторые глюкоза превращается в молочную кислоту с помощью астроцитов , которые затем используют в качестве источника энергии с помощью клеток головного мозга ; некоторая часть глюкозы используется клетками кишечника и эритроцитами , а остальная часть достигает печени , жировой ткани и мышечных клеток, где она абсорбируется и сохраняется в виде гликогена (под действием инсулина ). Гликоген клеток печени может превращаться в глюкозу и возвращаться в кровь при низком уровне инсулина или его отсутствии; Гликоген мышечных клеток не возвращается в кровь из-за недостатка ферментов. В жировых клетках глюкоза используется для активации реакций, которые синтезируют некоторое количество жира.типы и имеют другие цели. Гликоген - это механизм «хранения энергии глюкозы» в организме, потому что он гораздо более «экономичен» и менее реактивен, чем сама глюкоза.
В результате своей важности для здоровья человека глюкоза является аналитом в тестах на глюкозу, которые являются обычными медицинскими анализами крови . [87] Прием пищи или голодание до взятия пробы крови влияет на анализ глюкозы в крови; высокий уровень сахара в крови натощак может быть признаком преддиабета или сахарного диабета . [88]
Гликемический индекс является показателем скорости резорбции и преобразования в уровень глюкозы в крови из углеводов глотавших, измеренная как площадь под кривой уровня глюкозы в крови после потребления по сравнению с глюкозой (глюкоза определяется как 100). [89] Клиническая важность гликемического индекса является спорной [89] [90], поскольку продукты с высоким содержанием жира замедляют резорбцию углеводов и снижают гликемический индекс, например, мороженое. [90] Альтернативный показатель является индекс инсулина , [91] измеряется как воздействие углеводов потребления на уровне инсулина в крови. Гликемический индекс является показателем количества глюкозы, добавленной к уровню глюкозы в крови после потребления, на основе гликемического индекса и количества потребляемой пищи.
Предшественник [ править ]
Организмы используют глюкозу в качестве прекурсора для синтеза нескольких важных веществ. Крахмал , целлюлоза и гликоген («животный крахмал») являются обычными полимерами глюкозы ( полисахаридами ). Некоторые из этих полимеров (крахмал или гликоген) служат в качестве накопителей энергии, в то время как другие (целлюлоза и хитин , производные глюкозы) играют структурную роль. Олигосахариды глюкозы в сочетании с другими сахарами служат важными запасами энергии. К ним относятся лактоза , преобладающий сахар в молоке, который представляет собой дисахарид глюкоза-галактоза, и сахарозу , другой дисахарид, который состоит из глюкозы ифруктоза . Глюкоза также добавляется к определенным белкам и липидам в процессе, называемом гликозилированием . Это часто имеет решающее значение для их функционирования. Ферменты, которые соединяют глюкозу с другими молекулами, обычно используют фосфорилированную глюкозу для формирования новой связи, связывая ее с разрывом глюкозо-фосфатной связи.
Помимо прямого использования в качестве мономера, глюкоза может быть расщеплена для синтеза большого количества других биомолекул. Это важно, поскольку глюкоза служит одновременно и основным хранилищем энергии, и источником органического углерода. Глюкоза может расщепляться и превращаться в липиды . Он также является предшественником синтеза других важных молекул, таких как витамин С ( аскорбиновая кислота ). В живых организмах глюкоза превращается в несколько других химических соединений, которые являются исходным материалом для различных метаболических путей . Среди них все другие моносахариды [92], такие как фруктоза (через путь полиола ), [46]манноза (эпимер глюкозы в положении 2), галактоза (эпимер в положении 4), фукоза, различные уроновые кислоты и аминосахара производятся из глюкозы. [48] В дополнение к фосфорилированию до глюкозо-6-фосфата, которое является частью гликолиза, глюкоза может окисляться во время разложения до глюконо-1,5-лактона . Глюкоза используется некоторыми бактериями как строительный блок в биосинтезе трегалозы или декстрана, а у животных как строительный блок гликогена. Глюкоза также может превращаться из бактериальной ксилозоизомеразы во фруктозу. Кроме того, метаболиты глюкозы производят все заменимые аминокислоты., Сахарные спирты , такие как маннит и сорбит , жирных кислот , холестерина и нуклеиновых кислот . [92] Наконец, глюкоза используется в качестве строительного блока при гликозилировании белков до гликопротеинов , гликолипидов , пептидогликанов , гликозидов и других веществ (катализируемых гликозилтрансферазами ) и может отщепляться от них гликозидазами .
Патология [ править ]
Диабет [ править ]
Диабет - это нарушение обмена веществ, при котором организм не может регулировать уровень глюкозы в крови либо из-за нехватки инсулина в организме, либо из-за неспособности клеток организма должным образом реагировать на инсулин. Каждая из этих ситуаций может быть вызвана постоянно высоким повышением уровня глюкозы в крови, выгоранием поджелудочной железы и инсулинорезистентностью . Поджелудочная железа является органом , ответственным за секрецию инсулина и глюкагона гормонов. [93] Инсулин - это гормон, который регулирует уровень глюкозы, позволяя клеткам организма поглощать и использовать глюкозу. Без него глюкоза не может попасть в клетку и, следовательно, не может использоваться в качестве топлива для функций организма. [94]Если поджелудочная железа постоянно подвергается повышенному уровню глюкозы в крови, вырабатывающие инсулин клетки поджелудочной железы могут быть повреждены, что приведет к нехватке инсулина в организме. Инсулинорезистентность возникает, когда поджелудочная железа пытается производить все больше и больше инсулина в ответ на постоянно повышенный уровень глюкозы в крови. В конце концов, остальная часть тела становится устойчивой к инсулину, который вырабатывает поджелудочная железа, тем самым требуя больше инсулина для достижения того же эффекта снижения уровня глюкозы в крови и заставляя поджелудочную железу производить еще больше инсулина, чтобы конкурировать с резистентностью. Эта негативная спираль способствует выгоранию поджелудочной железы и прогрессированию диабета.
Чтобы контролировать реакцию организма на терапию, снижающую уровень глюкозы в крови, можно измерить уровень глюкозы. Мониторинг уровня глюкозы в крови может выполняться несколькими методами, такими как тест на глюкозу натощак, который измеряет уровень глюкозы в крови после 8 часов голодания. Другой тест - это двухчасовой тест на толерантность к глюкозе (GTT) - для этого теста человеку делают тест на глюкозу натощак, затем он выпивает 75-граммовый напиток с глюкозой и повторно тестируется. Этот тест измеряет способность организма человека перерабатывать глюкозу. Со временем уровень глюкозы в крови должен снизиться, поскольку инсулин позволяет ему поглощаться клетками и выходить из кровотока.
Управление гипогликемией [ править ]
Люди с диабетом или другими состояниями, которые приводят к низкому уровню сахара в крови, часто переносят небольшое количество сахара в различных формах. Одним из обычно используемых сахаров является глюкоза, часто в форме таблеток глюкозы (глюкоза спрессована в форму таблетки, иногда с одним или несколькими другими ингредиентами в качестве связующего), карамель или сахарный пакет .
Источники [ править ]
Большинство пищевых углеводов содержат глюкозу либо в качестве единственного строительного материала (как полисахариды, крахмал и гликоген ), либо вместе с другим моносахаридом (как в гетерополисахаридах сахароза и лактоза ). [95] Неограниченная глюкоза - один из основных ингредиентов меда .
| Питание пункт | Углеводы, всего, A, включая пищевые волокна | Всего сахаров | Свободная фруктоза | Свободная глюкоза | Сахароза | Соотношение фруктоза / глюкоза | Сахароза как доля от общего количества сахаров (%) |
|---|---|---|---|---|---|---|---|
| Фрукты | |||||||
| яблоко | 13,8 | 10,4 | 5.9 | 2,4 | 2.1 | 2.0 | 19,9 |
| Абрикос | 11.1 | 9.2 | 0,9 | 2,4 | 5.9 | 0,7 | 63,5 |
| Банан | 22,8 | 12,2 | 4.9 | 5.0 | 2,4 | 1.0 | 20,0 |
| Инжир сушеный | 63,9 | 47,9 | 22,9 | 24,8 | 0,9 | 0,93 | 0,15 |
| Виноград | 18,1 | 15.5 | 8.1 | 7.2 | 0,2 | 1.1 | 1 |
| Пупок оранжевый | 12,5 | 8,5 | 2,25 | 2.0 | 4.3 | 1.1 | 50,4 |
| Персик | 9,5 | 8,4 | 1.5 | 2.0 | 4.8 | 0,9 | 56,7 |
| Груша | 15.5 | 9,8 | 6.2 | 2,8 | 0,8 | 2.1 | 8.0 |
| Ананас | 13,1 | 9.9 | 2.1 | 1,7 | 6.0 | 1.1 | 60,8 |
| слива | 11,4 | 9.9 | 3.1 | 5.1 | 1.6 | 0,66 | 16,2 |
| Овощи | |||||||
| Свекла красная | 9,6 | 6,8 | 0,1 | 0,1 | 6.5 | 1.0 | 96,2 |
| Морковь | 9,6 | 4,7 | 0,6 | 0,6 | 3,6 | 1.0 | 77 |
| Красный перец сладкий | 6.0 | 4.2 | 2.3 | 1.9 | 0,0 | 1.2 | 0,0 |
| Лук сладкий | 7,6 | 5.0 | 2.0 | 2.3 | 0,7 | 0,9 | 14,3 |
| Сладкий картофель | 20,1 | 4.2 | 0,7 | 1.0 | 2,5 | 0,9 | 60,3 |
| сладкий картофель | 27,9 | 0,5 | Следы | Следы | Следы | N / A | Следы |
| Карамельная тросточка | 13–18 | 0,2–1,0 | 0,2–1,0 | 11–16 | 1.0 | высокая | |
| Сахарная свекла | 17–18 | 0,1–0,5 | 0,1–0,5 | 16–17 | 1.0 | высокая | |
| Зерна | |||||||
| Кукуруза сладкая | 19.0 | 6.2 | 1.9 | 3,4 | 0,9 | 0,61 | 15.0 |
^ A Ценность углеводов рассчитывается в базе данных USDA и не всегда соответствует сумме сахаров, крахмала и «пищевых волокон».
Коммерческое производство [ править ]
В промышленности глюкозу получают из крахмала путем ферментативного гидролиза с использованием глюкозоамилазы или кислот . Ферментативный гидролиз в значительной степени вытеснил гидролиз, катализируемый кислотой. [97] Результатом является глюкозный сироп (ферментативно содержащий более 90% глюкозы в сухом веществе) [97] с годовым объемом производства в мире 20 миллионов тонн (по состоянию на 2011 год). [98] Это причина бывшего общего названия «крахмальный сахар». Чаще всего амилазы происходят от Bacillus licheniformis [99] или Bacillus subtilis (штамм MN-385), [99]которые более термостабильны, чем изначально используемые ферменты. [99] [100] Начиная с 1982 года пуллуланазы из Aspergillus niger использовались в производстве сиропа глюкозы для преобразования амилопектина в крахмал (амилозу), тем самым увеличивая выход глюкозы. [101] Реакция проводится при pH = 4,6–5,2 и температуре 55–60 ° C. [8] Кукурузный сироп содержит от 20% до 95% глюкозы в сухом веществе. [102] [103] Японская форма глюкозного сиропа, Мидзуаме , производится из сладкого картофеля или рисового крахмала. [104] Мальтодекстрин содержит около 20% глюкозы.
В качестве источника крахмала можно использовать многие культуры. Кукуруза , [97] рис, [97] пшеница , [97] маниока , [97] картофель , [97] ячмень , [97] сладкий картофель, [105] кукурузная шелуха и саго используются в различных частях мира. В Соединенных Штатах , кукурузный крахмал (из кукурузы) используются почти исключительно. Некоторая коммерческая глюкоза входит в состав инвертного сахара , смеси глюкозы и фруктозы примерно 1: 1.который производится из сахарозы. В принципе, целлюлозу можно гидролизовать до глюкозы, но этот процесс еще не является коммерчески практичным. [24]
Превращение во фруктозу [ править ]
В США почти исключительно кукуруза (точнее: кукурузный сироп) используется в качестве источника глюкозы для производства изоглюкозы , которая представляет собой смесь глюкозы и фруктозы, поскольку фруктоза обладает более высокой подслащивающей способностью - с такой же физиологической теплотворной способностью 374 килокалорий на единицу. 100 г. Ежегодное мировое производство изоглюкозы составляет 8 миллионов тонн (по состоянию на 2011 год). [98] При изготовлении из кукурузного сиропа конечным продуктом является кукурузный сироп с высоким содержанием фруктозы (HFCS).
Коммерческое использование [ править ]
Глюкоза в основном используется для производства фруктозы и продуктов, содержащих глюкозу. В пищевых продуктах он используется в качестве подсластителя , увлажнителя , для увеличения объема и создания более мягкого ощущения во рту . [97] Различные источники глюкозы, такие как виноградный сок (для вина) или солод (для пива), используются для ферментации до этанола при производстве алкогольных напитков . В большинстве безалкогольных напитков в США используется HFCS-55 (с содержанием фруктозы 55% в сухой массе), в то время как в большинстве других подслащенных HFCS пищевых продуктов в США используется HFCS-42 (с содержанием фруктозы 42% в сухой массе). ). [107]В соседней стране Мексика, с другой стороны, тростниковый сахар используется в безалкогольных напитках в качестве подсластителя, который имеет более высокую подслащивающую способность. [108] Кроме того, сироп глюкозы используется, среди прочего, в производстве кондитерских изделий, таких как конфеты , ирис и помадка . [109] Типичными химическими реакциями глюкозы при нагревании в безводных условиях являются карамелизация и, в присутствии аминокислот, реакция Майяра .
Кроме того, различные органические кислоты могут быть получены биотехнологическим путем из глюкозы, например, путем ферментации с Clostridium thermoaceticum для получения уксусной кислоты , с Penicilium notatum для производства арабоаскорбиновой кислоты , с Rhizopus delemar для производства фумаровой кислоты , с Aspergillus niger для производство глюконовой кислоты , Candida brumptii для производства изоазимной кислоты , Aspergillus terreus для производства итаконовой кислоты , Pseudomonas fluorescensдля производства 2-кетоглюконовой кислоты , с Gluconobacter suboxydans для производства 5-кетоглюконовой кислоты , с Aspergillus oryzae для производства койевой кислоты , с Lactobacillus delbrueckii для производства молочной кислоты , с Lactobacillus brevis для производства яблочной кислоты , с Propionibacter shermanii для производства пропионовой кислоты , с Pseudomonas aeruginosa для производства пировиноградной кислоты и с Gluconobacter suboxydansдля производства винной кислоты . [110] О мощных, биоактивных природных продуктах, таких как триптолид, которые ингибируют транскрипцию млекопитающих посредством ингибирования субъединицы XPB общего фактора транскрипции TFIIH, недавно сообщалось в качестве конъюгата глюкозы для воздействия на гипоксические раковые клетки с повышенной экспрессией переносчика глюкозы. [111]
Анализ [ править ]
В частности, когда молекула глюкозы , чтобы обнаружить в определенном положении в более крупной молекулы, спектроскопия ядерного магнитного резонанса , рентгеновской кристаллографии анализа или лектин иммунным осуществляется с конканавалин А конъюгата фермент - репортер (который связывается только глюкозу или манноза).
Классические качественные реакции обнаружения [ править ]
Эти реакции имеют только историческое значение:
Тест Фелинга [ править ]
Тест Фелинга - классический метод обнаружения альдоз. [112] Из-за мутаротации глюкоза всегда присутствует в небольшом количестве в виде альдегида с открытой цепью. При добавлении реагентов Фелинга (раствор Фелинга (I) и раствор Фелинга (II)) альдегидная группа окисляется до карбоновой кислоты , а тартратный комплекс Cu 2+ восстанавливается до Cu + и образует осадок кирпично-красного цвета (Cu 2 О).
Тест Толленса [ править ]
В тесте Толленса после добавления аммиачного AgNO 3 к раствору образца Ag + восстанавливается глюкозой до элементарного серебра . [113]
Barfoed test [ править ]
В тесте Barfoed в , [114] раствор растворенного ацетата меди , ацетата натрия и уксусной кислоты добавляют к раствору сахара , чтобы быть проверены , а затем нагревают на водяной бане в течение нескольких минут. Глюкоза и другие моносахариды быстро образуют красноватый цвет и красновато-коричневый оксид меди (I) (Cu 2 O).
Тест Нюландера [ править ]
В тесте Ниландера глюкоза реагирует как редуцирующий сахар . [115]
Другие тесты [ править ]
При нагревании разбавленного раствора гидроксида калия с глюкозой до 100 ° C появляется сильное красноватое потемнение и карамельный запах. [116] Концентрированная серная кислота растворяет сухую глюкозу без почернения при комнатной температуре с образованием сахарной серной кислоты. [116] В дрожжевом растворе при спиртовой ферментации образуется углекислый газ в соотношении 2,0454 молекулы глюкозы на одну молекулу CO 2 . [116] Глюкоза образует черную массу с хлоридом олова . [116] В аммиачном растворе серебра глюкоза (а также лактоза и декстрин) приводит к отложению серебра. В аммиачном ацетате свинцаВ растворе белый гликозид свинца образуется в присутствии глюкозы, которая становится менее растворимой при приготовлении пищи и становится коричневой. [116] В аммиачном растворе меди желтый гидрат оксида меди образуется с глюкозой при комнатной температуре, а красный оксид меди образуется во время кипячения (то же самое с декстрином, за исключением аммиачного раствора ацетата меди ). [116] С реактивом Хагера глюкоза образует оксид ртути во время кипячения. [116] Щелочной раствор висмута используется для осаждения элементарного черно-коричневого висмута с глюкозой. [116] Глюкоза, сваренная враствор молибдата аммония окрашивает раствор в синий цвет. Раствор с индигокармином и карбонатом натрия разрушается при кипячении с глюкозой. [116]
Инструментальная количественная оценка [ править ]
Рефрактометрия и поляриметрия [ править ]
В концентрированных растворах глюкозы с низким содержанием других углеводов ее концентрацию можно определить с помощью поляриметра. Концентрацию сахарных смесей можно определять с помощью рефрактометра , например, при определении Oechsle в процессе производства вина.
Фотометрические ферментативные методы в растворе [ править ]
Фермент глюкозооксидаза (GOx) превращает глюкозу в глюконовую кислоту и перекись водорода, потребляя кислород. Другой фермент, пероксидаза, катализирует хромогенную реакцию (реакция Триндера) [117] из фенола с 4-аминоантипирином к фиолетовому красителю.
Фотометрический метод тест-полосок [ править ]
В методе тест-полосок используется упомянутое выше ферментативное превращение глюкозы в глюконовую кислоту с образованием перекиси водорода. Реагенты иммобилизованы на полимерной матрице, так называемой тест-полоске, которая приобретает более или менее интенсивный цвет. Это можно измерить рефлектометрическим методом на длине волны 510 нм с помощью портативного фотометра на основе светодиода. Это позволяет обычным людям определять уровень сахара в крови. В дополнение к реакции фенола с 4-аминоантипирином были разработаны новые хромогенные реакции, которые позволяют проводить фотометрию на более высоких длинах волн (550 нм, 750 нм). [118]
Амперометрический датчик глюкозы [ править ]
Электроанализ глюкозы также основан на ферментативной реакции, упомянутой выше. Полученный пероксид водорода может быть количественно определен амперометрическим методом анодным окислением при потенциале 600 мВ. [119] GOx иммобилизован на поверхности электрода или в мембране, расположенной рядом с электродом. В электродах используются драгоценные металлы, такие как платина или золото, а также электроды из углеродных нанотрубок, которые, например, легированы бором. [120] Нанопроволоки Cu – CuO также используются в качестве безферментных амперометрических электродов. Таким образом достигается предел обнаружения 50 мкмоль / л. [121]Особенно многообещающим методом является так называемая «ферментная разводка». В этом случае электрон, протекающий во время окисления, передается непосредственно от фермента через молекулярную проволоку к электроду. [122]
Другие сенсорные методы [ править ]
Существует множество других химических датчиков для измерения глюкозы. [123] [124] Учитывая важность анализа глюкозы в науках о жизни, были разработаны многочисленные оптические датчики для сахаридов на основе использования бороновых кислот, [125]которые особенно полезны для внутриклеточных сенсорных приложений, где другие (оптические) методы не подходят или могут использоваться только при определенных условиях. В дополнение к производным органической бороновой кислоты, которые часто очень специфично связываются с 1,2-диольными группами сахаров, существуют также другие концепции зондов, классифицированные по функциональным механизмам, которые используют селективные связывающие глюкозу белки (например, конканавалин A) в качестве рецептора. . Кроме того, были разработаны методы, которые косвенно определяют концентрацию глюкозы по концентрации продуктов метаболизма, например, по потреблению кислорода с помощью флуоресцентно-оптических датчиков. [126] Наконец, существуют концепции, основанные на ферментах, которые используют собственное поглощение или флуоресценцию (меченных флуоресценцией) ферментов в качестве репортеров. [123]
Йодометрия меди [ править ]
Глюкозу можно определить количественно с помощью йодометрии меди. [127]
Хроматографические методы [ править ]
В частности, для анализа сложных смесей, содержащих глюкозу, например, в меде, часто используются хроматографические методы, такие как высокоэффективная жидкостная хроматография и газовая хроматография [127] в сочетании с масс-спектрометрией . [128] [129] Принимая во внимание соотношение изотопов, с помощью этих методов также можно надежно обнаружить фальсификацию меда добавленными сахарами. [130] Обычно используется дериватизация с использованием силилирующих реагентов. [131] Также можно количественно определить пропорции ди- и трисахаридов.
Анализ in vivo [ править ]
Поглощение глюкозы клетками организмов измеряется с помощью 2-дезокси-D-глюкозы или фтордезоксиглюкозы . [80] ( 18 F) фтордезоксиглюкоза используется в качестве индикатора в позитронно-эмиссионной томографии в онкологии и неврологии [132], где она является наиболее часто используемым диагностическим агентом. [133]
Ссылки [ править ]
- ^ Б Boerio-козлов, Йулиана (1991), «измерения теплоемкости и термодинамические функции кристаллического a-D-глюкозы при температурах от 10К до 340K», J. Chem. Термодинамика. , 23 (5): 403-09, DOI : 10.1016 / S0021-9614 (05) 80128-4
- ^ Пономарев, В.В.; Мигарская Л.Б. Теплоты сгорания некоторых аминокислот // Успехи химии . J. Phys. Chem. (Англ. Пер.) , 34 : 1182–83.
- ^ Domb, Abraham J .; Кост, Иосиф; Уайзман, Дэвид (1998-02-04). Справочник биоразлагаемых полимеров . п. 275. ISBN 978-1-4200-4936-7.
- ^ Kamide, Кэндзи (2005). Целлюлоза и производные целлюлозы: молекулярная характеристика и ее применения (1-е изд.). Амстердам: Эльзевир. п. 1. ISBN 9780080454443. Дата обращения 13 мая 2021 .
- ^ a b Всемирная организация здравоохранения (2019). Примерный перечень Всемирной организации здравоохранения основных лекарственных средств: список двадцать первых 2019 . Женева: Всемирная организация здравоохранения. ЛВП : 10665/325771 . WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ "Интернет-словарь этимологии" . Etymonline.com . Архивировано 26 ноября 2016 года . Проверено 25 ноября 2016 .
- ^ Тенар, Гей-Люссак, Байот и Дюма (1838) "Раппорт сюр ип mémoire де М. Péligiot, озаглавливать: Recherches Sur La природы и др ле Свойства chimiques де сукре" . Архивировано 6 декабря 2015 г. в Wayback Machine (Отчет о мемуарах г-на Пелиджио, озаглавленный: Исследования природы и химических свойств сахаров), Comptes rendus , 7 : 106–113. Со страницы 109 . Архивировано 6 декабря 2015 года на Wayback Machine : "Илы résulte де Comparaisons Faites пар М. Пелья, дие ле сукре де изюм, celui d'Amidon, celui де сахарный диабет и др celui де Миэль ОНТ parfaitement л même композиции и др ль мема Свойство, и др составного корпус ип Seul дие поиз proposons d'appeler Глюкоза (1). … (1) γλευχος , moût, vin doux. "Из сравнений, сделанных г-ном Пелиго, следует, что сахар из винограда, сахар из крахмала, сахар от диабета и сахар из меда имеют точно такой же состав и одинаковые свойства и представляют собой единое вещество, которое мы предлагаем назвать глюкозой. (1)… (1) γλευχος , сусло, сладкое вино.
- ^ а б Энциклопедия еды и здоровья . Академическая пресса. 2015. стр. 239. ISBN. 9780123849533. Архивировано 23 февраля 2018 года.
- ^ Маргграф (1747) «Опыт chimiques Faites данс ль Dessein де tirer ун настоящего сукре де Diverses Плант, квьте croissent данс н.у.к. contrées» архивации 2016-06-24 в Wayback Machine [Химические опытыпроведенные с целью извлечения сахара из реального разнообразно растения, которые растут на наших землях], Histoire de l'académie royale des Sciences et belles-lettres de Berlin , стр. 79–90. Со страницы 90: Архивировано 27 октября 2014 года в Wayback Machine "Les raisins secs, etant humectés d'une petite Quantité d'eau, de maniere qu'ils mollissent, peuvent alors etre pilés, & le Suc qu'on en exprime , etant depuré & épaissi, fournira une espece de Sucre ". (Изюм, смоченный небольшим количеством воды до размягчения, затем может быть отжат, и выдавленный сок, [после] очистки и загустения, станет своего рода сахаром.)
- ^ Джон Ф. Робит: Основы химии углеводов. Springer Science & Business Media, 2012, ISBN 978-1-461-21622-3 . п. 7.
- ^ Rosanoff, MA (1906). "О классификации стереоизомеров Фишера.1" . Журнал Американского химического общества . 28 : 114–121. DOI : 10.1021 / ja01967a014 .
- ↑ Эмиль Фишер , Фонд Нобеля, заархивировано из оригинала 3 сентября 2009 г. , извлечено 2 сентября 2009 г.
- ^ Фрейзер-Рид, Берт, "Глюкоза Вант-Хоффа", Chem. Англ. Новости , 77 (39): 8
- ^ "Отто Мейерхоф - Факты - NobelPrize.org" Архивировано 15 июля 2018 г. в Wayback Machine . NobelPrize.org . Проверено 5 сентября 2018.
- ^ "Ганс фон Эйлер-Челпин - Факты - NobelPrize.org" Архивировано 3 сентября 2018 г. в Wayback Machine . NobelPrize.org . Проверено 5 сентября 2018.
- ^ "Артур Харден - Факты - NobelPrize.org" Архивировано 3 сентября 2018 г. в Wayback Machine . NobelPrize.org . Проверено 5 сентября 2018.
- ^ "Бернардо Хусей - Факты - NobelPrize.org" Архивировано 15 июля 2018 г. в Wayback Machine . NobelPrize.org . Проверено 5 сентября 2018.
- ^ "Карл Кори - Факты - NobelPrize.org" Архивировано 15 июля 2018 г. в Wayback Machine . NobelPrize.org . Проверено 5 сентября 2018.
- ^ "Герти Кори - Факты - NobelPrize.org" Архивировано 15 июля 2018 г. в Wayback Machine . NobelPrize.org . Проверено 5 сентября 2018.
- ^ "Луис Лелуар - Факты - NobelPrize.org" Архивировано 15 июля 2018 г. в Wayback Machine . NobelPrize.org . Проверено 5 сентября 2018.
- ^ Венюе Кан и Чжицзюнь Чжан (2020): «Селективное производство уксусной кислоты с помощью каталитического быстрого пиролиза гексоз над солями калия», Катализаторы , том 10, страницы 502-515. ‹См. Tfd› doi : 10.3390 / catal10050502
- ^ Ебра-Biurrun, MC (2005), "подсластители", Энциклопедия аналитической науки , Elsevier, стр 562-572,. DOI : 10.1016 / b0-12-369397-7 / 00610-5 , ISBN 978-0-12-369397-6
- ^ "глюкоза". Колумбийская энциклопедия, 6-е изд .. 2015. Encyclopedia.com. 17 ноября 2015 г. http://www.encyclopedia.com Архивировано 26 апреля2009 г. в Wayback Machine .
- ^ a b Скенк, Фред В. (2006). «Глюкоза и глюкозосодержащие сиропы». Энциклопедия промышленной химии Ульмана . DOI : 10.1002 / 14356007.a12_457.pub2 . ISBN 978-3527306732.
- ↑ Патрик Ф. Фокс: Продвинутая химия молочных продуктов, Том 3: Лактоза, вода, соли и витамины , Спрингер, 1992. Том 3, ISBN 9780412630200 . п. 316.
- ^ Бенджамин Кабальеро, Пол Финглас, Фидель Толдра: Энциклопедия еды и здоровья . Академическая пресса (2016). ISBN 9780123849533 , Том 1, стр. 76.
- ^ Takagi, S .; Джеффри, Джорджия (1979). «1,2-О-изопропилиден-D-глюкофураноза». Acta Crystallographica Раздел B . B35 (6): 1522–1525. DOI : 10.1107 / S0567740879006968 .
- ^ Белецкий, Миа; Эггерт, Ханне; Кристиан Норрилд, Йенс (1999). «Флуоресцентный датчик глюкозы, ковалентно связывающийся со всеми пятью гидроксигруппами α-D-глюкофуранозы. Повторное исследование». Журнал химического общества, Perkin Transactions . 2 (3): 449–456. DOI : 10.1039 / A808896I .
- ^ Chandran, Sreekanth K .; Нангиа, Ашвини (2006). «Модулированная кристаллическая структура (Z '= 2) α-d-глюкофуранозо-1,2∶3,5-бис (п-толил) бороната». CrystEngComm . 8 (8): 581–585. DOI : 10.1039 / B608029D .
- ^ Макмерри, Джон Э. (1988), Органическая химия (2-е изд.), Брукс / Коул, стр. 866, ISBN 0534079687.
- ^ Хуаристи, Эйсебио; Куэвас, Габриэль (1995), Аномерный эффект , CRC Press, стр. 9–10, ISBN 978-0-8493-8941-2
- ^ a b Манфред Гессе, Герберт Мейер, Бернд Зе, Стефан Биенц, Лоран Биглер, Томас Фокс: Spektroskopische Methoden in der Organischen Chemie . 8-е исправленное издание. Георг Тиме, 2011, ISBN 978-3-13-160038-7 , стр. 34 (на немецком языке).
- ^ а б в г Банн, HF; Хиггинс, П.Дж. (1981). «Реакция моносахаридов с белками: возможное эволюционное значение». Наука . 213 (4504): 222–24. Bibcode : 1981Sci ... 213..222B . DOI : 10.1126 / science.12192669 . PMID 12192669 .
- ^ Джереми М. Берг: Stryer Biochemie. Springer-Verlag, 2017, ISBN 978-3-662-54620-8 , стр. 531. (немецкий)
- ^ Реджинальд Х. Гарретт: Биохимия. Обучение Cengage, 2012, ISBN 978-1-133-10629-6 . С. 194, 199.
- ^ Дональд Воет, Джудит Г. Воет: Биохимия, 4-е издание. Джон Вили и сыновья, 2010, ISBN 978-0470-57095-1 . п. 363.
- ^ Альберт Л. Ленингер, Биохимия, 6-е издание , Worth Publishers Inc. 1972, ISBN 0-87901-009-6 стр. 228.
- ^ a b Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3 , стр. 195. (немецкий)
- ^ а б в г д У. Сатьянараяна: Биохимия. Elsevier Health Sciences, 2014, ISBN 978-8-131-23713-7 . п. 674.
- ^ Вассерман, DH (2009). «Четыре грамма глюкозы» . Американский журнал физиологии. Эндокринология и обмен веществ . 296 (1): E11–21. DOI : 10,1152 / ajpendo.90563.2008 . PMC 2636990 . PMID 18840763 .
- ^ «Высокий уровень глюкозы в крови и осложнения диабета: накопление молекул, известных как AGE, может быть ключевым звеном» , Прогноз диабета , Американская диабетическая ассоциация, 2010, ISSN 0095-8301 , заархивировано из оригинала на 2013-10-14 , извлечено из 2010 -05-20
- ^ Основы гликобиологии . Аджит Варки (ред.) (2-е изд.). Издательство Cold Spring Harbor Laboratories Press. 2009. ISBN. 978-0-87969-770-9. Архивировано 6 декабря 2016 года.CS1 maint: другие ( ссылка )
- ^ Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3 , стр. 404.
- ^ Гарольд А. Харпер: Medizinische Biochemie. Springer-Verlag, 2013, ISBN 978-3-662-22150-1 , стр. 641. (немецкий)
- ^ Навале, AM; Паранджапе, АН (2016). «Транспортеры глюкозы: физиологические и патологические роли» . Биофизические обзоры . 8 (1): 5–9. DOI : 10.1007 / s12551-015-0186-2 . PMC 5425736 . PMID 28510148 .
- ^ a b c d e f g Peter C. Heinrich: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3 , стр. 199, 200. (немецкий)
- ^ Thorens, В. (2015). «GLUT2, определение глюкозы и гомеостаз глюкозы» . Диабетология . 58 (2): 221–32. DOI : 10.1007 / s00125-014-3451-1 . PMID 25421524 .
- ^ a b Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3 , стр. 214. (немецкий)
- ^ Хуанг, S .; Чехия, депутат (2007). «Транспортер глюкозы GLUT4». Клеточный метаболизм . 5 (4): 237–52. DOI : 10.1016 / j.cmet.2007.03.006 . PMID 17403369 .
- ^ Govers, R. (2014). Клеточная регуляция поглощения глюкозы переносчиком глюкозы GLUT4 . Успехи клинической химии . 66 . С. 173–240. DOI : 10.1016 / B978-0-12-801401-1.00006-2 . ISBN 9780128014011. PMID 25344989 .
- ^ Ghezzi, C .; Loo DDF; Райт, EM (2018). «Физиология почечной обработки глюкозы через SGLT1, SGLT2 и GLUT2» . Диабетология . 61 (10): 2087–2097. DOI : 10.1007 / s00125-018-4656-5 . PMC 6133168 . PMID 30132032 .
- ^ Поульсен, SB; Фентон, РА; Риг, Т. (2015). «Котранспорт натрия с глюкозой» . Текущее мнение в нефрологии и гипертонии . 24 (5): 463–9. DOI : 10.1097 / MNH.0000000000000152 . PMC 5364028 . PMID 26125647 .
- ^ «Химия для биологов: фотосинтез» . www.rsc.org . Архивировано 4 августа 2016 года . Проверено 5 февраля 2018 .
- ^ Смит, Элисон М .; Zeeman, Samuel C .; Смит, Стивен М. (2005). «Деградация крахмала». Анну. Rev. Plant Biol . 56 : 73–98. DOI : 10.1146 / annurev.arplant.56.032604.144257 . PMID 15862090 .
- ^ Дональд Воет, Джудит Г. Воет: Биохимия, 4-е издание. Джон Вили и сыновья, 2010, ISBN 978-0470-57095-1 . п. 359.
- ^ a b Дональд Воет, Джудит Г. Воет: Биохимия, 4-е издание. Джон Вили и сыновья, 2010, ISBN 978-0470-57095-1 . п. 59.
- ^ a b Leszek Szablewski: Гомеостаз глюкозы и резистентность к инсулину. Издательство Bentham Science, 2011, ISBN 978-1-608-05189-2 , стр. 46.
- ^ Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3 , стр. 389. (немецкий)
- ^ Адева-Андани, ММ; Pérez-Felpete, N .; Fernández-Fernández, C .; Donapetry-García, C .; Пасос-Гарсия, К. (2016). «Метаболизм глюкозы в печени у человека» . Отчеты по биологии . 36 (6): e00416. DOI : 10.1042 / BSR20160385 . PMC 5293555 . PMID 27707936 .
- ^ Х. Роберт Хортон, Лоуренс А. Моран, К. Грей Скримджер, Марк Д. Перри, Дж. Дэвид Рон: Биохимия . Студия Пирсона; 4. aktualisierte Auflage 2008; ISBN 978-3-8273-7312-0 ; п. 490–496. (Немецкий)
- ^ а б Брайан К. Холл: Эволюция Стрикбергера. Jones & Bartlett Publishers, 2013, ISBN 978-1-449-61484-3 , стр. 164.
- ^ Реджинальд Х. Гарретт: Биохимия. Cengage Learning, 2012, ISBN 978-1-133-10629-6 , стр. 551.
- ^ Джонс, JG (2016). «Глюкоза и липидный обмен в печени» . Диабетология . 59 (6): 1098–103. DOI : 10.1007 / s00125-016-3940-5 . PMID 27048250 .
- ^ Entner, N .; Дудоров, М. (1952). «Окисление глюкозы и глюконовой кислоты Pseudomonas saccharophila». J Biol Chem . 196 (2): 853–862. PMID 12981024 .
- ^ Бонадонна, Риккардо C; Бонора, Энцо; Дель Прато, Стефано; Саккомани, Мария; Кобелли, Клаудио; Натали, Андреа; Фрассерра, Сильвия; Пекори, Неда; Ферраннини, Элеутерио; Бир, Деннис; ДеФронцо, Ральф А; Гулли, Джованни (июль 1996 г.). «Роль транспорта глюкозы и фосфорилирования глюкозы в мышечной инсулинорезистентности NIDDM» (PDF) . Диабет . 45 (7): 915–25. DOI : 10.2337 / diab.45.7.915 . PMID 8666143 . S2CID 219249555 . Проверено 5 марта 2017 года .
- ^ Краткий обзор медицинской биохимии @Google books , Blackwell Publishing, 2006, p. 52, ISBN 978-1-4051-1322-9, архивировано 23 февраля 2018 г.
- ^ Краткий обзор медицинской биохимии @Google books , Blackwell Publishing, 2006, p. 50, ISBN 978-1-4051-1322-9, архивировано 23 февраля 2018 г.
- ^ Аннибальди, А .; Видманн, К. (2010). «Метаболизм глюкозы в раковых клетках». Текущее мнение о клиническом питании и метаболическом лечении . 13 (4): 466–70. DOI : 10.1097 / MCO.0b013e32833a5577 . PMID 20473153 . S2CID 205782021 .
- ^ Szablewski, L. (2013). «Экспрессия переносчиков глюкозы при раке». Biochimica et Biophysica Acta (BBA) - Обзоры рака . 1835 (2): 164–9. DOI : 10.1016 / j.bbcan.2012.12.004 . PMID 23266512 .
- ^ Adekola, K .; Розен, СТ; Шанмугам, М. (2012). «Транспортеры глюкозы в метаболизме рака» . Текущее мнение в онкологии . 24 (6): 650–4. DOI : 10,1097 / CCO.0b013e328356da72 . PMC 6392426 . PMID 22913968 .
- ^ «Глава 3: Расчет энергосодержания продуктов питания - коэффициенты преобразования энергии» , Энергия продуктов питания - методы анализа и коэффициенты преобразования , Документ 77 ФАО по продовольствию и питанию, Рим: Продовольственная и сельскохозяйственная организация, 2003 г., ISBN 978-92-5-105014-9, архивировано 24 мая 2010 г.
- ^ Георг Шведт: Zuckersüße Chemie. John Wiley & Sons, 2012, ISBN 978-3-527-66001-8 , стр. 100 (на немецком языке).
- ^ Schmidt, Lang: Physiologie des Menschen , 30. Auflage. Springer Verlag, 2007, стр. 907 (на немецком языке).
- ^ Dandekar, T .; Schuster, S .; Snel, B .; Huynen, M .; Борк, П. (1999). «Выравнивание пути: приложение для сравнительного анализа гликолитических ферментов» . Биохимический журнал . 343 (1): 115–124. DOI : 10.1042 / bj3430115 . PMC 1220531 . PMID 10493919 .
- ^ Даш, Прамод. «Кровяной мозговой барьер и церебральный метаболизм (раздел 4, глава 11)» . Neuroscience Online: Электронный учебник для неврологии . Отделение нейробиологии и анатомии - Медицинская школа Техасского университета в Хьюстоне. Архивировано из оригинала на 2016-11-17.
- ^ Fairclough, Стивен Х .; Хьюстон, Ким (2004), «Метаболическая мера умственного усилия», Biol. Psychol. , 66 (2): 177-190, DOI : 10.1016 / j.biopsycho.2003.10.001 , PMID 15041139 , S2CID 44500072
- ^ Gailliot, Мэтью Т .; Баумейстер, Рой Ф .; Деуолл, К. Натан; Плант, Э. Эшби; Брюэр, Лорен Э .; Шмейхель, Брэндон Дж .; Тайс, Дайан М .; Манер, Джон К. (2007), «Самоконтроль полагается на глюкозу как на ограниченный источник энергии: сила воли - это больше, чем метафора» (PDF) , J. Pers. Soc. Psychol. , 92 (2): 325–336, CiteSeerX 10.1.1.337.3766 , doi : 10.1037 / 0022-3514.92.2.325 , PMID 17279852 , архив (PDF) из оригинала 18.08.2017
- ^ Gailliot, Мэтью Т .; Баумейстер, Рой Ф. (2007), «Физиология силы воли: связь глюкозы в крови с самоконтролем», Personal. Soc. Psychol. Rev. , 11 (4): 303-327, CiteSeerX 10.1.1.475.9484 , DOI : 10,1177 / 1088868307303030 , PMID 18453466 , S2CID 14380313
- ^ Masicampo, EJ; Баумейстер, Рой Ф. (2008), «К физиологии двойного процесса рассуждений и суждений: лимонад, сила воли и дорогостоящий анализ на основе правил», Psychol. Sci. , 19 (3): 255-60, DOI : 10.1111 / j.1467-9280.2008.02077.x , PMID 18315798 , S2CID 38596025
- ^ a b c Донард Дуайер: метаболизм глюкозы в мозге. Academic Press, 2002, ISBN 978-0-123-66852-3 , стр. XIII.
- ^ a b c Koekkoek, LL; Mul, JD; Ла Флер, ЮВ (2017). «Глюкоза-зондирование в системе вознаграждения» . Границы неврологии . 11 : 716. DOI : 10,3389 / fnins.2017.00716 . PMC 5742113 . PMID 29311793 .
- ^ а б Такер, РМ; Тан, SY (2017). «Влияют ли непитательные подсластители на острый гомеостаз глюкозы у людей? Систематический обзор» . Физиология и поведение . 182 : 17–26. DOI : 10.1016 / j.physbeh.2017.09.016 . PMID 28939430 . S2CID 38764657 .
- ^ La Fleur, SE; Fliers, E .; Калсбек, А. (2014). Неврология гомеостаза глюкозы . Справочник по клинической неврологии . 126 . С. 341–351. DOI : 10.1016 / B978-0-444-53480-4.00026-6 . ISBN 9780444534804. PMID 25410233 ..
- ^ Бишоп, PH; Fliers, E .; Калсбек, А. (2015). «Вегетативная регуляция выработки глюкозы в печени». Комплексная физиология . 5 (1): 147–165. DOI : 10.1002 / cphy.c140009 . PMID 25589267 .
- ^ WA Scherbaum, BM Lobnig, В: Ханс-Петер Вольф, Томас Р. Weihrauch: Internistische Терапи 2006, 2007 . 16-е издание. Elsevier, 2006, ISBN 3-437-23182-0 , стр. 927, 985 (на немецком языке).
- ^ Гарольд А. Харпер: Medizinische Biochemie . Springer-Verlag, 2013, ISBN 978-3-662-22150-1 , стр. 294.
- ^ Кларк, SF; Фостер, младший (2012). «История глюкометров и их роль в самоконтроле сахарного диабета». Британский журнал биомедицинских наук . 69 (2): 83–93. CiteSeerX 10.1.1.468.2196 . DOI : 10.1080 / 09674845.2012.12002443 . PMID 22872934 . S2CID 34263228 .
- ^ «Диагностика диабета и изучение предиабета» . Американская диабетическая ассоциация . Архивировано 28 июля 2017 года . Проверено 20 февраля 2018 .
- ^ a b Ричард А. Харви, Дениз Р. Ферье: Биохимия . 5-е издание, Lippincott Williams & Wilkins, 2011, ISBN 978-1-608-31412-6 , стр. 366.
- ^ а б У Сатьянараяна: Биохимия . Elsevier Health Sciences, 2014, ISBN 978-8-131-23713-7 , стр. 508.
- ^ Холт, SH; Миллер, JC; Петоч П. (1997). «Индекс инсулина продуктов питания: потребность в инсулине, вызванная порциями обычных продуктов питания мощностью 1000 кДж» . Американский журнал клинического питания . 66 (5): 1264–1276. DOI : 10.1093 / ajcn / 66.5.1264 . PMID 9356547 .
- ^ a b Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3 , стр. 27. (немецкий)
- ^ Рёдер П.В., Ву В, Лю У, Хан W (2016). «Панкреатическая регуляция гомеостаза глюкозы» . Exp. Мол. Med . 48 (3, март): e219–. DOI : 10.1038 / emm.2016.6 . PMC 4892884 . PMID 26964835 .
- ^ Эстела, Карлос (2011) "Уровни глюкозы в крови", Журнал математического моделирования для студентов: One + Two: Vol. 3: Вып. 2, статья 12.
- ^ «Углеводы и сахар в крови» . Источник питания . 2013-08-05. Архивировано 30 января 2017 года . Проверено 30 января 2017 г. - через Harvard TH Chan School of Public Health.
- ^ "FoodData Central" . fdc.nal.usda.gov .
- ^ a b c d e f g h i P. J. Научные сотрудники: Технология пищевой промышленности. Woodhead Publishing , 2016, ISBN 978-0-081-00523-1 , стр. 197.
- ^ a b Томас Беккер, Дитмар Брайтхаупт, Хорст Вернер Доэль, Армин Фихтер, Гюнтер Шлегель, Сакаю Симидзу, Хидеаки Ямада: биотехнология , в: Энциклопедия промышленной химии Ульмана , 7-е издание, Wiley-VCH, 2011. ISBN 978-3-527 -32943-4 . Том 6, стр. 48.
- ^ a b c Японское общество исследования амилазы: Справочник по амилазам и родственным ферментам. Elsevier, 2014, ISBN 978-1-483-29939-6 , стр. 195.
- ^ Мадсен, Великобритания; Норман, BE; Слотт, С. (1973). «Новая термостойкая бактериальная амилаза и ее использование при высокотемпературном сжижении». Крахмал - Stärke . 25 (9): 304–308. DOI : 10.1002 / star.19730250906 .
- ^ Норман, BE (1982). «Новый фермент разветвления для применения в индустрии глюкозного сиропа». Крахмал - Stärke . 34 (10): 340–346. DOI : 10.1002 / star.19820341005 .
- ^ Джеймс Н. Бемиллер, Рой Л. Уистлер (2009). Крахмал: химия и технология . Пищевая наука и технология (3-е изд.). Нью-Йорк: Academic Press. ISBN 978-0080926551.
- ^ BeMiller, Джеймс Н .; Уистлер, Рой Л., ред. (2009). Крахмал: химия и технология . Пищевая наука и технология (3-е изд.). Нью-Йорк: Academic Press. ISBN 978-0080926551. Проверено 25 ноября +2016 .
- ^ Алан Дэвидсон: Oxford Companion to Food (1999). «Мидзуаме», стр. 510 ISBN 0-19-211579-0 .
- ^ Алан Дэвидсон: Оксфордский компаньон к еде . ОУП Оксфорд, 2014, ISBN 978-0-191-04072-6 , стр. 527.
- ^ Университет штата Орегон : Сахар , доступ28 июня 2018.
- ^ «Кукурузный сироп с высоким содержанием фруктозы: вопросы и ответы» . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 2014-11-05. Архивировано 25 января 2018 года . Проверено 18 декабря 2017 .
- ↑ Кевин Панг: « Мексиканская кока-кола» стала хитом в США In: Seattle Times , 29 октября 2004 г.
- ^ Стив Т. Беккет: Промышленное производство и использование шоколада Беккета . John Wiley & Sons, 2017, ISBN 978-1-118-78014-5 , стр. 82.
- ^ Джеймс А. Кент: Справочник Ригеля по промышленной химии . Springer Science & Business Media, 2013, ISBN 978-1-475-76431-4 , стр. 938.
- ^ Датан E, Minn I, Peng X, он QL, Ahn H, Ю.Б., Pomper М.Г., Liu Jo (2020). «Конъюгат глюкоза-триптолид селективно нацелен на раковые клетки в условиях гипоксии» . iScience . 23 (9): 101536. DOI : 10.1016 / j.isci.2020.101536 . PMC 7509213 . PMID 33083765 .
- ^ Х. Фелинг: Количественная оценка Цукерса им Харн . В: Archiv für Physiologische Heilkunde (1848), том 7, стр. 64–73 (на немецком языке).
- ^ B. Толленс: Über Аммон-alkalische Silberlösung ALS Reagens Ауф альдегид . В Berichte der Deutschen Chemischen Gesellschaft (1882 г.), том 15, стр. 1635–1639 (на немецком языке).
- ^ Barfoed, C. (1873). "Ueber die Nachweisung des Traubenzuckers neben Dextrin und verwandten Körpern" . Zeitschrift für Analytische Chemie (на немецком языке). 12 : 27–32. DOI : 10.1007 / BF01462957 . S2CID 95749674 .
- ^ Эмиль Nylander: Über alkalische Wismuthlösung ALS Reagens Ауф Traubenzucker им Харн , Zeitschrift für Chemie physiologische . Том 8, выпуск 3, 1884 г., стр. 175–185 Аннотация . Архивировано 23 сентября 2015 года в Wayback Machine (на немецком языке).
- ^ a b c d e f g h i Георг Шведт: Zuckersüße Chemie . John Wiley & Sons, 2012, ISBN 978-3-527-66001-8 , стр. 102 (на немецком языке).
- ^ Триндер, П. (1969). «Определение глюкозы в крови с использованием глюкозооксидазы с альтернативным кислородным акцептором». Анналы клинической биохимии . 6 : 24–27. DOI : 10.1177 / 000456326900600108 . S2CID 58131350 .
- ↑ Мидзогути, Макото; Исияма, Мунетака; Шига, Масанобу (1998). «Водорастворимый хромогенный реагент для колориметрического определения перекиси водорода - альтернатива 4-аминоантипирину, работающему на длинных волнах». Аналитические сообщения . 35 (2): 71–74. DOI : 10.1039 / A709038B .
- Перейти ↑ Wang, J. (2008). «Электрохимические биосенсоры глюкозы». Химические обзоры . 108 (2): 814–825. DOI : 10.1021 / cr068123a . PMID 18154363 . .
- ^ Чен, X .; Chen, J .; Deng, C .; Xiao, C .; Ян, Й .; Nie, Z .; Яо, С. (2008). «Амперометрический биосенсор глюкозы на основе электрода, модифицированного углеродными нанотрубками, легированными бором». Таланта . 76 (4): 763–767. DOI : 10.1016 / j.talanta.2008.04.023 . PMID 18656655 .
- ^ Ван, Гуанфэн; Вэй, Ян; Чжан, Вэй; Чжан, Сяоцзюнь; Клык, Бин; Ван, Лун (2010). «Безферментное амперометрическое определение глюкозы с использованием композитов нанопроволоки Cu-CuO». Microchimica Acta . 168 (1–2): 87–92. DOI : 10.1007 / s00604-009-0260-1 . S2CID 98567636 .
- ^ Охара, TJ; Rajagopalan, R .; Хеллер, А. (1994). « » Ферментные электроды Проводных «для амперометрического определения глюкозы или лактата в присутствии мешающих веществ». Аналитическая химия . 66 (15): 2451–2457. DOI : 10.1021 / ac00087a008 . PMID 8092486 .
- ^ а б Борисов СМ; Вольфбайс, О.С. (2008). «Оптические биосенсоры». Химические обзоры . 108 (2): 423–461. DOI : 10.1021 / cr068105t . PMID 18229952 .
- ^ Ферри, S .; Кодзима, К .; Соде, К. (2011). «Обзор глюкозооксидаз и глюкозодегидрогеназ: ферменты, чувствительные к глюкозе с высоты птичьего полета» . Журнал диабетической науки и технологий . 5 (5): 1068–76. DOI : 10.1177 / 193229681100500507 . PMC 3208862 . PMID 22027299 .
- ^ Мадер, Хайке S .; Вольфбайс, Отто С. (2008). «Зонды на основе бороновой кислоты для микроопределения сахаридов и гликозилированных биомолекул». Microchimica Acta . 162 (1–2): 1–34. DOI : 10.1007 / s00604-008-0947-8 . S2CID 96768832 .
- ^ Wolfbeis, Отто S .; Оэме, Инес; Папковская, Наталья; Климант, Инго (2000). «Биосенсоры глюкозы на основе золь – геля, использующие оптические преобразователи кислорода, и способ компенсации переменного кислородного фона». Биосенсоры и биоэлектроника . 15 (1–2): 69–76. DOI : 10.1016 / S0956-5663 (99) 00073-1 . PMID 10826645 .
- ^ a b Галант А.Л .; Кауфман, RC; Уилсон, JD (2015). «Глюкоза: обнаружение и анализ». Пищевая химия . 188 : 149–160. DOI : 10.1016 / j.foodchem.2015.04.071 . PMID 26041177 .
- ^ Санс, ML; Sanz, J .; Мартинес-Кастро, И. (2004). «Газохромато-масс-спектрометрический метод качественного и количественного определения дисахаридов и трисахаридов в меде». Журнал хроматографии A . 1059 (1–2): 143–148. DOI : 10.1016 / j.chroma.2004.09.095 . PMID 15628134 .
- ^ Институт молекулярной физиологии растений Макса Планка в базе данных Golm (2007-07-19). «Масс-спектр глюкозы» . База данных метаболома Голма . Архивировано 9 сентября 2018 года . Проверено 4 июня 2018 .
- ^ Cabañero, AI; Ресио, JL; Руперес, М. (2006). «Жидкостная хроматография в сочетании с масс-спектрометрией изотопного состава: новый взгляд на обнаружение фальсификации меда». J. Agric Food Chem . 54 (26): 9719–9727. DOI : 10.1021 / jf062067x . PMID 17177492 .
- ^ Беккер, М .; Либнер, Ф .; Розенау, Т .; Поттхаст, А. (2013). «Подход этоксимации-силилирования для анализа моно- и дисахаридов и характеристики их идентификационных параметров с помощью ГХ / МС». Таланта . 115 : 642–51. DOI : 10.1016 / j.talanta.2013.05.052 . PMID 24054643 .
- ^ Gesellschaft Deutscher Chemiker : wayback = 20100331071121 Anlagen zum Positionspapier der Fachgruppe Nuklearchemie Архивировано 31 марта 2010 г. в Wayback Machine , февраль 2000 г.
- ^ Maschauer, S .; Пранте, О. (2014). «Подслащивание фармацевтической радиохимии с помощью (18) f-фторгликозилирования: краткий обзор» . BioMed Research International . 2014 : 1–16. DOI : 10.1155 / 2014/214748 . PMC 4058687 . PMID 24991541 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме глюкозы . |
- «Глюкоза» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- «Смесь декстрозы с хлоридом натрия» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
| vте Путь метаболизма гликолиза |
|---|
Глюкоза Гексокиназа АТФ ADP Глюкозо-6-фосфат Глюкозо-6-фосфат- изомераза Фруктоза 6-фосфат Фосфофруктокиназа-1 АТФ ADP 1,6-бисфосфат фруктозы Фруктозо-бисфосфат альдолаза Дигидроксиацетонфосфат + + Глицеральдегид 3-фосфат Триозофосфат изомераза 2 × Глицеральдегид-3-фосфат 2 × Глицеральдегид-3- фосфатдегидрогеназа НАД + + P i НАДН + Н + НАД + + P i НАДН + Н + 2 × 1,3-бисфосфоглицерат 2 × Фосфоглицераткиназа ADP АТФ ADP АТФ 2 × 3-фосфоглицерат 2 × Фосфоглицерат мутаза 2 × 2-фосфоглицерат 2 × Phosphopyruvate гидратаз ( енолаз ) H 2 O H 2 O 2 × Фосфоенолпируват 2 × Пируваткиназа ADP АТФ 2 × Пируват 2 × |