
| Физика конденсированного состояния |
|---|
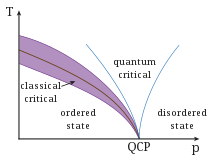 |
| Фазы · Фазовый переход · QCP |
Коллоид представляет собой смесь , в которой одно вещество микроскопически диспергированных нерастворимых частиц будут приостановлены в течение другого вещества. Тем не менее, некоторые определения указывают , что частицы должны быть диспергированы в жидкости , [1] и другие расширить определение включает вещества , такие как аэрозоли и гели . Термин коллоидная суспензия однозначно относится ко всей смеси (хотя в более узком смысле слова суспензияотличается от коллоидов более крупным размером частиц). Коллоид имеет дисперсную фазу (взвешенные частицы) и непрерывную фазу (суспензионная среда). Частицы дисперсной фазы имеют диаметр приблизительно от 1 нанометра до 1 микрометра . [2] [3]
Некоторые коллоиды полупрозрачны из-за эффекта Тиндаля , который представляет собой рассеяние света частицами в коллоиде. Другие коллоиды могут быть непрозрачными или иметь слабый цвет.
Коллоидные суспензии являются предметом науки о взаимодействии и коллоидах . Эта область исследований была введена в 1845 г. итальянским химиком Франческо Селми [4], а с 1861 г. ее исследовал шотландский ученый Томас Грэхем . [5]
Классификация [ править ]
Коллоиды можно разделить на следующие категории:
| Среда / фаза | Дисперсная фаза | |||
|---|---|---|---|---|
| Газ | Жидкость | Твердый | ||
| Дисперсионная среда | Газ | Такие коллоиды неизвестны. Известно, что гелий и ксенон при определенных условиях не смешиваются . [9] [10] | Примеры жидких аэрозолей : туман , облака , конденсат , туман , лаки для волос. | Примеры твердых аэрозолей : дым , ледяное облако , атмосферные твердые частицы. |
| Жидкость | Пример пены : взбитые сливки , крем для бритья. | Примеры эмульсии или жидких кристаллов : молоко , майонез , крем для рук , латекс , биологические мембраны , жидкий биомолекулярный конденсат. | Соль или подвески Примеры: пигментированные чернила , осадка , осадок , твердое вещество биомолекулярная конденсата | |
| Твердый | Примеры твердой пены : аэрогель , пенополистирол , пемза. | Гель Примеры: агар , желатин , желе , гелеобразный биомолекулярной конденсата | Твердый золь Пример: клюквенный стакан | |
Гомогенные смеси с дисперсной фазой в этом диапазоне размеров можно назвать коллоидными аэрозолями , коллоидными эмульсиями , коллоидными пенами , коллоидными дисперсиями или гидрозолями .
Коллоид по сравнению с раствором [ править ]
Коллоид имеет дисперсную фазу и непрерывную фазу, тогда как в растворе , то растворенное вещество и растворитель составляют только одну фазы. Растворенные вещества в растворе представляют собой отдельные молекулы или ионы , тогда как коллоидные частицы больше. Например, в растворе соли в воде кристалл хлорида натрия (NaCl) растворяется, и ионы Na + и Cl - окружены молекулами воды. Однако в коллоиде, таком как молоко, коллоидные частицы представляют собой шарики жира, а не отдельные молекулы жира.
Взаимодействие между частицами [ править ]
Следующие силы играют важную роль во взаимодействии коллоидных частиц: [11] [12]
- Исключенное объемное отталкивание : это относится к невозможности перекрытия между твердыми частицами.
- Электростатическое взаимодействие : коллоидные частицы часто несут электрический заряд и поэтому притягиваются или отталкиваются друг от друга. Заряд как непрерывной, так и дисперсной фазы, а также подвижность фаз являются факторами, влияющими на это взаимодействие.
- Силы Ван-дер-Ваальса : это происходит из-за взаимодействия между двумя диполями, которые являются постоянными или индуцированными. Даже если частицы не имеют постоянного диполя, флуктуации электронной плотности приводят к возникновению временного диполя в частице. Этот временный диполь индуцирует диполь в частицах поблизости. Затем временный диполь и индуцированные диполи притягиваются друг к другу. Это известно как сила Ван-дер-Ваальса, и она всегда присутствует (если показатели преломления дисперсной и непрерывной фаз не совпадают), является короткодействующей и привлекательной.
- Стерические силы между покрытыми полимером поверхностями или в растворах, содержащих неадсорбирующийся полимер, могут модулировать межчастичные силы, создавая дополнительную стерическую силу отталкивания (которая имеет преимущественно энтропийное происхождение) или притягивающую силу истощения между ними.
Скорость седиментации [ править ]
Гравитационное поле Земли действует на коллоидные частицы. Следовательно, если коллоидные частицы более плотные, чем среда суспензии, они будут осаждаться (упасть на дно), или, если они менее плотные, они будут сливаться (всплыть наверх). Более крупные частицы также имеют большую тенденцию к осаждению, поскольку они имеют меньшее броуновское движение, чтобы противодействовать этому движению.
Оседания или расслаивание скорости определяется путем приравнивания силы сопротивления Стокса с гравитационной силой :
где
- архимедова масса коллоидных частиц,
- вязкость суспензионной среды,
- радиус коллоидной частицы,
и - скорость осаждения или вспенивания.
Масса коллоидной частицы находится с использованием:
где
- объем коллоидной частицы, рассчитанный по объему шара ,
и - разница в массовой плотности между коллоидной частицей и суспензионной средой.
При перегруппировке скорость осаждения или взбивания составляет:
Существует верхний предел размера для диаметра коллоидных частиц, поскольку частицы размером более 1 мкм имеют тенденцию к осаждению, и, таким образом, вещество больше не будет считаться коллоидной суспензией. [13]
Говорят, что коллоидные частицы находятся в седиментационном равновесии, если скорость седиментации равна скорости движения от броуновского движения.
Подготовка [ править ]
Есть два основных способа приготовления коллоидов: [14]
- Диспергирование крупных частиц или капель до коллоидных размеров путем измельчения, распыления или приложения усилия сдвига (например, встряхивания, перемешивания или перемешивания с большим усилием сдвига ).
- Конденсация мелких растворенных молекул в более крупные коллоидные частицы путем осаждения , конденсации или окислительно-восстановительных реакций. Такие процессы используются при получении коллоидного кремнезема или золота .
Коллоидная стабильность [ править ]
Стабилизация [ править ]
Стабильность коллоидной системы определяется частицами, остающимися взвешенными в растворе, и зависит от сил взаимодействия между частицами. К ним относятся электростатические взаимодействия и силы Ван-дер-Ваальса, поскольку они оба вносят вклад в общую свободную энергию системы. [15]
Коллоид является стабильным, если энергия взаимодействия из-за сил притяжения между коллоидными частицами меньше kT , где k - постоянная Больцмана, а T - абсолютная температура . Если это так, то коллоидные частицы будут отталкиваться или слабо притягиваться друг к другу, и вещество останется суспензией.
Если энергия взаимодействия больше, чем kT, силы притяжения будут преобладать, и коллоидные частицы начнут слипаться. Этот процесс обычно называют агрегацией , но также называют флокуляцией , коагуляцией или осаждением . [16] Хотя эти термины часто используются как синонимы, для некоторых определений они имеют немного разные значения. Например, коагуляция может использоваться для описания необратимой постоянной агрегации, когда силы, удерживающие частицы вместе, сильнее любых внешних сил, вызванных перемешиванием или смешиванием. Флокуляцию можно использовать для описания обратимой агрегации с участием более слабых сил притяжения, и этот агрегат обычно называютфлок . Термин «осаждение» обычно используется для описания фазового перехода от коллоидной дисперсии к твердому (осадку), когда он подвергается возмущению. [13] Агрегация вызывает седиментацию или образование сливок, поэтому коллоид нестабилен: если происходит какой-либо из этих процессов, коллоид больше не будет суспензией.
Электростатическая стабилизация и стерическая стабилизация - два основных механизма стабилизации от агрегации.
- Электростатическая стабилизация основана на взаимном отталкивании одноименных электрических зарядов. Заряд коллоидных частиц структурирован в двойном электрическом слое , где частицы заряжаются на поверхности, но затем притягивают противоионы (ионы противоположного заряда), которые окружают частицу. Электростатическое отталкивание между взвешенными коллоидными частицами легче всего количественно определить с помощью дзета-потенциала . Совместное влияние ван-дер-ваальсова притяжения и электростатического отталкивания на агрегацию количественно описывается теорией DLVO . [17] Распространенным методом стабилизации коллоида (превращения его из осадка) является пептизация , процесс, при котором его встряхивают с электролитом.
- Стерическая стабилизация заключается в поглощении слоя полимера или поверхностно-активного вещества на частицах, чтобы предотвратить их сближение в диапазоне сил притяжения. [13]
Возможна также комбинация двух механизмов (электростерическая стабилизация).
Метод, называемый стабилизацией гелевой сетки, представляет собой основной способ получения коллоидов, устойчивых как к агрегации, так и к седиментации. Метод заключается в добавлении к коллоидной суспензии полимера, способного образовывать гелевую сетку. Осаждению частиц препятствует жесткость полимерной матрицы, в которой частицы захватываются [18], а длинные полимерные цепи могут обеспечивать стерическую или электростерическую стабилизацию диспергированных частиц. Примерами таких веществ являются ксантан и гуаровая камедь .
Дестабилизация [ править ]
Дестабилизация может осуществляться разными способами:
- Удаление электростатического барьера, предотвращающего агрегацию частиц. Это может быть достигнуто путем добавления соли к суспензии для уменьшения дебаевской длины просеивания (ширины двойного электрического слоя) частиц. Это также достигается путем изменения pH суспензии, чтобы эффективно нейтрализовать или «экранировать» поверхностный заряд частиц в суспензии. [1] Это устраняет силы отталкивания, которые разделяют коллоидные частицы, и обеспечивает коагуляцию из-за сил Ван-дер-Ваальса. Незначительные изменения pH могут проявляться в значительном изменении дзета-потенциала . Когда величина дзета-потенциалалежит ниже определенного порога, обычно около ± 5 мВ, имеет тенденцию происходить быстрая коагуляция или агрегация. [19]
- Добавление заряженного полимерного флокулянта. Полимерные флокулянты могут связывать отдельные коллоидные частицы за счет притягивающих электростатических взаимодействий. Например, отрицательно заряженные частицы коллоидного диоксида кремния или глины могут флокулироваться путем добавления положительно заряженного полимера.
- Добавление неадсорбированных полимеров, называемых деплетантами, которые вызывают агрегацию из-за энтропийных эффектов.
Нестабильные коллоидные суспензии фракции малого объема образуют кластерные жидкие суспензии, в которых отдельные кластеры частиц осаждаются, если они более плотные, чем суспензионная среда, или кремовые, если они менее плотные. Однако коллоидные суспензии фракции большего объема образуют коллоидные гели с вязкоупругими свойствами. Вязкоупругие коллоидные гели, такие как бентонит и зубная паста , текут как жидкости при сдвиге, но сохраняют свою форму, когда сдвиг снимается. Именно по этой причине зубную пасту можно выдавить из тюбика с зубной пастой, но она остается на зубной щетке после ее нанесения.
Мониторинг стабильности [ править ]
Наиболее широко используемый метод контроля состояния дисперсии продукта, а также выявления и количественной оценки явлений дестабилизации - это многократное рассеяние света в сочетании с вертикальным сканированием. [20] [21] [22] [23] Этот метод, известный как турбидиметрия, основан на определении количества света, излучаемого источником, и количества света, достигающего детектора после прохождения через образец коллоида. Когда свет проходит через образец, он отражается обратно коллоидными частицами. Интенсивность обратного рассеяния прямо пропорциональна среднему размеру частиц и объемной доле дисперсной фазы. Следовательно, локальные изменения концентрации, вызванные осаждением или вспениванием, и изменения размера частиц, вызванные агрегацией, обнаруживаются и контролируются. [24] Эти явления связаны с нестабильными коллоидами.
Ускоряющие методы прогнозирования срока годности [ править ]
Кинетический процесс дестабилизации может быть довольно длительным (до нескольких месяцев или даже лет для некоторых продуктов), и разработчику рецептур часто требуется использовать дополнительные методы ускорения, чтобы достичь разумного времени разработки дизайна нового продукта. Чаще всего используются термические методы, заключающиеся в повышении температуры для ускорения дестабилизации (ниже критических температур фазового обращения или химического разложения). Температура влияет не только на вязкость, но и на межфазное натяжение в случае неионных поверхностно-активных веществ или, в более общем смысле, на силы взаимодействия внутри системы. Хранение дисперсии при высоких температурах позволяет смоделировать реальные условия для продукта (например, тюбик солнцезащитного крема в автомобиле летом), а также ускорить процессы дестабилизации до 200 раз.Механическое ускорение, включая вибрацию,иногда используются центрифугирование и перемешивание. Они подвергают продукт воздействию различных сил, которые толкают частицы / капли друг к другу, тем самым способствуя дренажу пленки. Однако некоторые эмульсии никогда не слипнутся при нормальной гравитации, в отличие от искусственной. [25] Более того, сегрегация различных популяций частиц была подчеркнута при использовании центрифугирования и вибрации. [26]
Как модельная система для атомов [ править ]
В физике коллоиды представляют собой интересную модельную систему для атомов . [27] Коллоидные частицы микрометрового размера достаточно велики, чтобы их можно было наблюдать с помощью оптических методов, таких как конфокальная микроскопия . Многие силы, которые управляют структурой и поведением вещества, такие как исключенные объемные взаимодействия или электростатические силы, определяют структуру и поведение коллоидных суспензий. Например, те же методы, что и для моделирования идеальных газов, можно применить для моделирования поведения коллоидной суспензии твердых сфер. Кроме того, фазовые переходы в коллоидных суспензиях можно изучать в реальном времени с помощью оптических методов [28].и аналогичны фазовым переходам в жидкостях. Во многих интересных случаях оптическая текучесть используется для контроля коллоидных суспензий. [28] [29]
Кристаллы [ править ]
Коллоидная кристалл представляет собой высоко заказал массив частиц , которые могут быть образованы в течение очень длительного диапазона (обычно порядка нескольких миллиметров до одного сантиметра) и которые появляются аналогично их атомных или молекулярных аналогов. [30] Один из лучших природных примеров этого явления упорядочения можно найти в драгоценном опале , в котором блестящие области чистого спектрального цвета являются результатом плотноупакованных доменов аморфных коллоидных сфер диоксида кремния (или кремнезема , SiO 2 ). [31] [32]Эти сферические частицы осаждаются в высококремнистых лужах в Австралии и других местах и образуют эти высокоупорядоченные массивы после многих лет осаждения и сжатия под действием гидростатических и гравитационных сил. Периодические массивы сферических частиц субмикронного размера создают аналогичные массивы межузельных пустот , которые действуют как естественная дифракционная решетка для видимых световых волн , особенно когда межузельный интервал имеет тот же порядок величины, что и падающая световая волна. [33][34]
Таким образом, в течение многих лет было известно, что из-за отталкивающих кулоновских взаимодействий электрически заряженные макромолекулы в водной среде могут демонстрировать дальнодействующие кристаллические корреляции с расстояниями между частицами, часто значительно превышающими диаметр отдельных частиц. Во всех этих случаях в природе, та же самая блестящая переливы (или игра цветов) можно отнести к дифракции и интерференции видимых lightwaves , которые удовлетворяют закон Брэгга , в материи , аналогичная рассеянию от рентгеновских лучей в кристаллических твердых телах.
Большое количество экспериментов по изучению физики и химии этих так называемых «коллоидных кристаллов» возникло в результате относительно простых методов, разработанных за последние 20 лет для получения синтетических монодисперсных коллоидов (как полимерных, так и минеральных) и, через различные механизмы, реализующие и сохраняющие их формирование дальнего порядка. [35]
В биологии [ править ]
Коллоидное фазовое разделение является важным организационным принципом для компартментализации как цитоплазмы, так и ядра клеток в биомолекулярные конденсаты , аналогичные по важности компартментализации через липидные двухслойные мембраны - тип жидких кристаллов . Термин биомолекулярный конденсат используется для обозначения кластеров макромолекул, которые возникают в результате разделения фаз жидкость-жидкость или жидкость-твердое тело внутри клеток. Макромолекулярное скопление сильно усиливает разделение коллоидной фазы и образование биомолекулярных конденсатов .
В окружающей среде [ править ]
Коллоидные частицы также могут служить переносчиком [36] различных загрязнителей в поверхностных водах (морская вода, озера, реки, пресные водоемы) и в подземных водах, циркулирующих в трещиноватых породах [37] (например, известняк , песчаник , гранит ). Радионуклиды и тяжелые металлы легко сорбируются на взвешенных в воде коллоидах. Различают различные типы коллоидов: неорганические коллоиды (например, частицы глины , силикаты, оксигидроксиды железа ), органические коллоиды ( гуминовые и фульвовые вещества). Когда тяжелые металлы или радионуклиды образуют собственные чистые коллоиды, термин "eigencolloid "используется для обозначения чистых фаз, то есть чистого Tc (OH) 4 , U (OH) 4 или Am (OH) 3. Коллоиды подозреваются в переносе плутония на большие расстояния на ядерном полигоне в Неваде . Они были предметом подробных исследований в течение многих лет. Однако подвижность неорганических коллоидов очень мала в уплотненных бентонитах и в глубоких глинистых образованиях [38] из-за процесса ультрафильтрации, происходящего в плотной глинистой мембране. [39] Вопрос менее прозрачен для небольших органических коллоидов, часто смешанных в поровой воде с действительно растворенными органическими молекулами. [40]
В почвоведении , коллоидная фракция в почвах состоит из мельчайших глинистых и гумусовых частиц , которые меньше , чем 1 мкм в диаметре и несут либо положительные и / или отрицательные электростатические заряды , которые изменяются в зависимости от химических условий образца почвы, то есть рН почвы . [41]
Внутривенная терапия [ править ]
Коллоидные растворы, используемые при внутривенной терапии, относятся к основной группе расширителей объема и могут использоваться для замещения внутривенной жидкости . Коллоиды сохраняют высокое коллоидное осмотическое давление в крови, [42] и , следовательно, они должны теоретически преимущественно увеличить внутрисосудистый объем , в то время как другие типы объемных расширителей называемых кристаллоидами также увеличивают интерстициальный объем и внутриклеточный объем . Однако до сих пор существуют разногласия относительно реальной разницы в эффективности, связанной с этим различием [42].и большая часть исследований, связанных с этим использованием коллоидов, основана на мошеннических исследованиях Иоахима Болдта . [43] Другое отличие состоит в том, что кристаллоиды обычно намного дешевле коллоидов. [42]
Ссылки [ править ]
- ^ a b Исраэлачвили, Яков Н. (2011). Межмолекулярные и поверхностные силы (3-е изд.). Берлингтон, Массачусетс: Academic Press. ISBN 978-0-08-092363-5. OCLC 706803091 .
- ^ Международный союз чистой и прикладной химии. Подкомитет по полимерной терминологии (2009 г.). Компендиум терминологии и номенклатуры полимеров: рекомендации ИЮПАК, 2008 . Ричард Дж. Джонс, Международный союз чистой и прикладной химии. Комиссия по номенклатуре высокомолекулярных соединений. Кембридж: Королевское химическое общество. ISBN 978-1-84755-942-5. OCLC 406528399 .
- ^ Stepto, Роберт FT (1 января 2009). «Дисперсность в полимерной науке (Рекомендации ИЮПАК 2009 г.)» . Чистая и прикладная химия . 81 (2): 351–353. DOI : 10.1351 / PAC-REC-08-05-02 . ISSN 1365-3075 .
- ^ Francesco Selmi, Studi Сулла dimulsione ди cloruro d'Argento , Nuovi Annali делле Scienze Naturali ди Болонья, FASC. ди Агосто 1845.
- ^ Грэм ввел термин «коллоид» в 1861 году. См .: Graham, Thomas (1861) «Распространение жидкости в анализе» , Philosophical Transactions of the Royal Society of London , 151 : 183–224. Со страницы 183: «Поскольку желатин является его типом, предлагается обозначить вещества этого класса как коллоиды и говорить об их особой форме агрегации как о коллоидном состоянии вещества ».
- ^ а б Ричард Дж. Джонс; Эдвард С. Уилкс; В. Вал Метаномски; Ярослав Каховец; Майкл Хесс; Роберт Степто; Тацуки Китаяма, ред. (2009). Сборник терминологии и номенклатуры полимеров (Рекомендации ИЮПАК 2008 г.) (2-е изд.). РСК Publ. п. 464. ISBN 978-0-85404-491-7.
- ^ а б Степто, Роберт FT (2009). «Дисперсность в полимерной науке (Рекомендации ИЮПАК 2009 г.)» (PDF) . Чистая и прикладная химия . 81 (2): 351–353. DOI : 10.1351 / PAC-REC-08-05-02 . S2CID 95122531 .
- ^ Сломковский, Станислав; Alemán, José V .; Гилберт, Роберт Дж .; Гесс, Майкл; Хори, Казуюки; Джонс, Ричард Дж .; Кубиса, Пшемыслав; Мейзель, Ингрид; Морманн, Вернер; Пенчек, Станислав; Степто, Роберт FT (2011). «Терминология полимеров и процессов полимеризации в дисперсных системах (Рекомендации IUPAC 2011)» (PDF) . Чистая и прикладная химия . 83 (12): 2229–2259. DOI : 10.1351 / PAC-REC-10-06-03 . S2CID 96812603 .
- ^ de Swaan Arons, J .; Дипен, ГАМ (2010). «Несмешиваемость газов. Система He-Xe: (Краткое сообщение)». Recueil des Travaux Chimiques des Pays-Bas . 82 (8): 806. DOI : 10.1002 / recl.19630820810 . ISSN 0165-0513 .
- ^ de Swaan Arons, J .; Дипен, ГАМ (1966). «Газ — Газовые равновесия». J. Chem. Phys . 44 (6): 2322. Полномочный код : 1966JChPh..44.2322D . DOI : 10.1063 / 1.1727043 .
- ^ Lekkerkerker, Хенк NW; Туинье, Ремко (2011). Коллоиды и взаимодействие истощения . Гейдельберг: Springer. DOI : 10.1007 / 978-94-007-1223-2 . ISBN 9789400712225. Архивировано из оригинального 14 апреля 2019 года . Проверено 5 сентября 2018 года .
- ^ ван Андерс, Грег; Клоца, Дафна; Ахмед, Н. Халид; Энгель, Майкл; Глотцер, Шэрон К. (2014). «Понимание энтропии формы через локальную плотную упаковку» . Proc Natl Acad Sci USA . 111 (45): E4812 – E4821. arXiv : 1309.1187 . Bibcode : 2014PNAS..111E4812V . DOI : 10.1073 / pnas.1418159111 . PMC 4234574 . PMID 25344532 .
- ^ a b c Косгроув, Теренс (2010). Коллоидная наука: принципы, методы и приложения . Джон Вили и сыновья . ISBN 9781444320183.
- ^ Копелиович, Дмитрий. Приготовление коллоидов . substech.com
- Перейти ↑ Everett, DH (1988). Основные принципы коллоидной науки . Лондон: Королевское химическое общество. ISBN 978-1-84755-020-0. OCLC 232632488 .
- ^ Сломковский, Станислав; Alemán, José V .; Гилберт, Роберт Дж .; Гесс, Майкл; Хори, Казуюки; Джонс, Ричард Дж .; Кубиса, Пшемыслав; Мейзель, Ингрид; Морманн, Вернер; Пенчек, Станислав; Степто, Роберт FT (10 сентября 2011 г.). «Терминология полимеров и процессов полимеризации в дисперсных системах (Рекомендации IUPAC 2011)» . Чистая и прикладная химия (на немецком языке). 83 (12): 2229–2259. DOI : 10.1351 / PAC-REC-10-06-03 . ISSN 1365-3075 .
- ^ «Межмолекулярная сила» . Интерфейс науки и технологий . 18 : 1–57. 1 января 2011 г. doi : 10.1016 / B978-0-12-375049-5.00001-3 . ISSN 1573-4285 .
- ^ Комба, Сильвия; Сетхи (август 2009 г.). «Стабилизация высококонцентрированных суспензий наночастиц железа с использованием разжижающих сдвиг гелей ксантановой камеди». Исследования воды . 43 (15): 3717–3726. DOI : 10.1016 / j.watres.2009.05.046 . PMID 19577785 .
- ^ Бин, Элвуд L .; Кэмпбелл, Сильвестр Дж .; Анспах, Фредерик Р .; Окерсхаузен, Ричард В .; Питерман, Чарльз Дж. (1964). «Измерения дзета-потенциала в контроле доз химических веществ для свертывания крови [с обсуждением]» . Журнал (Американская ассоциация водопроводных сооружений) . 56 (2): 214–227. ISSN 0003-150X .
- ^ Роланд, я; Piel, G; Delattre, L; Эврард, Б. (2003). «Систематическая характеристика эмульсий типа« масло в воде »для разработки рецептур». Международный фармацевтический журнал . 263 (1-2): 85–94. DOI : 10.1016 / S0378-5173 (03) 00364-8 . PMID 12954183 .
- ^ Lemarchand, Кэролайн; Куврёр, Патрик; Беснар, Мадлен; Костантини, Доминик; Греф, Руксандра (2003). «Новые полиэфир-полисахаридные наночастицы». Фармацевтические исследования . 20 (8): 1284–92. DOI : 10,1023 / A: 1025017502379 . PMID 12948027 . S2CID 24157992 .
- ^ Mengual, О (1999). «Определение нестабильности концентрированных дисперсий с помощью нового оптического анализатора: TURBISCAN MA 1000». Коллоиды и поверхности A: физико-химические и технические аспекты . 152 (1–2): 111–123. DOI : 10.1016 / S0927-7757 (98) 00680-3 .
- ^ Bru, P .; и другие. (2004). Т. Провдер; J. Texter (ред.). Определение размеров и характеристик частиц .
- ^ Матусиак, Якуб; Grządka, Elżbieta (8 декабря 2017 г.). «Устойчивость коллоидных систем - обзор методов измерения устойчивости» . Annales Universitatis Mariae Curie-Sklodowska, section AA - Chemia . 72 (1): 33. DOI : 10,17951 / aa.2017.72.1.33 . ISSN 2083-358X .
- ^ Salager, JL (2000). Франсуаза Ниллу; Жильберте Марти-Местрес (ред.). Фармацевтические эмульсии и суспензии . CRC Press. п. 89. ISBN 978-0-8247-0304-2.
- ^ Снабре, Патрик; Пулиньи, Бернар (2008). «Разделение по размерам в жидко- или гелеобразной суспензии, оседающей под действием силы тяжести или в центрифуге». Ленгмюра . 24 (23): 13338–47. DOI : 10.1021 / la802459u . PMID 18986182 .
- ^ Манохаран, Vinothan Н. (2015). «Коллоидное вещество: упаковка, геометрия и энтропия» (PDF) . Наука . 349 (6251): 1253751. DOI : 10.1126 / science.1253751 . PMID 26315444 . S2CID 5727282 .
- ^ a b Гринфилд, Элад; Немировский, Джонатан; Эль-Ганаини, Рами; Christodoulides, Demetri N; Сегев, Мордехай (2013). «Нелинейно-оптическая манипуляция на основе ударных волн в плотно рассеивающих непрозрачных суспензиях» . Оптика Экспресс . 21 (20): 23785–23802. Bibcode : 2013OExpr..2123785G . DOI : 10,1364 / OE.21.023785 . PMID 24104290 .
- ^ Гринфилд, Элад; Ротшильд, Кармель; Самейт, Александр; Немировский, Джонатан; Эль-Ганаини, Рами; Христодулидес, Деметриос Н; Сараф, Мейрав; Лифшиц, Эфрат; Сегев, Мордехай (2011). «Светоиндуцированная самосинхронизирующиеся структуры потока» . Новый журнал физики . 13 (5): 053021. Bibcode : 2011NJPh ... 13e3021G . DOI : 10.1088 / 1367-2630 / 13/5/053021 .
- ^ Pieranski, P. (1983). «Коллоидные кристаллы». Современная физика . 24 : 25–73. Bibcode : 1983ConPh..24 ... 25P . DOI : 10.1080 / 00107518308227471 .
- ^ Сандерс, СП; Сандерс, СП; Сегнит, ER (1964). «Структура опала». Природа . 204 (4962): 1151. Bibcode : 1964Natur.204..990J . DOI : 10.1038 / 204990a0 . S2CID 4191566 .
- ^ Darragh, PJ; и другие. (1976). «Опалы». Scientific American . 234 (4): 84–95. Bibcode : 1976SciAm.234d..84D . DOI : 10.1038 / Scientificamerican0476-84 .
- ^ Удача, Вернер; Клиер, Манфред; Весслау, Герман (1963). "Über Bragg-Reflexe mit sichtbarem Licht an monodispersen Kunststofflatices. II". Berichte der Bunsengesellschaft für Physikalische Chemie . 67 (1): 84–85. DOI : 10.1002 / bbpc.19630670114 .
- ^ Хилтнер, Пенсильвания; Кригер, И.М. (1969). «Дифракция света на упорядоченных подвесах». J. Phys. Chem . 73 (7): 2306. DOI : 10.1021 / j100727a049 .
- ^ Лю, Сюэсон; Ли, Цзэцзин; Тан, Цзяньго; Ю, Бинг; Конг, Хайлинь (9 сентября 2013 г.). «Текущее состояние и перспективы получения и применения коллоидных кристаллов». Обзоры химического общества . 42 (19): 7774–7800. DOI : 10.1039 / C3CS60078E . ISSN 1460-4744 . PMID 23836297 .
- ^ Frimmel, Fritz H .; Франк фон дер Каммер; Ханс-Курт Флемминг (2007). Коллоидный транспорт в пористых средах (1-е изд.). Springer. п. 292. ISBN. 978-3-540-71338-8.
- ^ Алонсо, U .; Т. Миссана; А. Пателли; В. Ригато (2007). «Распространение бентонитового коллоида через вмещающую породу глубокого геологического хранилища». Физика и химия Земли, части A / B / C . 32 (1–7): 469–476. Bibcode : 2007PCE .... 32..469A . DOI : 10.1016 / j.pce.2006.04.021 . ISSN 1474-7065 .
- ^ Voegelin, A .; Кречмар, Р. (декабрь 2002 г.). «Стабильность и подвижность коллоидов в опалиновой глине» (PDF) . Technischer Bericht / NTB . Институт экологии суши, ETH Zürich. Технический отчет Nagra 02-14 .: 47. ISSN 1015-2636 . Архивировано из оригинального (PDF) 9 марта 2009 года . Проверено 22 февраля 2009 года .
- ^ "Диффузия коллоидов в уплотненном бентоните" . Архивировано из оригинала 4 марта 2009 года . Проверено 12 февраля 2009 года .
- ^ Уолд, Сюзанна; Трюгве Эриксен (2007). «Диффузия гуминовых коллоидов в уплотненном бентоните». Физика и химия Земли, части A / B / C . 32 (1–7): 477–484. Bibcode : 2007PCE .... 32..477W . DOI : 10.1016 / j.pce.2006.05.002 . ISSN 1474-7065 .
- ↑ R., Weil, Ray (11 октября 2018 г.). Элементы природы и свойств почв . Брэди, Найл С. (Четвертое изд.). Нью-Йорк, штат Нью-Йорк. ISBN 9780133254594. OCLC 1035317420 .
- ^ a b c Мартин, Грегори С. (19 апреля 2005 г.). «Обновленная информация о внутривенных жидкостях» . Medscape . Спасение от инфекционных заболеваний . Проверено 6 июля +2016 .
- ↑ Блейк, Хайди (3 марта 2011 г.). «Миллионы хирургических пациентов в группе риска в скандале с мошенничеством при исследовании наркотиков» . Телеграф . СОЕДИНЕННОЕ КОРОЛЕВСТВО. Архивировано из оригинала 4 ноября 2011 года . Проверено 4 ноября 2011 года .
Дальнейшее чтение [ править ]
- Берг, Дж. К. Введение в интерфейсы и коллоиды: мост к нанонауке. World Scientific Publishing Co., 2010, ISBN 981-4293-07-5
- Lyklema, J. Основы интерфейсной и коллоидной науки , Vol. 2, стр. 3208, 1995 г.
- Хантер, Р.Дж., Фонды коллоидной науки , издательство Оксфордского университета , 1989 г.
- Духин, С.С., Дерягин, Б.В. Электрокинетические явления , J. Wiley and Sons, 1974.
- Рассел, У. Б., Сэвилл, Д. А. и Шовальтер, У. Р. Коллоидные дисперсии , Кембридж, 1989 Cambridge University Press
- Крюйт, HR Colloid Science , Volume 1, Необратимые системы, Elsevier , 1959.
- Духин, А.С. и Гетц, П.Дж. Ультразвук для характеристики коллоидов , Elsevier, 2002.
- Родил, Ма. Лурдес К., Химия - центральная наука , 7-е изд. ISBN 0-13-533480-2
- Пиерански П. Коллоидные кристаллы // Contemp. Phys. , Vol. 24, стр. 25 (1983)
- Сандерс СП. Структура опала // Природа. 204, стр. 1151, (1964);
- Darragh, PJ, et al., Scientific American, Vol. 234, стр. 84, (1976)
- Luck, W. et al., Ber. Busenges Phys. Chem., Vol. 67, стр. 84 (1963);
- Хилтнер П.А., Кригер И.М. Дифракция света на упорядоченных суспензиях // J. Phys. Chem., Vol. 73, стр. 2306 (1969)
- Арора, АК, Тата, БВР, ред. Порядок и фазовые переходы в заряженных коллоидах Wiley, New York (1996)
- Суд, А.К., Физика твердого тела , Под ред. Эренрайх, Х., Тернбулл, Д., Vol. 45, стр. 1 (1991)
- Мюррей, Калифорния, и Гриер, Д. Г., Коллоидные кристаллы , Amer. Ученый, Vol. 83, стр. 238 (1995);
- Видеомикроскопия монодисперсных коллоидных систем , Annu. Rev. Phys. Chem., Vol. 47, стр. 421 (1996)
- Танака Т., Отзывчивые гели, Объемные переходы 1 , Под ред. Карл Дусек, Достижения в науке о полимерах, том 109, Springer Berlin (1993)









