 | |
| Имена | |
|---|---|
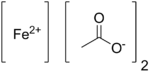
| Название ИЮПАК Железо (II) ацетат | |
| Другие имена Ацетат железа | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ChemSpider | |
| ECHA InfoCard | 100.019.492 |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| C 4 H 6 Fe O 4 | |
| Молярная масса | 173,933 г · моль -1 |
| Внешность | Белые кристаллы (безводные) Светло-зеленые кристаллы (тетрагидрат) |
| Запах | Без запаха |
| Плотность | 1,734 г / см 3 (-73 ° C) [1] |
| Температура плавления | 190–200 ° C (374–392 ° F, 463–473 K) разлагается [2] [3] |
| Растворимый [2] | |
| Структура | |
| Ромбическая , oP75 (200 К) | |
| Пбн, № 60 (200 К) [1] | |
| 2 / м 2 / м 2 / м (200 К) | |
a = 18,1715 (4) Å, b = 22,1453 (5) Å, c = 8,2781 (2) Å (200 K) α = 90 °, β = 90 °, γ = 90 ° | |
| Опасности | |
| Пиктограммы GHS |  [3] [3] |
| Сигнальное слово GHS | Предупреждение |
| H315 , H319 , H335 [3] | |
| P261 , P305 + 351 + 338 [3] | |
| NFPA 704 (огненный алмаз) | [4]  2 0 0 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Ацетат железа (II) представляет собой координационный комплекс с формулой Fe (O 2 CCH 3 ) 2 . Это белое твердое вещество, хотя нечистые образцы могут быть слегка окрашенными. [1] Также известен светло-зеленый тетрагидрат , который хорошо растворяется в воде.
Подготовка и структура [ править ]
Порошок железа реагирует с горячей уксусной кислотой с образованием ацетата двухвалентного железа с выделением газообразного водорода: [1]
- Fe + 2 CH 3 CO 2 H → Fe (CH 3 CO 2 ) 2 + H 2
Он также может быть изготовлен из нерастворимого карбоната железа (II) оливково-зеленого цвета . [ необходима цитата ]
Он имеет полимерную структуру с октаэдрическими центрами Fe (II), соединенными ацетатными лигандами. Это координационный полимер . [1]
Гидратированная форма получается реакцией закиси железа или гидроксида железа с уксусной кислотой . [5]
Реакция железного лома с уксусной кислотой дает коричневую смесь различных ацетатов железа (II) и железа (III), которые используются при крашении. [6]
Использует [ редактировать ]
Ацетат железа используется в красильной промышленности в качестве протравы . Эбонизация древесины - один из таких процессов. [7]
Ссылки [ править ]
- ^ Б с д е е Вебера, Birgit; Бец, Ричард; Бауэр, Вольфганг; Шламп, Стефан (2011). «Кристаллическая структура ацетата железа (II)». Zeitschrift für anorganische und allgemeine Chemie . 637 : 102–107. DOI : 10.1002 / zaac.201000274 .
- ^ a b Лиде, Дэвид Р., изд. (2009). CRC Справочник по химии и физике (90-е изд.). Бока-Ратон, Флорида : CRC Press . ISBN 978-1-4200-9084-0.
- ^ a b c d Sigma-Aldrich Co. , Ацетат железа (II) . Проверено 3 мая 2014.
- ^ "MSDS ацетата железа" . fishersci.ca . Ярмарка лужайки : Fisher Scientific . Проверено 2 августа 2014 .
- ^ «Синтез гидрата ацетата железа (II) (ацетат железа)» . Архивировано из оригинала на 2013-08-25 . Проверено 7 января 2009 .
- ^ Вильдермут, Эгон; Старк, Ганс; Фридрих, Габриэле; Эбенхох, Франц Людвиг; Кюборт, Бриджит; Сильвер, Джек; Ритупер, Рафаэль (2000). «Соединения железа». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a14_591 .
- ^ Эбонизация древесины ацетатом железа
| AcOH | Он | |||||||||||||||||||
| LiOAc | Be (OAc) 2 BeAcOH | B (OAc) 3 | AcOAc ROAc | NH 4 OAc | AcOOH | FAc | Ne | |||||||||||||
| NaOAc | Mg (OAc) 2 | Al (OAc) 3 АЛСОЛ Al (OAc) 2 OH Al 2 SO 4 (OAc) 4 | Si | п | S | ClAc | Ar | |||||||||||||
| KOAc | Ca (OAc) 2 | Sc (OAc) 3 | Ti (OAc) 4 | VO (OAc) 3 | Cr (OAc) 2 Cr (OAc) 3 | Mn (OAc) 2 Mn (OAc) 3 | Fe (OAc) 2 Fe (OAc) 3 | Co (OAc) 2 , Co (OAc) 3 | Ni (OAc) 2 | Cu (OAc) 2 | Zn (OAc) 2 | Ga (OAc) 3 | Ge | As (OAc) 3 | Se | BrAc | Kr | |||
| RbOAc | Sr (OAc) 2 | Y (OAc) 3 | Zr (OAc) 4 | Nb | Мо (OAc) 2 | Tc | Ru (OAc) 2 Ru (OAc) 3 Ru (OAc) 4 | Rh 2 (OAc) 4 | Pd (OAc) 2 | AgOAc | Cd (OAc) 2 | В | Sn (OAc) 2 Sn (OAc) 4 | Sb (OAc) 3 | Te | IAc | Xe | |||
| CsOAc | Ba (OAc) 2 | * | Лу (OAc) 3 | Hf | Та | W | Re | Операционные системы | Ir | Pt (OAc) 2 | Au | Hg 2 (OAc) 2 , Hg (OAc) 2 | TlOAc Tl (OAc) 3 | Pb (OAc) 2 Pb (OAc) 4 | Bi (OAc) 3 | По | В | Rn | ||
| Пт | Ра | ** | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Ур. | Ц | Og | ||
| * | La (OAc) 3 | Ce (OAc) x | Pr | Nd | Вечера | Sm (OAc) 3 | Eu (OAc) 3 | Gd (OAc) 3 | Tb | Dy (OAc) 3 | Хо (OAc) 3 | Э | Тм | Yb (OAc) 3 | ||||||
| ** | Ac | Чт | Па | UO 2 (OAc) 2 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | ||||||