 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Оксид свинца (II) | |
| Другие имена | |
| Идентификаторы | |
| ChemSpider | |
| ECHA InfoCard | 100,013,880 |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 3288 |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| PbO | |
| Молярная масса | 223,20 г / моль |
| Внешность | красный или желтый порошок |
| Плотность | 9,53 г / см 3 |
| Температура плавления | 888 ° С (1630 ° F, 1161 К) |
| Точка кипения | 1477 ° С (2691 ° F, 1750 К) |
| 0,017 г / л [1] | |
| Растворимость | не растворим в разбавленных щелочах , растворим в спирте в концентрированных щелочах, растворим в HCl , хлориде аммония |
| 4,20 × 10 -5 см 3 / моль | |
| Структура | |
| Тетрагональный , tP4 | |
| P4 / nmm, № 129 | |
| Опасности | |
| Паспорт безопасности | ICSC 0288 |
Классификация ЕС (DSD) (устарела) | Repr. Кот. 1/3 Токсично ( T ) Вредно ( Xn ) Опасно для окружающей среды ( N ) |
| R-фразы (устаревшие) | R61 , R20 / 22 , R33 , R62 , R50 / 53 |
| S-фразы (устаревшие) | S53 , S45 , S60 , S61 |
| NFPA 704 (огненный алмаз) |  3 0 0 |
| точка возгорания | Негорючий |
| Смертельная доза или концентрация (LD, LC): | |
LD Lo ( самый низкий опубликованный ) | 1400 мг / кг (собака, перорально) [2] |
| Родственные соединения | |
Другие анионы | Сульфид свинца Селенид свинца Теллурид свинца |
Другие катионы | Окись углерода Оксид кремния Оксид олова (II) |
Связанные оксиды свинца | Оксид свинца (II, II, IV) Диоксид свинца |
Родственные соединения | Оксид таллия (III) Оксид висмута (III) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Оксид свинца (II) , также называемый моноксид свинца , является неорганическим соединением с молекулярной формулой Pb O . PbO встречается в двух полиморфных формах : глет с тетрагональной кристаллической структурой и массикот с ромбической кристаллической структурой . Современные применения PbO в основном связаны с промышленным стеклом на основе свинца и промышленной керамикой, включая компьютерные компоненты. Это амфотерный оксид. [3]
Подготовка [ править ]
PbO может быть получен нагреванием металлического свинца на воздухе примерно до 600 ° C (1100 ° F). При этой температуре он также является конечным продуктом окисления других оксидов свинца на воздухе: [4]
- PbO
2 Pb
12О
19 Pb
12О
17 Pb
3О
4 PbO
Термическое разложение свинца (II) , нитрат или свинца (II) , карбонат , также приводит к образованию PbO:
- 2 Pb (НЕТ
3)
2→ 2 PbO + 4 НО2+ O
2 - PbCO
3→ PbO + CO2
PbO производится в больших масштабах как промежуточный продукт при переработке сырых свинцовых руд в металлический свинец. Обычная свинцовая руда - это галенит ( сульфид свинца (II) ). При температуре около 1000 ° C (1800 ° F) сульфид превращается в оксид: [5]
- 2 PbS + 3 O
2→ 2 PbO + 2 SO2
Металлический свинец получают восстановлением PbO оксидом углерода при температуре около 1200 ° C (2200 ° F): [6]
- PbO + CO → Pb + CO
2
Структура [ править ]
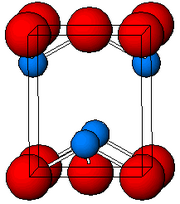
Как определено рентгеновской кристаллографией , оба полиморфа, тетрагональный и ромбический, имеют пирамидальный четырехкоординатный свинцовый центр. В тетрагональной форме четыре связи свинец – кислород имеют одинаковую длину, но в ромбической две - короче, а две - длиннее. Пирамидальный характер указывает на наличие стереохимически активной неподеленной пары электронов. [7] Когда PbO встречается в структуре тетрагональной решетки, это называется глетом ; а когда PbO имеет ромбическую решетчатую структуру, его называют массикотом . PbO можно изменить с массикота на глет и наоборот, контролируя нагрев и охлаждение. [8]Тетрагональная форма обычно красного или оранжевого цвета, в то время как ромбическая обычно желтого или оранжевого цвета, но цвет не очень надежный индикатор структуры. [9] Тетрагональные и ромбические формы PbO встречаются в природе как редкие минералы.
Реакции [ править ]
Красная и желтая формы этого материала связаны небольшим изменением энтальпии :
- PbO (красный) → PbO (желтый) Δ H = 1,6 кДж / моль
PbO является амфотерным , что означает, что он реагирует как с кислотами, так и с основаниями. С кислотами образует соли Pb.2+
через посредство оксо- кластеров, таких как [Pb
6О (ОН)
6]4+
. С сильными основаниями PbO растворяется с образованием солей плюмбита (также называемого плюмбатом (II)): [10]
- PbO + H2О + ОН-
→ [Pb (OH)
3]-
Приложения [ править ]
Свинец в свинцовом стекле обычно представляет собой PbO, и PbO широко используется при производстве стекла. В зависимости от стекла преимуществом использования PbO в стекле может быть одно или несколько из увеличения показателя преломления стекла, уменьшения вязкости стекла, увеличения удельного электрического сопротивления стекла и увеличения способности стекла поглощать. Рентгеновские лучи . Добавление PbO в промышленную керамику (а также стекло) делает материалы более магнитно и электрически инертными (за счет повышения их температуры Кюри ), и он часто используется для этой цели. [11] Исторически PbO также широко использовался в керамической глазури.для бытовой керамики, и он все еще используется, но уже не так широко. Другие, менее распространенные области применения включают вулканизацию резины и производство определенных пигментов и красок. [3] PbO используется в стекле электронно-лучевой трубки для блокирования рентгеновского излучения, но в основном в шейке и воронке, поскольку он может вызвать обесцвечивание при использовании на лицевой панели. Для лицевой панели предпочтительнее оксид стронция . [ необходима цитата ]
Потребление свинца и, следовательно, переработка PbO коррелирует с количеством автомобилей, поскольку он остается ключевым компонентом автомобильных свинцово-кислотных аккумуляторов . [12]
Ниша или отказ от использования [ править ]
Смесь PbO с глицерином затвердевает в твердом водонепроницаемом цементе , который использовался для соединения плоских стеклянных стенок и дна аквариумов , а также когда-то использовался для герметизации стеклянных панелей в оконных рамах. Входит в состав свинцовых красок .
PbO использовался для ускорения процесса, чтобы получить больше прибыли за меньшее время и искусственно повысить качество столетних яиц , типа китайских консервированных яиц . На некоторых небольших фабриках это была недобросовестная практика, но она стала широко распространяться в Китае и вынудила многих честных производителей маркировать свои коробки «бессвинцовыми» после того, как скандал стал массовым в 2013 году.
В виде порошка тетрагональной глетки его можно смешать с льняным маслом, а затем прокипятить, чтобы получить стойкую к атмосферным воздействиям проклейку, используемую при золочении . Глет придает проклейке темно-красный цвет, благодаря которому сусальное золото выглядит теплым и блестящим, а льняное масло придает адгезию и плоскую прочную связывающую поверхность.
PbO используется в некоторых реакциях конденсации в органическом синтезе . [13]
PbO - это входной фотопроводник в трубке видеокамеры, называемой Plumbicon .
Проблемы со здоровьем [ править ]
Оксид свинца может быть смертельным при проглатывании или вдыхании. Вызывает раздражение кожи, глаз и дыхательных путей. Он влияет на ткань десен, центральную нервную систему, почки, кровь и репродуктивную систему. Он может накапливаться в организме растений и млекопитающих. [14]
Ссылки [ править ]
- ^ Blei (II) -оксид . Merck
- ^ «Свинцовые соединения (как Pb)» . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ a b Карр, Додд С. (2005). «Свинцовые соединения». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a15_249 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.[ требуется страница ]
- «Термический и рентгеновский анализ египетского галенита». Журнал термического анализа и калориметрии . 86 (2): 393–401. DOI : 10.1007 / s10973-005-6785-6 . S2CID 96393940 .
- ^ Lead Processing @ Universalium.academic.ru . Альтернативный адрес: Обработка лидов @ Enwiki.net .
- ^ Уэллс, AF (1984), Структурная неорганическая химия (5-е изд.), Оксфорд: Clarendon Press, ISBN 0-19-855370-6[ требуется страница ]
- ^ Простой пример приведен в Anil Kumar De (2007). «§9.2.6 Свинец (Pb): оксид свинца PbO» . Учебник неорганической химии . Нью Эйдж Интернэшнл. п. 383. ISBN. 978-81-224-1384-7.Более сложный пример - у Турова, Нью-Йорк (2002). «§9.4 Алкоксиды германия, олова, свинца» . Химия алкоксидов металлов . Springer. п. 115. ISBN 978-0-7923-7521-0.
- ^ Роу, Дэвид Джон (1983). Ведущее производство в Великобритании: история . Крум Шлем. п. 16. ISBN 978-0-7099-2250-6.
- ^ Холлеман, Арнольд Фредерик; Виберг, Эгон (2001), Виберг, Нильс (ред.), Неорганическая химия , перевод Иглсона, Мэри; Брюэр, Уильям, Сан-Диего / Берлин: Academic Press / De Gruyter, ISBN 0-12-352651-5[ требуется страница ]
- ↑ Глава 9 «Соединения свинца» в книге « Керамические и стеклянные материалы: структура, свойства и обработка» , опубликованной Springer в 2008 году.
- ^ Сазерленд, Чарльз А .; Милнер, Эдвард Ф .; Керби, Роберт С .; Тейндл, Герберт; Мелин, Альберт; Болт, Герман М. «Свинец». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a15_193.pub2 .
- ^ Корсон, BB (1936). «1,4-Дифенилбутадиен» . Органический синтез . 16 : 28.; Сборник , 2 , стр. 229
- ^ "Оксид свинца (II)" . Международный информационный центр по безопасности и гигиене труда. Проверено 6 июня 2009 .
Внешние ссылки [ править ]
- Примеры из практики экологической медицины - токсичность свинца
- ToxFAQ: Ведущий
- Национальный реестр загрязнителей - Свинец и сведения о свинцовых соединениях
- Webelements PbO