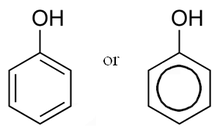
В биохимии , встречающиеся в природе фенолов относится к фенолу функциональной группы , которая найдена в натуральных продуктах . [1] [2] [3] Фенольные соединения производятся растениями и микроорганизмами. [4] Организмы иногда синтезируют фенольные соединения в ответ на экологическое давление, такое как нападение патогенов и насекомых, УФ-излучение и ранения. [5] Поскольку они присутствуют в продуктах питания, потребляемых в рационе человека, и в растениях, используемых в традиционной медицине нескольких культур, их роль в здоровье человека и болезнях является предметом исследований. [1] [5] [6] [7] :104 Некоторые фенолы обладают бактерицидным действием и используются при приготовлении дезинфицирующих средств.
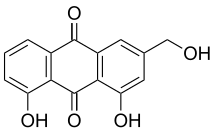
Классификация [ править ]
Могут применяться различные схемы классификации . [8] : 2 Обычно используемая схема основана на количестве атомов углерода и была разработана Джеффри Харборном и Симмондсом в 1964 году и опубликована в 1980 году: [8] : 2 [9]
| Количество атомов углерода | Базовый скелет | Количество фенольных циклов | Учебный класс | Примеры |
|---|---|---|---|---|
| 6 | С 6 | 1 | Простые фенолы, бензохиноны | Катехол, гидрохинон, 2,6-диметоксибензохинон |
| 7 | С 6 -С 1 | 1 | Фенольные кислоты , фенольные альдегиды | Галловая, салициловая кислоты |
| 8 | С 6 -С 2 | 1 | Ацетофеноны , производные тирозина, фенилуксусные кислоты | 3-ацетил-6-метоксибензальдегид , тирозол , п-гидроксифенилуксусная кислота , гомогентизиновая кислота |
| 9 | С 6 -С 3 | 1 | Гидроксикоричные кислоты , фенилпропены , кумарины , изокумарины , хромоны | Кофейная, феруловая кислоты, миристицин, эвгенол , умбеллиферон , эскулетин, бергенон , евгенин |
| 10 | С 6 -С 4 | 1 | Нафтохиноны | Юглоне, Плумбагин |
| 13 | С 6 -С 1 -С 6 | 2 | Ксантоноиды | Мангиферин |
| 14 | С 6 -С 2 -С 6 | 2 | Стилбеноиды , антрахиноны | Ресвератрол, Эмодин |
| 15 | С 6 -С 3 -С 6 | 2 | Халконоиды , флавоноиды , изофлавоноиды, неофлавоноиды | Кверцетин, цианидин, генистеин |
| 16 | С 6 -С 4 -С 6 | 2 | Галогенированные фенольные соединения водорослей | Кавиол А , кольпол |
| 18 | (С 6 -С 3 ) 2 | 2 | Лигнаны , неолигнаны | Пинорезинол, Эусидерин |
| 30 | (С 6 -С 3 -С 6 ) 2 | 4 | Бифлавоноиды | Аментофлавон |
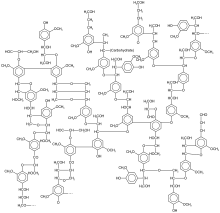
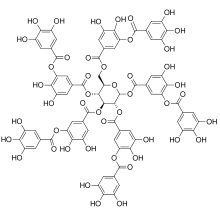
| много | (C 6 -C 3 ) n , (C 6 ) n , (C 6 -C 3 -C 6 ) n | n> 12 | Лигнины , катехоловые меланины , флаволаны ( конденсированные танины ), полифенольные белки , полифенолы | Малиновый эллагитаннин , Дубильная кислота |
В эту классификацию Харборна не входят диарилгептаноиды C 6 -C 7 -C 6 .
Их также можно классифицировать по количеству фенольных групп. Поэтому их можно назвать простыми фенолами или монофенолами с одной фенольной группой или ди ( би ), три- и олигофенолами с двумя, тремя или несколькими фенольными группами соответственно.
Разнообразное семейство природных фенолов - это флавоноиды , которые включают несколько тысяч соединений, среди которых флавонолы , флавоны , флаван-3ол ( катехины ), флаваноны , антоцианидины и изофлавоноиды . [10]
Фенольная единица может быть димеризована или подвергнута дальнейшей полимеризации, создавая новый класс полифенолов. Например, эллаговая кислота представляет собой димер галловой кислоты и образует класс эллагитаннинов, или катехин и галлокатехин могут объединяться с образованием красного соединения теафлавин , процесс, который также приводит к большому классу коричневых теарубигинов в чае.
Два природных фенола из двух разных категорий, например флавоноид и лигнан, могут объединяться, образуя гибридный класс, такой как флавонолигнаны .
Номенклатура полимеров :
| Базовый блок: | |||
|---|---|---|---|
| Класс / Полимер: | Гидролизуемые танины | Флавоноиды , конденсированные танины |
Гибридные химические классы [ править ]
Растения рода Humulus и Cannabis производят метаболиты терпенофенолов, соединения, которые являются меротерпенами . [11] Фенольные липиды представляют собой длинные алифатические цепи, связанные с фенольным фрагментом.
Хиральность [ править ]
Многие природные фенолы хиральны . Примером таких молекул является катехин . Кавикулярин - необычный макроцикл, потому что он был первым соединением, изолированным от природы, проявляющим оптическую активность из-за наличия плоской хиральности и аксиальной хиральности .
УФ видимое поглощение [ править ]
Природные фенолы обладают оптическими свойствами, характерными для бензола, например поглощением около 270 нм. Согласно правилам Вудворда , батохромные сдвиги также часто происходят, что указывает на присутствие делокализованных π-электронов, возникающих в результате сопряжения между бензольными и виниловыми группами. [12]
Поскольку молекулы с более высокими уровнями сопряжения подвергаются этому явлению батохромного сдвига, часть видимого спектра поглощается. Длины волн, оставшиеся в процессе (как правило, в красной части спектра), изменяют цвет конкретного вещества. Ацилирование антоцианидинов коричными кислотами приводило к смещению цветовой тональности ( угол оттенка CIE Lab ) на пурпурный . [13]
Вот серия УФ- видимых спектров молекул, классифицированных слева направо в зависимости от уровня их сопряжения:
УФ-видимый спектр галловой кислоты с макс. Лямбда около 270 нм. | УФ-видимый спектр феруловой кислоты с лямбда макс при 321 и плечом при 278 нм. | УФ-видимый спектр кверцетина с лямбда макс при 369 нм. | УФ-видимый спектр цианидин-3-O-глюкозида (хризантемина) с лямбда макс при 518 нм. |
Химическая структура галловой кислоты , фенольной кислоты. | Химическая структура феруловой кислоты , гидроксикоричной кислоты. | Химическая структура кверцетина , флавонола. | Химическая структура цианидина , антоцианидина. |
Характер поглощения, ответственный за красный цвет антоцианов, может быть дополнительным к таковому у зеленого хлорофилла в фотосинтетически активных тканях, таких как молодые листья Quercus coccifera . [14]
Окисление [ править ]
Природные фенолы являются реактивными по отношению к окислению соединениями , особенно сложная смесь фенолов, содержащаяся, например, в пищевых продуктах, может подвергаться самоокислению в процессе старения. Простые природные фенолы могут приводить к образованию процианидинов B-типа в винах [15] или в модельных растворах. [16] [17] Это связано с неферментативным потемнением цвета, характерным для этого процесса. [18] Это явление можно наблюдать в таких продуктах, как морковное пюре. [19]
Браунинг, связанный с окислением фенольных соединений, также считается причиной гибели клеток каллусов, образующихся в культурах in vitro . Эти фенольные соединения происходят как из тканей эксплантата, так и из его секрета.
Фенольные соединения [ править ]
Естественно [ править ]
| Каннабиноиды | активные компоненты каннабиса |
| Капсаицин | острый состав перца чили |
| Карвакрол | содержится, например, в орегано ; антимикробное и нейропротекторное [20] |
| Крезол | содержится в каменноугольной смоле и креозоте |
| Эстрадиол | эстроген - гормоны |
| Эвгенол | основной составной частью эфирного масла из гвоздики |
| Галловая кислота | найдено в галлах |
| Guaiacol | (2-метоксифенол) - имеет аромат дыма , содержится в жареном кофе , виски и дыме. |
| Метил салицилат | основной компонент эфирного масла грушанки |
| Малиновый кетон | состав с интенсивным запахом малины |
| Салициловая кислота | соединение-предшественник аспирина (в производстве используется химический синтез) |
| Серотонин / дофамин / адреналин / норадреналин | естественные нейротрансмиттеры |
| Тимол | (2-изопропил-5-метилфенол) - содержится в тимьяне ; антисептик , который используется в жидкости для полоскания рта |
| Тирозин | аминокислота |
| Сезамол | встречающееся в природе соединение, содержащееся в семенах кунжута |
Синтетический [ править ]
| Фенол | исходное соединение, используемое в качестве дезинфицирующего средства и для химического синтеза |
| Бисфенол А | и другие бисфенолы, полученные из кетонов и фенола / крезола |
| BHT | (бутилированный гидрокситолуол) - жирорастворимый антиоксидант и пищевая добавка |
| 4-нонилфенол | продукт распада моющих средств и ноноксинола-9 |
| Ортофенил фенол | фунгицид используется для депиляции цитрусовых |
| Пикриновая кислота | (тринитрофенол) - взрывчатое вещество |
| Фенолфталеин | индикатор pH |
| Ксиленол | используется в антисептических и дезинфицирующих средствах |
Биосинтез [ править ]
Фенольные соединения образуются тремя различными путями биосинтеза: (i) путем шикимат / хоризмат или сукцинилбензоат, который производит производные фенилпропаноидов (C6 – C3); (ii) ацетат / малонатный или поликетидный путь, который продуцирует фенилпропаноиды с удлиненными боковыми цепями, включая большую группу флавоноидов (C6 – C3 – C6) и некоторые хиноны; и (iii) ацетатно-мевалонатный путь, который дает ароматические терпеноиды, в основном монотерпены, путем реакций дегидрирования. [21] [22] Ароматическая аминокислота фенилаланин , синтезируемая путем метаболизма шикимовой кислоты , является обычным предшественником фенола, содержащего аминокислоты и фенольные соединения.
У растений фенольные звенья этерифицируются или метилируются и подвергаются конъюгации , что означает, что природные фенолы в основном находятся в гликозидной форме, а не в форме агликона .
В оливковом масле тирозол образует сложные эфиры с жирными кислотами. [23] В ржи алкилрезорцины представляют собой фенольные липиды.
В некоторых процессах ацетилирования участвуют терпены, такие как гераниол . [24] Эти молекулы называются меротерпенами (химическое соединение, имеющее частичную терпеноидную структуру).
Метилирование может происходить путем образования простой эфирной связи на гидроксильных группах с образованием O-метилированных полифенолов. В случае тангеритина O-метилированного флавона все пять гидроксилов метилированы, не оставляя свободных гидроксилов фенольной группы. Метилирование также может происходить непосредственно на атоме углерода бензольного кольца, как в случае пориола , C-метилированного флавоноида .
Биоразложение [ править ]
Грибок белой гнили Phanerochaete chrysosporium может удалять до 80% фенольных соединений из сточных вод коксования . [25]
Приложения [ править ]
Танины используются в кожевенной промышленности.
Некоторые природные фенолы можно использовать в качестве биопестицидов . Furanoflavonoids как karanjin или rotenoids используются в качестве акарицидов или инсектицидов . [26]
Энологические танины - важные элементы вкуса вина. [27]
Некоторые фенолы продаются в виде пищевых добавок . Фенолы исследовались как лекарства. Например, Crofelemer (USAN, торговое название Fulyzaq) - это разрабатываемый препарат для лечения диареи, связанной с лекарствами против ВИЧ. Кроме того, были изготовлены производные фенольного соединения комбретастатин А-4 , противораковой молекулы, включающей атомы азота или галогенов, для повышения эффективности лечения. [28]
Промышленная переработка и анализ [ править ]
Извлечение фенола [ править ]
Экстракция фенола - это технология обработки, используемая для получения фенолов в качестве сырья, соединений или добавок для промышленной обработки древесины и для химической промышленности.
Экстракцию можно проводить с использованием разных растворителей. Существует риск того, что полифенолоксидаза (PPO) ухудшает содержание фенолов в образце, поэтому необходимо использовать ингибиторы PPO, такие как дитионит калия (K 2 S 2 O 4 ), или проводить эксперимент с использованием жидкого азота или кипятить образец для несколько секунд ( бланширование ), чтобы инактивировать фермент. Дальнейшее фракционирование экстракта может быть достигнуто с использованием колонок для твердофазной экстракции и может привести к выделению отдельных соединений.
Извлечение природных фенолов из остатков биомассы является частью биоочистки . [29]
Разделение [ править ]
pK a фенольных соединений можно рассчитать по времени удерживания в жидкостной хроматографии . [30] [31]
Аналитические методы [ править ]
В исследованиях по оценке антиоксидантной способности могут использоваться электрохимические методы. [32]
Обнаружение может быть выполнено с помощью рекомбинантных люминесцентных бактериальных сенсоров . [33]
Профилирование [ править ]
Фенольное профилирование может быть достигнуто с помощью жидкостной хроматографии-масс-спектрометрии (ЖХ / МС). [34]
Количественная оценка [ править ]
Метод количественного определения содержания фенола - это объемное титрование . Окислитель, перманганат , используется для окисления стандартных концентраций стандартных растворов с получением стандартной кривой . Затем содержание неизвестных фенолов выражается в эквиваленте соответствующего стандарта.
Некоторые методы количественного определения общего содержания фенолов основаны на колориметрических измерениях. Общее количество фенолов (или антиоксидантный эффект) можно измерить с помощью реакции Фолина-Чокальтеу . Результаты обычно выражаются в эквивалентах галловой кислоты (GAE). Тест с хлоридом железа (FeCl 3 ) также является колориметрическим тестом .
Ламейсон и Карнет разработали тест для определения общего содержания флавоноидов в образце ( метод AlCI 3 ). После надлежащего смешивания образца и реагента смесь инкубируют в течение 10 минут при температуре окружающей среды и определяют оптическую плотность раствора при 440 нм. Содержание флавоноидов выражается в мг / г кверцетина. [35]
Результаты количественного анализа, полученные с помощью ВЭЖХ с диодной матрицей и детектором , обычно даются как относительные, а не абсолютные значения, поскольку отсутствуют коммерчески доступные стандарты для каждой фенольной молекулы. Этот метод также можно сочетать с масс-спектрометрией (например, HPLC – DAD – ESI / MS) для более точной идентификации молекул .
Оценка антиоксидантного эффекта [ править ]
- Измерения in vitro
Другие тесты измеряют антиоксидантную способность фракции. Некоторые делают использование 2,2'-азиной-бис (3-этилбензотиазолин-6-сульфоновый кислота) ( ABTS ) катион - радикал, который является реакционноспособным по отношению к большинству антиоксидантов , включая фенольные, тиолы и витамин С . [36] Во время этой реакции синий катион-радикал ABTS превращается обратно в свою бесцветную нейтральную форму. За реакцией можно следить спектрофотометрически. Этот анализ часто называют анализом антиоксидантной способности эквивалента Trolox (TEAC). Реакционная способность различных протестированных антиоксидантов сравнивается с реактивностью Тролокса , который является аналогом витамина Е.
Другие анализы антиоксидантной способности, в которых Trolox используется в качестве стандарта, включают дифенилпикрилгидразил (DPPH), емкость поглощения кислородных радикалов (ORAC), анализ способности плазмы к восстановлению железа (FRAP) или ингибирование катализируемого медью окисления липопротеинов низкой плотности человека in vitro . [37]
Также существует анализ клеточной антиоксидантной активности (CAA). Дихлорфлуоресцин - это зонд, который задерживается внутри клеток и легко окисляется до флуоресцентного дихлорфлуоресцеина (DCF). Метод измеряет способность соединений предотвращать образование DCF пероксильными радикалами, генерируемыми 2,2'-азобис (2-амидинопропан) дигидрохлоридом (ABAP), в клетках гепатокарциномы человека HepG2 . [38]
Другие методы включают бутилированный гидрокситолуол (BHT), бутилированный гидроксианизол (BHA), метод Rancimat (оценка прогоркания жира). [39]
- Модели in vivo
Личинки модельного животного Galleria mellonella , также называемые восковыми червями , могут быть использованы для проверки антиоксидантного действия отдельных молекул с использованием борной кислоты в пище для индукции индуцированного окислительного стресса. [40] Можно контролировать содержание малонового диальдегида , индикатор окислительного стресса, и активность антиоксидантных ферментов супероксиддисмутазы , каталазы , глутатион-S-трансферазы и глутатионпероксидазы . Про фенолоксидаза может также быть извлечена из насекомого. [41]
Генетический анализ [ править ]
Фенольные биосинтетические и метаболические пути и ферменты могут быть изучены с помощью трансгенеза генов. Arabidopsis , регулирующий ген для производства Антоцианина Пигмент 1 (AtPAP1) может быть выражен в других видах растений. [42]
Природные явления [ править ]
Фенолы встречаются в природе, особенно в растительном мире.
Встречи у прокариот [ править ]
Оробол содержится в Streptomyces neyagawaensis (актинобактерии). [ необходима цитата ] Фенольные соединения можно найти в цианобактериях Arthrospira maxima , используемых в пищевой добавке спирулина . [43] Три цианобактерии: Microcystis aeruginosa , Cylindrospermopsis raciborskii и Oscillatoria sp. являются предметом исследования естественного производства бутилированного гидрокситолуола (БГТ) [44] , антиоксиданта, пищевой добавки и промышленного химического вещества.
Proteobacterium Pseudomonas fluorescens продуцирует флороглюцин , флороглюцинкарбоновую кислоту и диацетилфлороглюцин . [45] Другой пример фенолов , полученных в протеобактерий является 3,5-дигидрокси-4-изопропил-транс-стильбена , бактериальный stilbenoid производится в Photorhabdus бактериальных симбионтов Heterorhabditis нематод.
Возникновение грибов [ править ]
Фенольные кислоты можно найти в грибах базидиомицетов . [46] Например, протокатеховая кислота и пирокатехол содержатся в Agaricus bisporus [47], а также в других фенилированных веществах, таких как фенилуксусная и фенилпировиноградная кислоты . Другие соединения , такие как atromentin и телефоровая кислота , также могут быть выделены из грибов в агарикомицете классе. Оробол , изофлавон , можно выделить из Aspergillus niger .
- в дрожжах
Ароматические спирты (например, тирозол ) производятся дрожжами Candida albicans . [48] Их также можно найти в пиве . [49] Эти молекулы являются соединениями, определяющими кворум для Saccharomyces cerevisiae . [50]
- Метаболизм
Дегидрогеназа арил-спирта использует ароматический спирт и NAD + для производства ароматического альдегида , NADH и H + .
Дегидрогеназа арил-спирта (НАДФ +) использует ароматический спирт и НАДФ + для производства ароматического альдегида , НАДФН и H + .
Арилдиалкилфосфатаза (также известная как фосфорорганическая гидролаза, фосфотриэстераза и параоксон гидролаза) использует арилдиалкилфосфат и H 2 O для производства диалкилфосфата и арилового спирта.
Встречи с лишайником [ править ]
Гирофорная кислота , депсид и орцинол содержатся в лишайниках . [51]
Встречаемость в водорослях [ править ]
Зеленая водоросль Botryococcus braunii является предметом исследований в естественное производство бутилгидрокситолуола (BHT), [44] антиоксидант, пищевая добавка и промышленные химическое вещества.
Фенольные кислоты , такие как протокатеховые , р-гидроксибензойный , 2,3-дигидроксибензойный , хлорогеновые , ванилиновые , кофейные , р -coumaric и салициловая кислота , коричная кислота и гидроксибензальдегиды , такие как п-гидроксибензальдегид , 3,4-дигидроксибензальдегид , ванилин , были выделен из in vitro культивирование пресноводной зеленой водоросли Spongiochloris spongiosa . [52]
Флоротанины , например эккол , содержатся в бурых водорослях . Валенолон содержится в тропической красной водоросле Vidalia sp . [53]
Встречается у наземных растений (эмбриофитов) [ править ]
Встречи в сосудистых растениях [ править ]
Фенольные соединения в основном содержатся в сосудистых растениях (трахеофиты), например, Lycopodiophyta [54] (ликоподы), Pteridophyta (папоротники и хвощ), покрытосеменные (цветущие растения или Magnoliophyta) и голосеменные [55] ( хвойные деревья , саговники , гинкго и Gnetales ). [ необходима цитата ]
В папоротниках такие соединения, как кемпферол и его глюкозид, могут быть выделены из метанольного экстракта листьев Phegopteris connectilis [56], или кемпферол-3-O-рутинозид , известный горький флавоноидный гликозид, может быть выделен из корневищ Selliguea. Fei . [57] Гипогалловую кислоту , кофейную кислоту , пеонифлорин и пикурозид можно выделить из пресноводного папоротника Salvinia molsta . [58]
У хвойных пород (Pinophyta) фенольные соединения хранятся в полифенольных клетках паренхимы , ткани, изобилующей флоэмой всех хвойных пород. [59]
Водные растения уруть колосистый производит эллагиевые , галловый и pyrogallic кислоты и (+) - катехин . [60]
Встречи в однодольных [ править ]
Алкилрезорцины можно найти в злаках. [ необходима цитата ]
2,4-Бис (4-гидроксибензил) фенол - это фенольное соединение, которое содержится в орхидеях Gastrodia elata и Galeola faberi . [ необходима цитата ]
Встречаемость у несосудистых растений [ править ]
Фенолы также можно найти в несосудистых наземных растениях ( мохообразных ). Dihydrostilbenoids и бис (bibenzyls) могут быть найдены в печеночников ( печёночные мхи ), к примеру, макроциклов cavicularin и riccardin С . Хотя лигнин отсутствует у мхов (Bryophyta) и роголистников (Anthocerotophyta), некоторые фенольные соединения можно найти в этих двух таксонах. [61] Например, розмариновая кислота и 3'-O-β-D-глюкозид розмариновой кислоты могут быть найдены в роголистнике Anthoceros agrestis . [62]
Встречи у других эукариот [ править ]
Встречи у насекомых [ править ]
Было показано, что отверждение белкового компонента кутикулы насекомых происходит из-за дубильного действия агента, образующегося при окислении фенольного вещества, образующего склеротин . [ необходимая цитата ] При аналогичном закаливании яйцеклетки таракана фенольное вещество представляет собой 3: 4-дигидроксибензойную кислоту ( протокатехиновую кислоту ). [63]
Ацетосирингон вырабатывается самцом листового клопа ( Leptoglossus phyllopus ) и используется в его системе коммуникации. [64] [65] [66] Гваякол производится в кишечнике пустынной саранчи , Schistocerca gregaria , при распаде растительного материала. Этот процесс осуществляется кишечной бактерией Pantoea agglomerans . [67] Гуаякол - один из основных компонентов феромонов, вызывающих скопление саранчи. [68] Орцинол был обнаружен в «токсичном клее» муравьев Camponotus saundersi . [ необходима цитата ] Rhynchophorus ferrugineus (красный пальмовый долгоносик) использует 2-метокси-4-винилфенол для передачи химических сигналов ( феромоны ). [69] Другие простые и сложные фенолы могут быть найдены у эусоциальных муравьев (таких как Crematogaster ) как компоненты яда. [70]
Встречи у млекопитающих [ править ]
У слонов-самок в образцах мочи были обнаружены два соединения: 3-этилфенол и 2-этил-4,5-диметилфенол . [71] Исследование секрета височных желез показало присутствие фенола , м-крезола и пара-крезола (4-метилфенол) во время сусла у самцов слонов . [72] [73] [74]
п-крезол и о-крезол также являются компонентами человеческого пота . [ необходима цитата ] P-крезол также является основным компонентом запаха свиней . [75]
4-этилфенол , 1,2-дигидроксибензол , 3-гидроксиацетофенон , 4-метил-1,2-дигидроксибензол , 4-метоксиацетофенон , 5-метоксисалициловая кислота , салицилальдегид и 3-гидроксибензойная кислота являются компонентами кастореума , экссудата касторового масла. мешочки зрелого североамериканского бобра ( Castor canadensis ) и европейского бобра ( Castor fiber ), используемые в парфюмерии. [76]
Роли [ править ]
В некоторых случаях природные фенолы присутствуют в вегетативной листве, чтобы препятствовать развитию травоядных , например, в случае западного ядовитого дуба . [77]
Роль в почвах [ править ]
В почвах , предполагаются , что большое количества фенолов освобождаются от разлагающейся растительной подстилки , а не из проникающих сквозь в любом естественном растительном сообществе. [ Править ] Разложение мертвого растительного материала вызывает сложные органические соединения , которые будут медленно окисленным лигнином -подобного гумусовым или распадаться на более простые формы (сахара и аминокислоты сахаров, алифатические и фенольные органические кислоты), которые далее превращаются в микробную биомассу (микробного гумус) или реорганизуются и далее окисляются в гуминовые ассоциации ( фульвокислоты и гуминовые кислоты), которые связываются с глинистыми минералами и гидроксидами металлов. [ необходима цитата ] О способности растений поглощать гуминовые вещества из корневой системы и метаболизировать их ведутся долгие споры. [ необходима цитата ] В настоящее время существует консенсус относительно того, как гумус играет гормональную роль, а не просто питательную роль в физиологии растений. [ необходима цитата ]
В почве растворимые фенолы сталкиваются с четырьмя разными судьбами. Они могут разлагаться и минерализоваться как источник углерода гетеротрофными микроорганизмами ; они могут превращаться в нерастворимые и трудно поддающиеся лечению гуминовые вещества реакциями полимеризации и конденсации (с участием почвенных организмов); они могут адсорбироваться на глинистых минералах или образовывать хелаты с ионами алюминия или железа; или они могут оставаться в растворенной форме, вымываться просачивающейся водой и, наконец, покидать экосистему как часть растворенного органического углерода (DOC). [4]
Выщелачивание - это процесс, при котором катионы, такие как железо (Fe) и алюминий (Al), а также органические вещества удаляются из подстилки и транспортируются вниз, в почву. Этот процесс известен как оподзоление и особенно интенсивен в бореальных лесах и лесах с прохладным умеренным климатом, которые в основном состоят из хвойных сосен, опада которых богата фенольными соединениями и фульвокислотой . [78]
Роль в выживании [ править ]
Фенольные соединения могут действовать как защитные агенты, ингибиторы, природные токсические вещества для животных и пестициды против вторгающихся организмов, то есть травоядных, нематод, насекомых-фитофагов, грибковых и бактериальных патогенов. Аромат и пигментация, присущие другим фенольным соединениям, могут привлекать симбиотических микробов, опылителей и животных, разносящих фрукты. [21]
Защита от хищников [ править ]
Летучие фенольные соединения содержатся в смоле растений, где они могут привлекать таких благодетелей, как паразитоиды или хищники травоядных, нападающих на растение. [79]
У водорослей Alaria marginata фенольные соединения действуют как химическая защита от травоядных. [80] В тропических видах Sargassum и Turbinaria , которые часто преимущественно потребляются травоядными рыбами и ехиноидами , наблюдается относительно низкий уровень фенольных соединений и дубильных веществ. [81] Морские аллелохимические вещества обычно присутствуют в большем количестве и разнообразии в тропических регионах, чем в регионах с умеренным климатом. Сообщается, что фенольные морские водоросли являются очевидным исключением из этой биогеографической тенденции. Высокие концентрации фенолов встречаются у видов бурых водорослей (отряды Dictyotales и Fucales).) как в умеренных, так и в тропических регионах, что указывает на то, что широта сама по себе не является разумным предиктором концентраций фенолов в растениях. [82]
Защита от инфекции [ править ]
В винограде культурный виноград, транс - ресвератрол является фитоалексином , выработанный против роста грибковых патогенов , таких как Botrytis сшегеа [83] и дельты-viniferin является еще виноградной лоза фитоалексин получает следующий грибковую инфекцию по Plasmopara viticola . [84] Пиносилвин - это преинфекционный стильбеноидный токсин (т.е. синтезированный до заражения), в отличие от фитоалексинов , которые синтезируются во время инфекции. Он присутствует в сердцевине из сосновых . [85]Это фунгитоксин, защищающий древесину от грибковой инфекции . [86]
Сакуранетин - это флаванон , разновидность флавоноидов. Его можно найти в Polymnia fruticosa [87] и рисе , где он действует как фитоалексин против прорастания спор Pyricularia oryzae . [88] В сорго , то SbF3'H2 ген, кодирующий в флавоноидов 3'-гидроксилазы , как представляется, выражается в патогена -специфические 3-deoxyanthocyanidin фитоалексины синтеза, [89] , например , в Sorghum- Colletotrichum взаимодействий. [90]
6-Methoxymellein является dihydroisocoumarin и фитоалексина , индуцированное в моркови ломтиками с помощью УФ-C , [91] , что позволяет устойчивость к Botrytis сшегеа [92] и других микроорганизмов . [93]
Даниэлон - это фитоалексин, содержащийся в плодах папайи . Это соединение показало высокую противогрибковую активность против Colletotrichum gloesporioides , патогенного гриба папайи. [94]
Стильбены производятся в Eucalyptus sideroxylon в случае атаки патогенов. Такие соединения могут быть связаны с гиперчувствительной реакцией растений. Высокий уровень фенольных соединений в некоторых лесах может объяснить их естественную защиту от гниения. [95]
В растениях VirA представляет собой протеин-гистидинкиназу, которая воспринимает определенные сахара и фенольные соединения. Эти соединения обычно обнаруживаются в поврежденных растениях, и в результате VirA используется Agrobacterium tumefaciens для определения местонахождения потенциальных организмов-хозяев для инфекции. [96]
Роль в аллелопатических взаимодействиях [ править ]
Природные фенолы могут участвовать в аллелопатических взаимодействиях, например, в почве [97] или в воде. Юглон является примером такой молекулы, подавляющей рост других видов растений вокруг ореховых деревьев. [ необходима цитата ] Водное сосудистое растение Myriophyllum spicatum производит эллаговую , галловую и пирогалловую кислоты и (+) - катехин , аллелопатические фенольные соединения, подавляющие рост сине-зеленой водоросли Microcystis aeruginosa . [60]
Фенолы, в частности флавоноиды и изофлавоноиды , могут участвовать в образовании эндомикоризы . [98]
Ацетосирингон был наиболее известен своим участием в распознавании патогенов растений [99], особенно своей ролью в качестве сигнала, привлекающего и трансформирующего уникальные онкогенные бактерии рода Agrobacterium . [ необходима цитата ] Ген virA на плазмиде Ti в геноме Agrobacterium tumefaciens и Agrobacterium rhizogenes используется этими почвенными бактериями для заражения растений посредством его кодирования рецептора ацетосирингона и других фенольных фитохимических веществ, выделяемых ранами растений. [100]Это соединение также обеспечивает более высокую эффективность трансформации растений в процедурах трансформации, опосредованных A. tumefaciens, и поэтому имеет важное значение в биотехнологии растений. [101]
Содержание в человеческой пище [ править ]
Известные источники природных фенолов в питании человека включают ягоды , чай , пиво , оливковое масло , шоколад или какао , кофе , гранаты , попкорн , йерба мате , фрукты и фруктовые напитки (включая сидр, вино и уксус ) и овощи . Травы и специи , орехи (грецкие орехи, арахис) и водоросли также потенциально важны для обеспечения некоторых природных фенолов.
Природные фенолы также можно найти в жирных матрицах, таких как оливковое масло . [102] Нефильтрованное оливковое масло имеет более высокий уровень фенолов или полярных фенолов, которые образуют сложный фенол-белковый комплекс.
Было показано, что фенольные соединения при использовании в напитках , таких как сливовый сок , улучшают цвет и чувствительность, например, уменьшают горечь . [103]
Некоторые сторонники органического земледелия утверждают, что выращенный органическим способом картофель , апельсины и листовые овощи содержат больше фенольных соединений, и они могут обеспечить антиоксидантную защиту от болезней сердца и рака . [104] Однако данных о существенных различиях между органическими продуктами питания и обычными продуктами питания недостаточно, чтобы утверждать, что органические продукты питания безопаснее или полезнее обычных продуктов питания. [105] [106]
Человеческий метаболизм [ править ]
У животных и людей после приема внутрь природные фенолы становятся частью метаболизма ксенобиотиков . В последующих реакциях фазы II эти активированные метаболиты конъюгированы с заряженными частицами, такими как глутатион , сульфат , глицин или глюкуроновая кислота . Эти реакции катализируются большой группой трансфераз с широкой специфичностью. UGT1A6 представляет собой ген человека, кодирующий фенол-UDP-глюкуронозилтрансферазу, активную по отношению к простым фенолам. [107] Фермент, кодируемый геном UGT1A8, обладает глюкуронидазной активностью со многими субстратами, включая кумарины , антрахиноны и флавоны.. [108]
Ссылки [ править ]
- ^ а б Ходдами, А; и другие. (2013). «Методика анализа фенольных соединений растений» . Молекулы . 18 (2): 2328–75. CiteSeerX 10.1.1.386.9960 . DOI : 10,3390 / молекулы18022328 . PMC 6270361 . PMID 23429347 .
- ^ Amorati, R; Валгимигли, Л. (2012). «Модуляция антиоксидантной активности фенолов нековалентными взаимодействиями». Org Biomol Chem . 10 (21): 4147–58. DOI : 10.1039 / c2ob25174d . PMID 22505046 .
- ^ Роббинс, Ребекка J (2003). «Фенольные кислоты в пищевых продуктах: обзор аналитической методологии» . Журнал сельскохозяйственной и пищевой химии . 51 (10): 2866–2887. DOI : 10.1021 / jf026182t . PMID 12720366 .
- ^ a b Hättenschwiler, Стефан; Витаусек, Питер М. (2000). «Роль полифенолов в круговороте питательных веществ наземных экосистем». Тенденции в экологии и эволюции . 15 (6): 238–243. DOI : 10.1016 / S0169-5347 (00) 01861-9 . PMID 10802549 .
- ^ a b Клепка, Дж; и другие. (2011). «Фенольные соединения как факторы, определяющие сорта и сорта в некоторых растительных продуктах» . Растительная еда Hum Nutr . 66 (1): 64–69. DOI : 10.1007 / s11130-010-0205-1 . PMC 3079089 . PMID 21243436 .
- ^ Мишра, BB; Тивари, ВК. (2011). «Натуральные продукты: развивающаяся роль в открытии новых лекарств». Eur J Med Chem . 46 (10): 4769–807. DOI : 10.1016 / j.ejmech.2011.07.057 . PMID 21889825 .
- ^ Роберт EC Wildman, редактор. Справочник по нутрицевтикам и функциональным продуктам питания, второе издание . CRC Press; 2 издание, 2006 г. ISBN 0849364094
- ^ a b Уилфред Вермеррис и Ральф Николсон. Биохимия фенольных соединений Springer, 2008 г.
- ^ Harborne, JB (1980). «Растительные фенолы». В Белле, EA; Чарлвуд, Б.В. (ред.). Энциклопедия физиологии растений, том 8 Вторичные растительные продукты . Берлин Гейдельберг Нью-Йорк: Springer-Verlag. С. 329–395.
- Перейти ↑ Jamison, Jennifer R. (2003). Клиническое руководство по питанию и диетическим добавкам в лечении заболеваний . п. 525. ISBN 978-0-443-07193-5.
- ^ Глава восемь: «Биосинтез terpenophenolic метаболитов хмеля и конопли». Джонатан Е. Пейдж и Яна Nagel, Последние достижения в фитохимии ., 2006, том 40, стр 179-210, DOI : 10.1016 / S0079-9920 (06) 80042-0
- ^ Jeandenis, J .; Pezet, R .; Табаччи, Р. (2006). «Экспресс-анализ стильбенов и производных листьев виноградной лозы, пораженных ложной мучнистой росой, методом жидкостной хроматографии - фотоионизационной масс-спектрометрии при атмосферном давлении». Журнал хроматографии A . 1112 (1–2): 263–8. DOI : 10.1016 / j.chroma.2006.01.060 . PMID 16458906 .
- ^ Стинцинг, ФК; Stintzing, AS; Carle, R .; Frei, B .; Wrolstad, RE (2002). «Цвет и антиоксидантные свойства антоциановых пигментов на основе цианидина». Журнал сельскохозяйственной и пищевой химии . 50 (21): 6172–6181. DOI : 10.1021 / jf0204811 . PMID 12358498 .
- ^ Karageorgou, P .; Манетас Ю. (2006). «Важность красного цвета в молодости: антоцианы и защита молодых листьев Quercus coccifera от травоядных насекомых и избытка света» . Физиология деревьев . 26 (5): 613–621. DOI : 10.1093 / treephys / 26.5.613 . PMID 16452075 .
- ^ "Тандемная масс-спектрометрия процианидинов B-типа в вине и дегидродикатехинов B-типа в смеси автоокисления (+) - катехина и (-) - эпикатехина". Вейксинг Сан, Миллер Джек М., Журнал масс-спектрометрии , 2003 г., том 38, номер 4, стр. 438–446, INIST : 14708334
- ^ Он, F .; Пан, QH; Shi, Y .; Чжан, XT; Дуань, CQ (2009). «Идентификация олигомеров автоокисления флаван-3-олов в модельных растворах методом HPLC-MS / MS» . Журнал масс-спектрометрии . 44 (5): 633–640. Bibcode : 2009JMSp ... 44..633H . DOI : 10.1002 / jms.1536 . PMID 19053150 .
- ^ Cilliers, JJL; Синглтон, ВЛ (1989). «Неферментные автоокислительные реакции фенольного потемнения в модельной системе кофейной кислоты». Журнал сельскохозяйственной и пищевой химии . 37 (4): 890–896. DOI : 10.1021 / jf00088a013 .
- ^ "Неферментативные аутоокислительные реакции кофейной кислоты в вине". Johannes JL Cilliers и Vernon L. Singleton, Am. J. Enol. Витич. , 1990, 41: 1, с. 84–86, ( аннотация )
- ^ Talcott, ST; Ховард, Л. Р. (1999). «Фенольное самоокисление несет ответственность за ухудшение цвета обработанного морковного пюре». Журнал сельскохозяйственной и пищевой химии . 47 (5): 2109–2115. DOI : 10.1021 / jf981134n . PMID 10552504 .
- ^ «Карвакрол, пищевая добавка, обеспечивает нейропротекцию при очаговой церебральной ишемии / реперфузионной травме у мышей» , Yu et al. 2012 [1]
- ^ а б Бхаттачарья, А; и другие. (2010). «Обзор: роль фенольных соединений растений в защите и коммуникации при заражении Agrobacterium и Rhizobium» . Мол Растение Патол . 11 (5): 705–19. DOI : 10.1111 / j.1364-3703.2010.00625.x . PMC 6640454 . PMID 20696007 .
- ^ Knaggs, Эндрю Р. (2001). «Биосинтез метаболитов шикимата (1999)». Отчеты о натуральных продуктах . 18 (3): 334–55. DOI : 10.1039 / b001717p . PMID 11476485 .
- ^ Лукас, Рикардо; Комель, Франсиско; Алькантара, Давид; Мальдонадо, Оливия С .; Куркуроз, Мелани; Parra, Jose L .; Моралес, Хуан К. (2010). «Поверхностно-активные свойства липофильных антиоксидантов Тирозол и гидрокситирозол и сложные эфиры жирных кислот: возможное объяснение нелинейной гипотезы антиоксидантной активности в эмульсиях масло-в-воде». Журнал сельскохозяйственной и пищевой химии . 58 (13): 8021–6. DOI : 10.1021 / jf1009928 . PMID 20524658 .
- ^ Шмейкал, Карел; Грыцова, Ленка; Марек, Радек; Лемьер, Филип; Янковска, Дагмар; Forejtníková, Hana; Ванко, Ян; Сухи, Вацлав (2007). «C-гераниловые соединения из плодов Paulownia tomentosa ». Журнал натуральных продуктов . 70 (8): 1244–8. DOI : 10.1021 / np070063w . PMID 17625893 .
- ^ Лу Y; Ян Л; Ван Ю; Чжоу С; Fu J; Чжан Дж. (Июнь 2009 г.). «Биоразложение фенольных соединений из сточных вод коксования иммобилизованным грибком белой гнили Phanerochaete chrysosporium». Журнал опасных материалов . 165 (1–3): 1091–7. DOI : 10.1016 / j.jhazmat.2008.10.091 . PMID 19062164 .
- ^ Perumalsamy, Haribalan; Чан, Мён Джин; Ким, Джун-Ран; Кадаркарай, Муруган; Ан, Ён-Джун (2015). «Ларвицидная активность и возможный механизм действия четырех флавоноидов и двух жирных кислот, идентифицированных в семенах Millettia pinnata, по отношению к трем видам комаров» . Паразиты и переносчики . 8 (1): 237. DOI : 10,1186 / s13071-015-0848-8 . ISSN 1756-3305 . PMC 4410478 . PMID 25928224 .
- ↑ Рыночный потенциал инноваций, связанных с танинами, в винодельческой промышленности, Меган Хилл и Джефф Кейн, Департамент первичной промышленности штата Виктория, 2007 г.
- ^ Карр, Мириам; Грин, Лиза М .; Нокс, Эндрю Дж. С.; Ллойд, Дэвид Дж .; Zisterer, Daniela M .; Миган, Мэри Дж. (2010). «Провести идентификацию конформационно ограниченных аналогов комбретастатина β-лактамного типа: синтез, антипролиферативная активность и таргетные эффекты тубулина». Европейский журнал медицинской химии . 45 (12): 5752–5766. DOI : 10.1016 / j.ejmech.2010.09.033 . PMID 20933304 .
- ^ Вильяверде, JJ; Де Вега, А .; Ligero, P .; Фрейре, CSR; Нето, КП; Сильвестр, AJD (2010). "Фракционирование органосольв коры мискантуса x giganteus: судьба липофильных компонентов и образование ценных фенольных побочных продуктов". Журнал сельскохозяйственной и пищевой химии . 58 (14): 8279–8285. DOI : 10.1021 / jf101174x . PMID 20593898 .
- ^ Hanai, T .; Коидзуми, К .; Киношита, Т .; Arora, R .; Ахмед, Ф. (1997). «Прогнозирование значений pK a фенольных и азотсодержащих соединений с помощью компьютерно-химического анализа по сравнению с результатами, измеренными с помощью жидкостной хроматографии». Журнал хроматографии A . 762 (1–2): 55–61. DOI : 10.1016 / S0021-9673 (96) 01009-6 . PMID 9098965 .
- Перейти ↑ Beltran, J. (2003). «Спектрофотометрические, потенциометрические и хроматографические значения pK a полифенольных кислот в воде и ацетонитрил-водной среде». Analytica Chimica Acta . 484 (2): 253–264. DOI : 10.1016 / S0003-2670 (03) 00334-9 .
- ^ Рене, Алиса; Абаск, Мари-Лоуренс; Хаушар, Дидье; Хапио, Филипп (2010). «Как фенольные соединения реагируют на ион супероксида? Простой электрохимический метод оценки антиоксидантной способности». Аналитическая химия . 82 (20): 8703–10. DOI : 10.1021 / ac101854w . PMID 20866027 .
- ^ Leedjarv, A .; Ivask, A .; Вирта, М .; Кахру, А. (2006). «Анализ биодоступных фенолов из природных образцов с помощью рекомбинантных люминесцентных бактериальных сенсоров». Chemosphere . 64 (11): 1910–9. Bibcode : 2006Chmsp..64.1910L . DOI : 10.1016 / j.chemosphere.2006.01.026 . PMID 16581105 .
- ^ Stobiecki, M .; Skirycz, A .; Kerhoas, L .; Kachlicki, P .; Muth, D .; Einhorn, J .; Мюллер-Робер, Б. (2006). «Профилирование фенольных гликозидных конъюгатов в листьях Arabidopsis thaliana с использованием ЖХ / МС». Метаболомика . 2 (4): 197–219. DOI : 10.1007 / s11306-006-0031-5 . S2CID 39140266 .
- ^ "Teneurs en Principaux flavonoides des fleurs de Cratageus monogyna Jacq et de Cratageus Laevigata (Poiret DC) en Fonction de la Vegetation ". JL Lamaison и A. Carnet, Plantes Medicinales Phytotherapie , 1991, XXV, страницы 12–16.
- ^ Уокер, Ричард Б .; Эверетт, Джейс Д. (2009). «Сравнительная скорость реакции различных антиоксидантов с радикальным катионом ABTS». Журнал сельскохозяйственной и пищевой химии . 57 (4): 1156–61. DOI : 10.1021 / jf8026765 . PMID 19199590 .
- ^ Мейер, Энн S .; Йи, Ок-Сук; Пирсон, Дебра А .; Уотерхаус, Эндрю Л .; Франкель, Эдвин Н. (1997). «Ингибирование окисления липопротеинов низкой плотности человека в отношении состава фенольных антиоксидантов в винограде ( Vitis vinifera )». Журнал сельскохозяйственной и пищевой химии . 45 (5): 1638–1643. DOI : 10.1021 / jf960721a .
- ^ Wolfe, KL; Лю, Р.Х. (2007). «Анализ клеточной антиоксидантной активности (CAA) для оценки антиоксидантов, продуктов питания и пищевых добавок». Журнал сельскохозяйственной и пищевой химии . 55 (22): 8896–8907. DOI : 10.1021 / jf0715166 . PMID 17902627 .
- ^ Астрид; фон Гадоу, Элизабет Жубер; Хансманн, Крис Ф. (1997). «Сравнение антиоксидантной активности аспалатина с другими растительными фенолами чая ройбуш (Aspalathus linearis), α-токоферола, BHT и BHA». J. Agric. Food Chem . 45 (3): 632–638. DOI : 10.1021 / jf960281n .
- ^ Гиршл, Павел; Бююкгюзель, Эндер; Бююкгюзель, Кемаль (2007). «Влияние окислительного стресса, вызванного борной кислотой, на антиоксидантные ферменты и выживаемость в Galleria mellonella». Архивы биохимии и физиологии насекомых . 66 (1): 23–31. DOI : 10.1002 / arch.20194 . PMID 17694562 .
- ^ Копачек, Петр; Вайзе, Кристоф; Гётц, Питер (1995). «Пропенолоксидаза восковой моли Galleria mellonella: очистка и характеристика профермента». Биохимия и молекулярная биология насекомых . 25 (10): 1081–1091. DOI : 10.1016 / 0965-1748 (95) 00040-2 . PMID 8580908 .
- ^ Ли, Сян; Гао, Мин-Цзюнь; Пан, Хун-Ю; Цуй, Де-Джун; Грубер, Маргарет Ю. (2010). «Пурпурный канола: ArabidopsisPAP1 увеличивает антиоксиданты и фенолы в листьях Brassica napus ». Журнал сельскохозяйственной и пищевой химии . 58 (3): 1639–45. DOI : 10.1021 / jf903527y . PMID 20073469 .
- ^ Производство фенольных соединений микроводорослями Spirulina maxima и их защитные эффекты in vitro в отношении модели гепатотоксичности . Абд Эль-Бакы Ханаа Х., Эль-Баз Фарук К. и Эль-Бароти Гамаль С., Достижения в области пищевых наук , 2009 г., том 31, номер 1, стр. 8–16, INIST : 21511068
- ^ а б Бабу Б .; Wu JT (декабрь 2008 г.). «Производство природного бутилированного гидрокситолуола в качестве антиоксиданта пресноводным фитопланктоном» (PDF) . Журнал психологии . 44 (6): 1447–1454. DOI : 10.1111 / j.1529-8817.2008.00596.x . PMID 27039859 . S2CID 26084768 .
- ^ Ачкар, Джихейн; Сиань, Мо; Чжао, Хуйминь; Фрост, JW (2005). «Биосинтез флороглюцина». Варенье. Chem. Soc . 127 (15): 5332–5333. DOI : 10.1021 / ja042340g . PMID 15826166 .
- ^ Баррос, Лилиан; Дуэньяс, Монтсеррат; Феррейра, Изабель CFR; Баптиста, Паула; Сантос-Буэльга, Селестино (2009). «Определение фенольных кислот с помощью ВЭЖХ – DAD – ESI / MS в шестнадцати различных португальских видах диких грибов». Пищевая и химическая токсикология . 47 (6): 1076–9. DOI : 10.1016 / j.fct.2009.01.039 . PMID 19425182 .
- ^ Дельсиньор, А; Ромео, F; Джаччио, М. (1997). «Содержание фенольных веществ в базидиомицетах». Микологические исследования . 101 (5): 552–6. DOI : 10.1017 / S0953756296003206 .
- ^ Гош, Суман; Кебаара, Бесси В .; Аткин, Одри Л .; Никерсон, Кеннет В. (2008). «Регулирование производства ароматического спирта у Candida albicans» . Прикладная и экологическая микробиология . 74 (23): 7211–7218. DOI : 10,1128 / AEM.01614-08 . PMC 2592902 . PMID 18836025 .
- ^ Szlavko, Клара М. (1973). «Тртптофол, тирозол и фенилэтанол - ароматические высшие спирты в пиве». Журнал Института пивоварения . 79 (4): 283–288. DOI : 10.1002 / j.2050-0416.1973.tb03541.x .
- ^ Хоган, Дебора А. (2006). «Чувство кворума: алкоголь в социальной ситуации». Текущая биология . 16 (12): R457 – R458. DOI : 10.1016 / j.cub.2006.05.035 . PMID 16782000 . S2CID 3970864 .
- ^ Робике (1829). "Essai analytique des lichens de l'orseille". Анналы химии и тела . 42 : 236–257.
- ^ Onofrejová, L .; Vašíčková, J .; Клейдус, Б .; Stratil, P .; Mišurcová, L .; Kráčmar, S .; Kopecký, J .; Вацек, Дж. (2010). «Биоактивные фенолы в водорослях: применение методов жидкостной и твердофазной экстракции под давлением». Журнал фармацевтического и биомедицинского анализа . 51 (2): 464–470. DOI : 10.1016 / j.jpba.2009.03.027 . PMID 19410410 .
- ^ Йу, HD; Ketchum, SO; Франция, Д .; Bair, K .; Гервик, WH (2002). «Валенолон, новый фенольный метаболит из тропических красных водорослей AlgaVidaliasp». Журнал натуральных продуктов . 65 (1): 51–53. DOI : 10.1021 / np010319c . PMID 11809064 .
- ^ Педерсен, JA; Олльгаард Б. (1982). «Фенольные кислоты рода Lycopodium». Биохимическая систематика и экология . 10 : 3–9. DOI : 10.1016 / 0305-1978 (82) 90044-8 .
- ^ Карначан, SM; Харрис, П.Дж. (2000). «Феруловая кислота связана с первичными клеточными стенками всех семейств голосеменных». Биохимическая систематика и экология . 28 (9): 865–879. DOI : 10.1016 / S0305-1978 (00) 00009-0 . PMID 10913848 .
- ^ Адам, КП (1999). «Фенольные составляющие папоротника Phegopteris connectilis». Фитохимия . 52 (5): 929–934. DOI : 10.1016 / S0031-9422 (99) 00326-X .
- ^ Флавоноиды и проантроцианидин из корневищ Selliguea feei. Пэк Нам-Ин, Кеннелли Э.Дж., Кардоно Л.Б.С., Цаури С., Падмавината К., Соеджарто Д.Д. и Кингхорн А.Д., Фитохимия , 1994, т. 36, нет. 2. С. 513–518, INIST : 3300075.
- ^ Чоудхари, Мичиган; Naheed, N .; Abbaskhan, A .; Musharraf, SG; Siddiqui, H .; Атта-Ур-Рахман (2008). «Фенольные и другие составляющие пресноводного папоротника Salvinia molsta». Фитохимия . 69 (4): 1018–1023. DOI : 10.1016 / j.phytochem.2007.10.028 . PMID 18177906 .
- ^ Krokene, P .; Надь, NE; Креклинг, Т. (2008). «Протоки травматической смолы и полифенольные клетки паренхимы у хвойных растений». Индуцированная устойчивость растений к травоядным . п. 147. DOI : 10.1007 / 978-1-4020-8182-8_7 . ISBN 978-1-4020-8181-1.
- ^ a b Накай, С. (2000). «Выделяемые Myriophyllum spicatum аллелопатические полифенолы, подавляющие рост сине-зеленых водорослей Microcystis aeruginosa». Исследования воды . 34 (11): 3026–3032. DOI : 10.1016 / S0043-1354 (00) 00039-7 .
- ^ Эриксон, М .; Микше, Г.Е. (1974). «О наличии лигнина или полифенолов в некоторых мхах и печеночниках». Фитохимия . 13 (10): 2295–2299. DOI : 10.1016 / 0031-9422 (74) 85042-9 .
- ^ Vogelsang, K .; Schneider, B .; Петерсен, М. (2005). «Производство розмариновой кислоты и нового 3'-O-β-D-глюкозида розмариновой кислоты в суспензионных культурах роголистника Anthoceros agrestis Paton». Planta . 223 (2): 369–373. DOI : 10.1007 / s00425-005-0089-8 . PMID 16133208 . S2CID 29302603 .
- ^ Hackman, RH; Прайор, MG; Тодд, AR (1948). «Встречаемость фенольных веществ у членистоногих» . Биохимический журнал . 43 (3): 474–477. DOI : 10.1042 / bj0430474 . PMC 1274717 . PMID 16748434 .
- ^ Acetosyringone на www.pherobase.com, база данных по феромонам
- ^ Олдрич, младший; Blum, MS; Даффи, СС; Fales, HM (1976). «Специфические для мужчин натуральные продукты клопов Leptoglossus phyllopus: химия и возможные функции». Журнал физиологии насекомых . 22 (9): 1201–1206. DOI : 10.1016 / 0022-1910 (76) 90094-9 .
- ^ Олдрич, младший; Blum, MS; Fales, HM (1979). «Видовые природные продукты взрослых самцов листоногих клопов (Hemiptera: Heteroptera)». Журнал химической экологии . 5 : 53–62. DOI : 10.1007 / BF00987687 . S2CID 34346907 .
- ^ Диллон, RJ; Веннард, Коннектикут; Чарнли, AK (апрель 2002 г.). «Примечание: кишечные бактерии производят компоненты феромона сращивания саранчи» . Журнал прикладной микробиологии . 92 (4): 759–763. DOI : 10.1046 / j.1365-2672.2002.01581.x . ISSN 1364-5072 . PMID 11966918 . S2CID 8561972 .
- ^ Диллон, Род Дж .; Веннард, Крис Т .; Чарнли, А. Кейт (2000). «Эксплуатация кишечных бактерий на саранче». Природа . 403 (6772): 851. DOI : 10.1038 / 35002669 . PMID 10706273 . S2CID 5207502 .
- ^ Семиохимический - 2-метокси-4-винилфенол , Pherobase.com
- ^ Marlier, J .; Quinet, Y .; Дебизо, Дж. (2004). «Защитное поведение и биологическая активность абдоминальной секреции у муравьев Crematogaster Scutellaris (Hymenoptera: Myrmicinae)» (PDF) . Поведенческие процессы . 67 (3): 427–40. DOI : 10.1016 / j.beproc.2004.07.003 . PMID 15518992 . S2CID 21599793 .
- ^ Запахи мочевых, височных желез и дыхания азиатских слонов в национальном парке Мудумалай. LEL Rasmussen и V. Krishnamurthy, Gajah, Journal of the Asian Elephant Specialist Group , январь 2001 г., номер 20, страницы 1-8 ( статья )
- ^ Расмуссен, LEL; Перрин Т. Е. (1999). «Физиологические корреляты Musth». Физиология и поведение . 67 (4): 539–49. DOI : 10.1016 / S0031-9384 (99) 00114-6 . PMID 10549891 . S2CID 21368454 .
- ^ "Musth в слонах". Дипа Анант,Печатный журнал зоопарка , 15 (5), стр. 259-262 ( статья заархивирована 4 июня 2018 г. в Wayback Machine )
- ^ Адамс, J .; Garcia, A .; Фут, CS (1978). «Некоторые химические составляющие секрета височной железы африканского слона (Loxodonta africana)». Журнал химической экологии . 4 : 17–25. DOI : 10.1007 / BF00988256 . S2CID 45857570 .
- ^ "Зачем изучать запах свиньи?" .
- ^ Müller-Schwarze, D .; Хулихан, П. У. (1991). «Феромонная активность отдельных составляющих кастореума у бобра, Castor canadensis». Журнал химической экологии . 17 (4): 715–34. DOI : 10.1007 / BF00994195 . PMID 24258917 . S2CID 29937875 .
- ^ C.Michael Hogan (2008) Западный ядовитый дуб: Toxicodendron diversilobum , GlobalTwitcher, ed. Никлас Стромберг "Архивная копия" . Архивировано из оригинала на 2009-07-21 . Проверено 21 июля 2009 .CS1 maint: заархивированная копия как заголовок ( ссылка )
- ^ Биогеохимия: анализ глобальных изменений . 2-е издание. Уильям Х. Шлезингер, Academic Press, 1997, 108, 135, 152–158, 180–183, 191–194
- ^ Смолы растений: химия, эволюция, экология и этноботаника , Джин Лангенхайм, Timber Press , Портленд, Орегон. 2003 г.
- Перейти ↑ Steinberg, PD (1984). «Химическая защита водорослей от травоядных: распределение фенольных соединений в водорослях Alaria marginata». Наука . 223 (4634): 405–407. Bibcode : 1984Sci ... 223..405S . DOI : 10.1126 / science.223.4634.405 . PMID 17829890 . S2CID 36409146 .
- Перейти ↑ Steinberg, PD (1986). «Химическая защита и восприимчивость тропических морских бурых водорослей к травоядным животным». Oecologia . 69 (4): 628–630. Bibcode : 1986Oecol..69..628S . DOI : 10.1007 / BF00410374 . PMID 28311627 . S2CID 19551247 .
- ^ Targett, Нэнси М .; Коэн, Лорен Д .; Boettcher, Anne A .; Таннер, Кристофер Э. (1992). «Биогеографические сравнения полифенолов морских водорослей: свидетельства против широтной тенденции». Oecologia . 89 (4): 464–470. Bibcode : 1992Oecol..89..464T . DOI : 10.1007 / BF00317150 . JSTOR 4219911 . PMID 28311874 . S2CID 5655010 .
- ^ Ф. Favaron, М. Lucchetta, С. Odorizzi, АТ Паиш да Кунья и Л. Селла (2009). «Роль полифенолов винограда на активность транс-ресвератрола против Botrytis cinerea и лакказы грибов на растворимость предполагаемых белков PR винограда» (PDF) . Журнал патологии растений . 91 (3): 579–588. doi : 10.4454 / jpp.v91i3.549 (неактивен 2021-01-14) . Проверено 22 января 2011 . CS1 maint: multiple names: authors list (link) CS1 maint: DOI inactive as of January 2021 (link)
- ^ Timperio, AM; d'Alessandro, A .; Fagioni, M .; Magro, P .; Золла, Л. (2012). «Производство фитоалексинов транс-ресвератрола и дельта-виниферина в двух экономически значимых сортах винограда при заражении Botrytis cinerea в полевых условиях». Физиология и биохимия растений . 50 (1): 65–71. DOI : 10.1016 / j.plaphy.2011.07.008 . PMID 21821423 .
- ^ Hovelstad, H .; Leirset, I .; Oyaas, K .; Фиксдал, А. (2006). "Скрининговые анализы пиносилвин-стильбенов, смоляных кислот и лигнанов в норвежских хвойных деревьях" . Молекулы . 11 (1): 103–114. DOI : 10.3390 / 11010103 . PMC 6148674 . PMID 17962750 .
- ^ Ли, СК; Ли, HJ; Мин, HY; Park, EJ; Ли, КМ; Ан, YH; Чо, YJ; Пай, JH (2005). «Антибактериальное и противогрибковое действие пиносильвина, входящего в состав сосны». Фитотерапия . 76 (2): 258–260. DOI : 10.1016 / j.fitote.2004.12.004 . PMID 15752644 .
- ^ "Сакуранетин" . home.ncifcrf.gov . Архивировано из оригинала на 2018-12-03 . Проверено 2 декабря 2018 .
- ^ Сакуранетин, флавононовый фитоалексин из листьев риса, облученных ультрафиолетом, Кодама О., Миякава Дж., Акацука Т. и Кийосава С., Фитохимия , 1992, том 31, номер 11, стр. 3807–3809, INIST : 4682303
- ^ Ши, C. -H .; Чу И.К .; Yip, WK; Ло, К. (2006). «Дифференциальная экспрессия двух кДНК флавоноидов 3'-гидроксилазы, участвующих в биосинтезе антоцианиновых пигментов и фитоалексинов 3-дезоксиантоцианидина в сорго» . Физиология растений и клеток . 47 (10): 1412–1419. DOI : 10.1093 / PCP / pcl003 . PMID 16943219 .
- ^ «Биосинтез и регулирование 3-deoxyanthocyanidin фитоалексины индуцированных во сорго - Colletotrichum взаимодействия: гетерологичной экспрессии в кукурузе». Чопра Surinder, Gaffoor Iffa, Ibraheem Farag, плакат на Американском обществе биологов растений ( аннотация архивной 2011-07-25 в Wayback Machine )
- ^ Мерсье, Дж .; Arul, J .; Ponnampalam, R .; Буле, М. (1993). «Индукция 6-метоксимеллеина и устойчивость к патогенам хранения в ломтиках моркови с помощью УФ-С». Журнал фитопатологии . 137 : 44–54. DOI : 10.1111 / j.1439-0434.1993.tb01324.x .
- ^ Hoffman, R .; Heale, JB (1987). «Гибель клеток, накопление 6-метоксимеллеина и индуцированная устойчивость к Botrytis cinerea в ломтиках корня моркови». Физиологическая и молекулярная патология растений . 30 : 67–75. DOI : 10.1016 / 0885-5765 (87) 90083-X .
- ^ Куросаки, Ф .; Ниши, А. (1983). «Выделение и антимикробная активность фитоалексина 6-метоксимеллеина из культивированных клеток моркови». Фитохимия . 22 (3): 669–672. DOI : 10.1016 / S0031-9422 (00) 86959-9 .
- ^ Danielone, фитоалексин из плодов папайи . Эчеверри Ф., Торрес Ф., Хинонес В., Кардона Г., Арчболд Р., Ролдан Дж., Брито И., Луис Дж. Г. и Лахлу У. Э.-Х., Phytochemistry , 1997, vol. 44, нет. 2. С. 255–256, INIST : 2558881.
- ^ Харт, Джон Х .; Хиллис, WE (1974). «Ингибирование древесных грибов стильбенами и другими полифенолами в Eucalyptus sideroxylon ». Фитопатология . 64 (7): 939–48. DOI : 10.1094 / Фито-64-939 .
- ^ Бренчич, Аня; Винанс, Стивен С. (март 2005 г.). «Обнаружение и ответ на сигналы, участвующие во взаимодействиях хозяина-микроба бактериями, ассоциированными с растениями» . Microbiol Mol Biol Rev . 69 (1): 155–194. DOI : 10.1128 / mmbr.69.1.155-194.2005 . PMC 1082791 . PMID 15755957 .
- ^ Блюм, Удо; Шафер, Стивен Р .; Леман, Мэри Э. (1999). «Доказательства ингибирующих аллелопатических взаимодействий с участием фенольных кислот в полевых почвах: концепции против экспериментальной модели». Критические обзоры в науках о растениях . 18 (5): 673–93. DOI : 10.1080 / 07352689991309441 .
- ^ Моранди, Д. (1996). «Возникновение фитоалексинов и фенольных соединений в эндомикоризных взаимодействиях и их потенциальная роль в биологическом контроле». Растение и почва . 185 (2): 241–305. DOI : 10.1007 / BF02257529 . S2CID 30091640 .
- ^ «Участие ацетосирингона в распознавании патогенов растений». Бейкер К. Джасин, Мок Нортон М., Уитакер Брюс Д., Робертс Дэниел П., Райс Клиффорд П., Деаль Кеннет Л. и Аверъянов Андрей А., Biochemical and Biophysical Research Communications , 2005, том 328, номер 1 , стр. 130–136, INIST : 16656426
- ^ Schrammeijer, B .; Beijersbergen, A .; Бездельник, КБ; Мельчерс, LS; Томпсон, Д.В.; Hooykaas, PJ (2000). «Анализ последовательности vir-области из плазмиды октопина Ti pTi15955 Agrobacterium tumefaciens» . Журнал экспериментальной ботаники . 51 (347): 1167–1169. DOI : 10.1093 / jexbot / 51.347.1167 . PMID 10948245 .
- ^ Шейхолеслам, СН; Уикс, Д.П. (1987). «Ацетосирингон способствует высокоэффективной трансформации эксплантатов Arabidopsis thaliana с помощью Agrobacterium tumefaciens». Молекулярная биология растений . 8 (4): 291–298. DOI : 10.1007 / BF00021308 . PMID 24301191 . S2CID 32005770 .
- ^ Gutfinger, Т. (1981). «Полифенолы в оливковом масле». Журнал Американского общества химиков-нефтяников . 58 (11): 966–8. DOI : 10.1007 / BF02659771 . S2CID 85367601 .
- ^ Донован, Дженнифер Л .; Мейер, Энн С .; Уотерхаус, Эндрю Л. (1998). «Фенольный состав и антиоксидантная активность чернослива и сока чернослива (Prunus domestica)». Журнал сельскохозяйственной и пищевой химии . 46 (4): 1247–1252. DOI : 10.1021 / jf970831x .
- ^ Асами, Дэнни К. «Сравнение общего содержания фенольной и аскорбиновой кислоты в лиофилизированных и сушеных на воздухе марионнике, клубнике и кукурузе, выращенных с использованием традиционных, органических и устойчивых методов ведения сельского хозяйства» . Журнал сельскохозяйственной и пищевой химии (Американское химическое общество), 51 (5), 1237–1241, 2003. 10.1021 / jf020635c S0021-8561 (02) 00635-0. Проверено 10 апреля 2006 года.
- ^ Смит-Спэнглер, C .; Брандо, М.Л . ; Хантер, GE; Bavinger, JC; Pearson, M .; Eschbach, PJ; Сундарам, V .; Liu, H .; Schirmer, P .; Stave, C .; Олькин, И .; Бравата, DM (4 сентября 2012 г.). «Являются ли органические продукты безопаснее или полезнее обычных альтернатив ?: систематический обзор» . Анналы внутренней медицины . 157 (5): 348–366. DOI : 10.7326 / 0003-4819-157-5-201209040-00007 . PMID 22944875 . S2CID 21463708 .
- ^ Блер, Роберт. (2012). Органическое производство и качество пищевых продуктов: практический анализ . Wiley-Blackwell, Оксфорд, Великобритания. ISBN 978-0-8138-1217-5
- ^ «Клонирование и субстратная специфичность человеческой фенольной глюкуронозилтрансферазы UDP, экспрессируемой в клетках COS-7». Дэвид Хардинг, Сильви Фурнель-Жигле, Майкл Р. Джексон и Брайан Берчелл, Proc. Natl. Акад. Sci. США , ноябрь 1988 г., том 85, стр. 8381–8385, ( аннотация )
- ^ Риттер JK; Chen F .; Sheen YY; Tran HM; Kimura S .; Yeatman MT; Оуэнс И.С. (март 1992 г.). «Новый сложный локус UGT1 кодирует человеческий билирубин, фенол и другие изоферменты UDP-глюкуронозилтрансферазы с идентичными карбоксильными концами» . J Biol Chem . 267 (5): 3257–61. DOI : 10.1016 / S0021-9258 (19) 50724-4 . PMID 1339448 .
Книги [ править ]
- Биохимия фенольных соединений , JB Harborne, 1964, Academic Press ( Google Книги )
- Фенольные смолы растений , Паскаль Риберо-Гайон, 1972, Издания Оливер и Бойд ( Google Книги , ISBN 0050025120 , ISBN 9780050025123 )
- Биохимия фенольных соединений растений , CF van Sumere и PJ Lea, Phytochemical Society of Europe, 1985, Clarendon Press ( Google Книги , ISBN 9780198541707 )
- Биохимия фенольных соединений , Уилфред Вермеррис и Ральф Николсон, 2006, Springer ( книга Google )
Внешние ссылки [ править ]
- Природные источники фенолов на www.britannica.com
Базы данных [ править ]
- Phenol -Explorer ( phenol-explorer.eu ), база данных, посвященная фенолам, содержащимся в продуктах питания, Огюстеном Скальбертом, INRA Клермон-Ферран, Unité de Nutrition Humaine (Human food unit)
- Фенолы в ChEBI (Химические вещества, представляющие биологический интерес)
- ChEMBLdb , база данных биоактивных малых молекул, подобных лекарствам, Европейского института биоинформатики
- Foodb , база данных соединений, содержащихся в продуктах питания