 | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Азид калия | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ECHA InfoCard | 100.039.997 | ||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| КН 3 | |||
| Молярная масса | 81,1184 г / моль | ||
| Внешность | Бесцветные кристаллы [1] | ||
| Плотность | 2,038 г / см3 [1] | ||
| Температура плавления | 350 ° C (662 ° F, 623 K) (в вакууме) [1] | ||
| Точка кипения | разлагается | ||
| 41,4 г / 100 мл (0 ° C) 50,8 г / 100 мл (20 ° C) 105,7 г / 100 мл (100 ° C) | |||
| Растворимость | растворим в этаноле не растворим в эфире | ||
| Термохимия | |||
Std энтальпия формации (Δ F H ⦵ 298 ) | -1,7 кДж / моль | ||
| Опасности | |||
| Основные опасности | Очень токсичен, взрывоопасен при сильном нагревании | ||
| NFPA 704 (огненный алмаз) | |||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 27 мг / кг (перорально, крыса) [2] | ||
| Родственные соединения | |||
Другие катионы | Азид натрия , меди (II) , азид , свинца (II) , азид , азид серебра | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Азид калия представляет собой неорганическое соединение, имеющее формулу KN
3. Это белая водорастворимая соль . Он используется как реагент в лаборатории.
Было обнаружено, что он действует как ингибитор нитрификации в почве. [3]
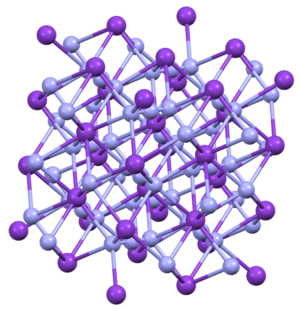
Структура [ править ]
KN 3 , RbN 3 , CsN 3 и TlN 3 имеют одинаковые структуры. Они кристаллизуются по форме тетрагональной формы. [4] Азид связан с восемью катионами в затменной ориентации. Катионы связаны с восемью концевыми N центрами. [5]
Синтез и реакции [ править ]
К.Н. 3 получают путем обработки карбоната калия с азотистоводородной кислотой , который генерируется на месте. [6] Напротив, аналогичный азид натрия получают (промышленным способом) с помощью « процесса Wislicenus », который протекает по реакции амида натрия с закисью азота . [7]
При нагревании или облучении ультрафиолетом он разлагается на металлический калий и газообразный азот . [8] Температуры разложения азидов щелочных металлов: NaN 3 (275 ° C), KN 3 (355 ° C), RbN 3 (395 ° C), CsN 3 (390 ° C). [9]
Опасности для здоровья [ править ]
Как и азид натрия, азид калия очень токсичен. ТДЗ из соответствующего азида натрия составляет 0,07 частей на миллион. Токсичность азидов обусловлена их способностью ингибировать цитохром с оксидазу . [7]
Ссылки [ править ]
- ^ a b c Дейл Л. Перри; Сидни Л. Филлипс (1995). Справочник неорганических соединений . CRC Press. п. 301. ISBN. 0-8493-8671-3.
- ^ http://chem.sis.nlm.nih.gov/chemidplus/rn/20762-60-1
- ^ Т. Д. Хьюз; Л. Ф. Уэлч (1970). «Азид калия как ингибитор нитрификации». Агрономический журнал . Американское агрономическое общество. 62 : 595–599. DOI : 10,2134 / agronj1970.00021962006200050013x .
- ^ Хилджи, MY; Шерман, ВФ; Уилкинсон, Г. Р. (1982). «Рамановские спектры при изменении температуры и давления азида калия KN.
3". Журнал Рамановской спектроскопии . 12 (3): 300–303. Bibcode : 1982JRSp ... 12..300K . Doi : 10.1002 / jrs.1250120319 . - ^ Ульрих Мюллер "Verfeinerung der Kristallstrukturen von KN 3 , RbN 3 , CsN 3 и TIN 3 " Zeitschrift für anorganische und allgemeine Chemie 1972, Volume 392, 159–166. DOI : 10.1002 / zaac.19723920207
- ^ PW Schenk "Щелочные азиды из карбонатов" в Справочнике по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, NY. Vol. 1. п. 475.
- ^ a b Хорст Х. Джобелиус, Ханс-Дитер Шарфф «Гидразойная кислота и азиды» в Энциклопедии промышленной химии Ульмана, 2005, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a13_193
- ^ Томпкинс, ФК; Янг, Д.А. (1982). «Фотохимическое и термическое образование центров окраски в кристаллах азида калия». Труды Лондонского королевского общества . Серия А, Математические и физические науки. 236 (1204): 10–23.
- ^ E. Dönges "Щелочные металлы" в Справочнике по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, NY. Vol. 1. п. 475.
| HN 3 | Он | ||||||||||||||||||
| LiN 3 | Быть (N 3 ) 2 | В (N 3 ) 3 | CH 3 N 3 , C (N 3 ) 4 | N (N 3 ) 3 , H 2 N — N 3 | О | FN 3 | Ne | ||||||||||||
| NaN 3 | Мг (N 3 ) 2 | Al (N 3 ) 3 | Si (N 3 ) 4 | п | SO 2 (N 3 ) 2 | ClN 3 | Ar | ||||||||||||
| Кн 3 | Ca (N 3 ) 2 | СБН (N 3 ) 3 | Ti (N 3 ) 4 | ВО (№ 3 ) 3 | Cr (N 3 ) 3 , CrO 2 (N 3 ) 2 | Mn (N 3 ) 2 | Fe (N 3 ) 2 , Fe (N 3 ) 3 | Co (N 3 ) 2 , Co (N 3 ) 3 | Ni (N 3 ) 2 | CuN 3 , Cu (N 3 ) 2 | Zn (N 3 ) 2 | Ga (N 3 ) 3 | Ge | В качестве | Se (N 3 ) 4 | 3 руб. | Kr | ||
| 3 руб. | Sr (N 3 ) 2 | Y | Zr (N 3 ) 4 | Nb | Пн | Tc | Ru (N 3 ) 6 3- | Rh (N 3 ) 6 3- | Pd (N 3 ) 2 | AgN 3 | Cd (N 3 ) 2 | В | Sn | Sb | Te | В 3 | Xe (N 3 ) 2 | ||
| ЦСН 3 | Ba (N 3 ) 2 | Hf | Та | W | Re | Операционные системы | Ir (N 3 ) 6 3- | Pt (N 3 ) 6 2− | Au (N 3 ) 4 - | Hg 2 (N 3 ) 2 , Hg (N 3 ) 2 | TlN 3 | Pb (N 3 ) 2 | Би (N 3 ) 3 | По | В | Rn | |||
| Пт | Ra (N 3 ) 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Ур. | Ц | Og | |||
| ↓ | |||||||||||||||||||
| Ла | Ce (N 3 ) 3 , Ce (N 3 ) 4 | Pr | Nd | Вечера | См | Европа | Gd (N 3 ) 3 | Tb | Dy | Хо | Э | Тм | Yb | Лу | |||||
| Ac | Чт | Па | UO 2 (N 3 ) 2 | Np | Пу | Являюсь | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||||
