 | |
| Имена | |
|---|---|
| Название ИЮПАК Диоксид калия | |
| Другие имена Супероксид калия | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.031.574 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| K O 2 | |
| Молярная масса | 71,096 г · моль -1 |
| Внешность | желтое твердое вещество |
| Плотность | 2,14 г / см 3 , твердый |
| Температура плавления | 560 ° С (1040 ° F, 833 К) (разлагается) |
| Гидролиз | |
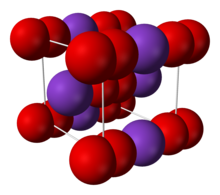
| Структура | |
| Телоцентрированный кубический ( O- 2) [ оспаривается ] | |
| Термохимия | |
Стандартная мольная энтропия ( S | 117 Дж · моль −1 · K −1 [1] |
Std энтальпия формации (Δ F H ⦵ 298 ) | −283 кДж · моль −1 [1] |
| Опасности | |
| Основные опасности | коррозионный, окислитель |
| R-фразы (устаревшие) | 8-14-34 |
| S-фразы (устарели) | 17-27-36 / 37/39 |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Другие анионы | Оксид калия Перекись калия |
Другие катионы | Супероксид натрия |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Супероксид калия - это неорганическое соединение с формулой KO 2 . [2] Это желтое парамагнитное вещество, которое разлагается во влажном воздухе. Это редкий пример стабильной соли супероксид- аниона. Супероксид калия используется как CO2скруббер, H2O осушитель и O2Генератор в ребризерах , космических кораблях , подводных лодках и системах жизнеобеспечения скафандров .
Производство и реакции [ править ]
Супероксид калия получают путем сжигания расплавленного калия в атмосфере кислорода . [3]
- К + О
2 → КО
2
Соль состоит из K+
и O-
2ионы, связанные ионной связью. Расстояние O-O составляет 1,28 Å. [4]
Реакционная способность [ править ]
Супероксид калия - сильный окислитель , способный превращать оксиды в пероксиды или молекулярный кислород . Гидролиз дает газообразный кислород, перекись водорода и гидроксид калия :
- 2 КО
2 + 2 часа
2О → 2 КОН + Н
2О
2+ O
2[5]
Гидроксид калия (КОН), поглощающий диоксид углерода, дает карбонаты:
- 2 КОН + СО
2 → К 2 СО 3 + Н 2 О - КОН + СО
2 → KHCO 3
Объединение этих двух реакций дает:
- 4 КО
2 + 2 СО
2 → 2 К 2 СО 3 + 3 О
2 - 4 КО
2 + 4 СО
2 + 2 H 2 O → 4 KHCO 3 + 3 O
2
Супероксид калия в качестве лабораторного реактива находит лишь нишевое применение. Поскольку он реагирует с водой, KO
2часто изучается в органических растворителях. Поскольку соль плохо растворяется в неполярных растворителях, обычно используются краун-эфиры . Тетраэтиламмония соль также известны. Типичные реакции этих солей включают использование супероксида в качестве нуклеофила , например, при превращении алкилбромидов в спирты и ацилхлоридов в диацилпероксиды . [6]
Приложения [ править ]
России космическое агентство имело успех с использованием супероксида калия в химических генераторах кислорода для его скафандра и Союз космических аппаратов . КО
2также использовался в канистрах для ребризеров для пожаротушения и горноспасательных работ, но имел ограниченное применение в ребризерах с аквалангом из-за его взрывоопасной реакции с водой.
КО
2реагирует с CO
2 в следующей реакции:
- 4 KO 2 (т) + 2 CO 2 (г) → 2K 2 CO 3 (т) + 3O 2 (г)
Теоретически 1 кг КО
2поглощает 0,310 кг CO
2при выпуске 0,338 кг O
2. Один моль КО
2абсорбирует 0,5 моль CO
2но высвобождает только 0,75 моль молекул газообразного кислорода ( O 2 ). Человеческое тело будет производить меньше CO.
2 молекулы кислорода необходимы, потому что окисление пищи также требует кислорода для производства воды и мочевины.
Опасности [ править ]
Супероксид калия является сильным окислителем и может вызывать взрывные реакции в сочетании с различными веществами и соединениями, включая воду, кислоты, органические вещества или порошкообразный графит. Даже сухой супероксид может образовывать чувствительное к ударам взрывчатое вещество в сочетании с органическими маслами, такими как керосин. [7] В 1999 году в Национальной лаборатории Ок-Риджа очистка от оксидов калия из утечки металла NaK привела к взрывочувствительному взрыву при насыщении минеральным маслом. [8]
Ссылки [ править ]
- ^ a b Zumdahl, Стивен С. (2009). Химические принципы (6-е изд.). Хоутон Миффлин. п. A22. ISBN 978-0-618-94690-7.
- ^ Хайян М .; Хашим MA; АльНашеф И.М. (2016). «Ион супероксида: генерация и химические последствия» . Chem. Ред . 116 (5): 3029–3085. DOI : 10.1021 / acs.chemrev.5b00407 . PMID 26875845 . CS1 maint: использует параметр авторов ( ссылка )
- ^ Якоб, Харальд; Лейнингер, Стефан; Леманн, Томас; Якоби, Сильвия; Gutewort, Свен (2007). «Пероксосоединения неорганические». Энциклопедия промышленной химии Ульмана . Wiley-VCH. DOI : 10.1002 / 14356007.a19_177.pub2 . ISBN 978-3527306732.
- ^ Абрахамс, Южная Каролина; Калнайс, Дж. (1955). «Кристаллическая структура α-супероксида калия» . Acta Crystallographica . 8 (8): 503–6. DOI : 10.1107 / S0365110X55001540 .
- Перейти ↑ Kumar De, Anil (2007). Учебник неорганической химии . New Age International. п. 247. ISBN. 978-8122413847.
- ^ Джонсон, Рой А .; Адрио, Хавьер; Рибагорда, Мария (2001). «Супероксид калия». e-EROS Энциклопедия реагентов для органического синтеза . Вайли. DOI : 10.1002 / 047084289X.rp250.pub2 . ISBN 0471936235.
- Перейти ↑ Aerojet Nuclear Company (1975). «Анализ взрывоопасности эвтектического раствора NaK и KO.
2". Национальная инженерная лаборатория Айдахо. - ^ "Расследование несчастного случая Y-12 NaK" . Министерство энергетики США. Февраль 2000. Архивировано из оригинала на 2010-05-28.
