| SH3 домен | |||||||||
|---|---|---|---|---|---|---|---|---|---|
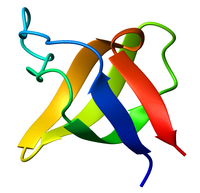 Ленточная диаграмма домена SH3, альфа-спектрина, от курицы (код доступа PDB 1SHG), окрашена от синего (N-конец) до красного (C-конец). | |||||||||
| Идентификаторы | |||||||||
| Символ | SH3_1 | ||||||||
| Pfam | PF00018 | ||||||||
| Клан пфам | CL0010 | ||||||||
| ИнтерПро | IPR001452 | ||||||||
| УМНАЯ | SM00326 | ||||||||
| PROSITE | PS50002 | ||||||||
| SCOP2 | 1ШФ / СФЕРА / СУПФАМ | ||||||||
| CDD | cd00174 | ||||||||
| |||||||||
SRC Гомология 3 домен (или SH3 домен ) представляет собой небольшой домен белка около 60 аминокислотных остатков. Первоначально SH3 был описан как консервативная последовательность в вирусном адапторном белке v-Crk. Этот домен также присутствует в молекулах фосфолипазы и нескольких цитоплазматических тирозинкиназ, таких как Abl и Src . [1] [2] Он также был идентифицирован в нескольких других семействах белков, таких как: киназа PI3 , белок , активирующий ГТФазу Ras , CDC24 и cdc25.. [3] [4] [5] Домены SH3 обнаружены в белках сигнальных путей, регулирующих цитоскелет , белке Ras , киназе Src и многих других. Белки SH3 взаимодействуют с адапторными белками и тирозинкиназами. Белки SH3, взаимодействуя с тирозинкиназами, обычно связываются далеко от активного центра . Приблизительно 300 SH3 доменов обнаружены в белках, кодируемых в геноме человека. В дополнение к этому, домен SH3 отвечал за контроль межбелковых взаимодействий в путях передачи сигналов [6] и регулирование взаимодействий белков, участвующих в передаче сигналов в цитоплазме. [7]
Структура [ править ]
Домен SH3 имеет характерную бета-бочкообразную складку, которая состоит из пяти или шести β-нитей, расположенных в виде двух плотно упакованных антипараллельных β-листов . Линкерные области могут содержать короткие спирали. Складка SH3-типа - это древняя складка, обнаруженная у эукариот, а также у прокариот. [8]
Связывание пептидов [ править ]
Классический домен SH3 обычно находится в белках, которые взаимодействуют с другими белками и опосредуют сборку специфических белковых комплексов, обычно через связывание с богатыми пролином пептидами в их соответствующих партнерах по связыванию. Классические домены SH3 ограничены у человека внутриклеточными белками, хотя небольшое семейство внеклеточных белков MIA человека также содержит домен с SH3-подобной складкой.
Многие SH3-связывающие эпитопы белков имеют консенсусную последовательность, которая может быть представлена как регулярное выражение или короткий линейный мотив :
-XPpXP- 1 2 3 4 5
причем 1 и 4 представляют собой алифатические аминокислоты, 2 и 5 всегда и 3 иногда являются пролином. Последовательность связывается с гидрофобным карманом домена SH3. Совсем недавно были описаны домены SH3, которые связываются с основным консенсусным мотивом RxxK. Примерами являются С-концевые домены SH3 адаптерных белков, таких как Grb2 и Mona (также известные как Gads, Grap2, Grf40, GrpL и т. Д.). Появились и другие связывающие SH3 мотивы, которые все еще появляются в ходе различных молекулярных исследований, подчеркивая универсальность этого домена.
SH3 интерактомы [ править ]
Сети белок-белковых взаимодействий, опосредованные доменом SH3, т. Е. SH3-интерактомы, показали, что SH3-интерактом червя напоминает аналогичную дрожжевую сеть, потому что он значительно обогащен белками, играющими роль в эндоцитозе. [9] [10] Тем не менее, взаимодействия, опосредованные ортологическим доменом SH3, сильно изменяются между червями и дрожжами. [9]
Белки с доменом SH3 [ править ]
- Адаптерные белки, передающие сигнал
- CDC24
- Cdc25
- PI3 киназа
- Фосфолипаза
- Белок, активирующий ГТФазу Ras
- Вав протоонкоген
- GRB2
- p54 S6 киназа 2 (S6K2)
- SH3D21
- ARMH3 (потенциально)
- STAC3
- Некоторые миозины
- SH3 и несколько доменов с анкириновыми повторами: SHANK1 , SHANK2 , SHANK3
- YAP1
- ARHGAP12
- вексин ( VXN )
- ТАНГО1
- Интеграза
- Киназа фокальной адгезии (FAK, PTK2)
- Пролин-богатая тирозинкиназа (Pyk2, CADTK, PTK2beta)
- TRIP10 (cip4)
См. Также [ править ]
- Src homology 2, содержащий домен
- Структурная область
Ссылки [ править ]
- ^ Поусон Т, Schlessingert J (июль 1993). «Домены SH2 и SH3». Текущая биология . 3 (7): 434–42. DOI : 10.1016 / 0960-9822 (93) 90350-W . PMID 15335710 . S2CID 53273571 .
- ^ Mayer BJ (апрель 2001). «Домены SH3: сложность в умеренности». Журнал клеточной науки . 114 (Pt 7): 1253–63. PMID 11256992 .
- ^ Музакие А, Т Gibson, ЛЕХТ В.П., Сараст М (июль 1992). «SH3 - богатый белковый домен в поисках функции» . Письма FEBS . 307 (1): 55–61. DOI : 10.1016 / 0014-5793 (92) 80901-R . PMID 1639195 . S2CID 8564342 .
- ^ Mayer BJ, Балтимор D (январь 1993). «Сигнализация через домены SH2 и SH3». Тенденции в клеточной биологии . 3 (1): 8–13. DOI : 10.1016 / 0962-8924 (93) 90194-6 . PMID 14731533 .
- ^ Pawson T (февраль 1995). «Белковые модули и сигнальные сети». Природа . 373 (6515): 573–80. DOI : 10.1038 / 373573a0 . PMID 7531822 . S2CID 4324726 .
- ^ Шлезингер J (февраль 1994). «Сигнальные белки SH2 / SH3». Текущее мнение в области генетики и развития . 4 (1): 25–30. DOI : 10.1016 / 0959-437X (94) 90087-6 . PMID 8193536 .
- Перейти ↑ Koch CA, Anderson D, Moran MF, Ellis C, Pawson T (май 1991). «Домены SH2 и SH3: элементы, которые контролируют взаимодействия цитоплазматических сигнальных белков». Наука . 252 (5006): 668–74. DOI : 10.1126 / science.1708916 . PMID 1708916 .
- ^ Whisstock JC, Lesk AM (апрель 1999). «Домены SH3 в прокариотах». Направления биохимических наук . 24 (4): 132–3. DOI : 10.1016 / s0968-0004 (99) 01366-3 . PMID 10322416 .
- ^ а б Синь, Сяофэн; Гфеллер, Дэвид; Ченг, Джеки; Тоникян, Раффи; Солнце, Линь; Го, Айлань; Лопес, Лианет; Павленко, Алевтина; Акинтоби, Аденреле (01.01.2013). «Интерактом SH3 сохраняет общую функцию по сравнению с конкретной формой» . Молекулярная системная биология . 9 : 652. DOI : 10.1038 / msb.2013.9 . ISSN 1744-4292 . PMC 3658277 . PMID 23549480 .
- ^ Тоникян, Раффи; Синь, Сяофэн; Торет, Кристофер П .; Гфеллер, Дэвид; Ландграф, Кристиана; Панни, Симона; Паолузи, Серена; Кастаньоли, Луиза; Каррелл, Бриджит (01.10.2009). «Байесовское моделирование дрожжевого взаимодействующего домена SH3 предсказывает пространственно-временную динамику белков эндоцитоза» . PLOS Биология . 7 (10): e1000218. DOI : 10.1371 / journal.pbio.1000218 . ISSN 1545-7885 . PMC 2756588 . PMID 19841731 .
Внешние ссылки [ править ]
- Ресурсный мотив эукариотического линейного мотива, класс LIG_SH3_1
- Ресурсный мотив Eukaryotic Linear Motif, класс LIG_SH3_2
- Ресурсный мотив Eukaryotic Linear Motif, класс LIG_SH3_3
- Ресурсный мотив Eukaryotic Linear Motif, класс LIG_SH3_4
- Ресурсный мотив Eukaryotic Linear Motif, класс LIG_SH3_5
- Ресурсный мотив эукариотического линейного мотива TRG_PEX_1
- Домены взаимодействия белков Nash Lab при передаче сигналов - домен SH3
- GENEART - Скрининг вашего белка на наличие всех SH3-доменов человека за один цикл фагового дисплея