 | |
 | |
| Имена | |
|---|---|
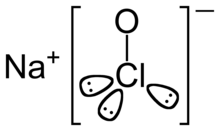
| Название ИЮПАК Гипохлорит натрия | |
Другие имена
| |
| Идентификаторы | |
| |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.028.790 |
| Номер ЕС |
|
| КЕГГ | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1791 |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| NaOCl | |
| Молярная масса | 74,442 г / моль |
| Внешность | зеленовато-желтое твердое вещество (пентагидрат) |
| Запах | хлороподобный и сладковатый |
| Плотность | 1,11 г / см 3 |
| Температура плавления | 18 ° С (64 ° F, 291 К) пентагидрат |
| Точка кипения | 101 ° С (214 ° F, 374 К) (разлагается) |
| 29,3 г / 100 мл (0 ° C) [1] | |
| Кислотность (p K a ) | 7,5185 |
| Основность (p K b ) | 6,4815 |
| Термохимия | |
Std энтальпия формации (Δ F H ⦵ 298 ) | -347,1 кДж / моль |
| Фармакология | |
| D08AX07 ( ВОЗ ) | |
| Опасности | |
| Паспорт безопасности | ICSC 1119 (раствор,> 10% активного хлора) ICSC 0482 (раствор, <10% активного хлора) |
Классификация ЕС (DSD) (устарела) | Коррозионный ( C ) Опасный для окружающей среды ( N ) |
| R-фразы (устаревшие) | R31 , R34 , R50 |
| S-фразы (устаревшие) | (S1 / 2) , S28 , S45 , S50 , S61 |
| NFPA 704 (огненный алмаз) |  2 0 1 OX |
| Родственные соединения | |
Другие анионы | Хлорид натрия Хлорит натрия Хлорат натрия Перхлорат натрия |
Другие катионы | Гипохлорит лития Гипохлорит кальция Гипохлорит калия |
Родственные соединения | Хлорноватистая кислота |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Гипохлорит натрия (обычно известный в разбавленном растворе как отбеливатель ) представляет собой химическое соединение с формулой NaOCl или NaClO, содержащее катион натрия ( Na+
) и гипохлорит- анион ( OCl-
или ClO-
). Он также может рассматриваться в качестве натриевой соли из хлорноватистой кислоты . Безводное соединение нестабильно и может взрывоопасно разлагаться. [2] [3] Его можно кристаллизовать в виде пентагидрата NaOCl · 5 H.
2О , бледное зеленовато-желтое твердое вещество, не взрывоопасное и стабильное при хранении в холодильнике. [4] [5]
Гипохлорит натрия чаще всего встречается в виде бледно-зеленовато-желтого разбавленного раствора, называемого жидким отбеливателем, который является бытовым химическим веществом, широко используемым (с 18 века) в качестве дезинфицирующего или отбеливающего средства .
В растворе соединение нестабильно и легко разлагается с высвобождением хлора, который является активным компонентом таких продуктов. Гипохлорит натрия - самый старый и самый важный отбеливатель на основе хлора . [6] [7]
Его коррозионные свойства, общедоступность и продукты реакции создают значительный риск для безопасности. В частности, смешивание жидкого отбеливателя с другими чистящими средствами, такими как кислоты или аммиак , может привести к образованию токсичных паров. [8]
Химия [ править ]
Устойчивость твердого тела [ править ]
Можно получить безводный гипохлорит натрия, но, как и многие гипохлориты, он очень нестабилен и взрывоопасно разлагается при нагревании или трении. [2] Разложение ускоряется углекислым газом на уровне атмосферы . [3] [8] Это белое твердое вещество с ромбической кристаллической структурой . [9]
Гипохлорит натрия также может быть получен в виде кристаллического пентагидрата NaOCl · 5 H.
2О , который не взрывоопасен и намного более стабилен, чем безводное соединение. [3] [4] Иногда формулу обозначают как 2 NaOCl · 10 H
2O . [ необходима цитата ] Прозрачные светло-зеленовато-желтые орторомбические [10] [11] кристаллы содержат 44% NaOCl по весу и плавятся при 25–27 ° C. Соединение быстро разлагается при комнатной температуре, поэтому его необходимо хранить в холодильнике. Однако при более низких температурах он довольно стабилен: по сообщениям, разлагается только 1% через 360 дней при 7 ° C. [5] [12]
Патент США 1966 г. утверждает, что стабильный твердый дигидрат гипохлорита натрия NaOCl · 2 H
2O можно получить, тщательно исключив ионы хлорида ( Cl-
), которые присутствуют в продуктах обычных производственных процессов и, как говорят, катализируют разложение гипохлорита до хлората ( ClO-
3) и хлорид. В одном из испытаний было заявлено, что дигидрат разлагается только на 6% после 13,5 месяцев хранения при -25 ° C. В патенте также утверждается, что дигидрат может быть восстановлен до безводной формы путем вакуумной сушки при температуре около 50 ° C, давая твердое вещество, которое не разлагается через 64 часа при -25 ° C. [13]
Равновесия и устойчивость решений [ править ]
При типичных температурах окружающей среды гипохлорит натрия более стабилен в разбавленных растворах, содержащих сольватированный Na.+
и OCl-
ионы. Плотность раствора составляет 1,093 г / мл при концентрации 5% [14] и 1,21 г / мл при 14% концентрации 20 ° C. [15] Стехиометрические растворы достаточно щелочные , с pH 11 или выше [5], поскольку хлорноватистая кислота является слабой кислотой :
- OCl-
+ H
2O ⇌ HOCl + OH-
В растворах NaOCl присутствуют следующие виды и равновесия : [16]
- HOCl (водн.) ⇌ H+
+ OCl- - HOCl (водн.) + Cl-
+ H+
⇌ Cl
2(водн.) + H
2О - Cl
2(водн.) + Cl-
⇌ Cl-
3 - Cl
2(водный) ⇌ Cl
2 (грамм)
Второе уравнение равновесия выше будет сдвинуто вправо, если хлор Cl
2позволяет улетучиваться в виде газа. Соотношения Cl
2, HOCl и OCl-
в растворе также зависят от pH. При pH ниже 2 большая часть хлора в растворе находится в форме растворенного элементарного Cl.
2. При pH более 7,4 большая часть находится в форме гипохлорита ClO.-
. [6] равновесие может быть сдвинуто добавлением кислоты (например, хлористоводородная кислота ) или основания (например, гидроксид натрия ) к раствору:
- ClO-
(водн.) + 2 HCl (водн.) → Cl
2(г) + H
2O (водн.) + Cl-
(водн.) - Cl
2(г) + 2 ОН-
→ ClO-
(водн.) + Cl-
(водн.) + H
2O (водн.)
При pH около 4, например при добавлении сильных кислот, таких как соляная кислота , количество недиссоциированной (неионизированной) HOCl является самым высоким. Реакцию можно записать так:
- ClO-
+ H+
⇌ HClO
Растворы гипохлорита натрия в сочетании с кислотой выделяют газообразный хлор, особенно сильно при pH <2, в результате реакций:
- HOCl (водн.) + Cl-
+ H+
⇌ Cl
2(водн.) + H
2О - Cl
2(водный) ⇌ Cl
2 (грамм)
При pH> 8 практически весь хлор находится в форме анионов гипохлорита ( OCl-
). Растворы достаточно стабильны при pH 11–12. Тем не менее, в одном отчете утверждается, что обычный 13,6% раствор реагента NaOCl потерял 17% своей прочности после хранения в течение 360 дней при 7 ° C. [5] По этой причине в некоторых приложениях можно использовать более стабильные соединения, выделяющие хлор, такие как гипохлорит кальция Ca (ClO).
2или трихлоризоциануровой кислоты (CNClO)
3.
Безводный гипохлорит натрия растворим в метаноле , и растворы стабильны. [ необходима цитата ]
Разложение до хлората или кислорода [ править ]
В растворе при определенных условиях анион гипохлорита может также диспропорционировать ( самоокисляться ) до хлорида и хлората : [17]
- 3 ClO-
+ H+
→ HClO
3+ 2 кл-
В частности, эта реакция происходит в растворах гипохлорита натрия при высоких температурах с образованием хлората натрия и хлорида натрия: [17] [18]
- 3 NaOCl (водн.) → 2 NaCl (водн.) + NaClO
3 (водн.)
Эта реакция используется при промышленном производстве хлората натрия.
При альтернативном разложении гипохлорита вместо этого образуется кислород:
- 2 OCl-
→ 2 Cl-
+ O
2
В горячих растворах гипохлорита натрия эта реакция конкурирует с образованием хлората, давая хлорид натрия и газообразный кислород: [17]
- 2 NaOCl (водн.) → 2 NaCl (водн.) + O
2 (грамм)
Эти две реакции разложения растворов NaClO максимальны при pH около 6. Реакция образования хлората преобладает при pH выше 6, в то время как кислородная реакция становится существенной ниже этого. Например, при 80 ° C, концентрациях NaOCl и NaCl 80 мМ и pH 6–6,5 хлорат производится с эффективностью ~ 95%. В преобладает кислород проводящих путей при рН 10. [17] Это разложение зависит от света [18] и ионов металлов катализаторов , таких как медь , никель , кобальт , [17] и иридия . [19] Катализаторы, такие как дихромат натрия Na
2Cr
2О
7и молибдат натрия Na
2МоО
4могут быть добавлены в промышленных масштабах для уменьшения кислородного пути, но в отчете утверждается, что только последний эффективен. [17]
Титрование [ править ]
Титрование растворов гипохлорита часто выполняется путем добавления отмеренного образца к избыточному количеству подкисленного раствора йодида калия ( KI ) и последующего титрования выделившегося йода ( I
2) стандартным раствором тиосульфата натрия или оксида фениларсина , используя крахмал в качестве индикатора, до исчезновения синего цвета. [11]
Согласно одному патенту США, стабильность содержания гипохлорита натрия в твердых веществах или растворах может быть определена путем мониторинга поглощения инфракрасного излучения за счет связи O – Cl. Характеристическая длина волны составляет 140,25 мкм для водных растворов, 140,05 мкм для твердого дигидрата NaOCl · 2 H.
2O и 139,08 мкм для безводной смешанной соли Na
2(OCl) (ОН) . [13]
Окисление органических соединений [ править ]
Окисление крахмала гипохлоритом натрия, который добавляет карбонильные и карбоксильные группы, имеет отношение к производству модифицированных крахмальных продуктов. [20]
В присутствии катализатора межфазного переноса спирты окисляются до соответствующего карбонильного соединения ( альдегида или кетона ). [21] [5] Гипохлорит натрия может также окислять органические сульфиды до сульфоксидов или сульфонов , дисульфиды или тиолы до сульфонилхлоридов или бромидов , имины до оксазиридинов . [5] Он также может деароматизировать фенолы . [5]
Окисление металлов и комплексов [ править ]
Гетерогенные реакции гипохлорита натрия и металлов, таких как цинк, протекают медленно с образованием оксида или гидроксида металла :
- NaOCl + Zn → ZnO + NaCl
Гомогенные реакции с координационными комплексами металлов протекают несколько быстрее. Это было использовано при эпоксидировании Якобсена .
Другие реакции [ править ]
При неправильном хранении в герметичных контейнерах гипохлорит натрия реагирует с диоксидом углерода с образованием карбоната натрия :
- 2 NaOCl + CO
2+ H2O → Na
2CO
3 + 2 HOCl
Гипохлорит натрия реагирует с большинством соединений азота с образованием летучих монохлорамин , дихлораминов и трихлорида азота :
- NH
3+ NaOCl → NH
2Cl + NaOH - NH
2Cl + NaOCl → NHCl
2 + NaOH - NHCl
2+ NaOCl → NCl
3 + NaOH
Нейтрализация [ править ]
Тиосульфат натрия - эффективный нейтрализатор хлора. Полоскание раствором 5 мг / л с последующим мытьем водой с мылом устранит запах хлора с рук. [22]
Производство [ править ]
Хлорирование соды [ править ]
Гипохлорит калия был впервые произведен в 1789 году Клодом Луи Бертолле в своей лаборатории на набережной Жавель в Париже , Франция, путем пропускания газообразного хлора через раствор калийного щелока . Полученная жидкость, известная как Eau de Javel («Жавельская вода»), представляла собой слабый раствор гипохлорита калия. Антуан Лабаррак заменил калийный щелок более дешевым содовым щелоком , получив таким образом гипохлорит натрия ( Eau de Labarraque ). [23] [24]
- Cl 2 (г) + 2 NaOH (водн.) → NaCl (водн.) + NaClO (водн.) + H 2 O (водн.)
Следовательно, хлор одновременно восстанавливается и окисляется ; этот процесс известен как диспропорционирование .
Этот процесс также используется для получения пентагидрата NaOCl · 5 H.
2O для промышленного и лабораторного использования. В типичном процессе газообразный хлор добавляется к 45–48% раствору NaOH. Часть хлорида натрия выпадает в осадок и удаляется фильтрацией, а затем получают пентагидрат путем охлаждения фильтрата до 12 ° C. [5]
Из гипохлорита кальция [ править ]
Другой метод заключается в реакции карбоната натрия («стиральная сода») с хлорированной известью («отбеливающий порошок»), смесью гипохлорита кальция Ca (OCl).
2, хлорид кальция CaCl
2, и гидроксид кальция Ca (OH)
2:
- Na
2CO
3(водн.) + Ca (OCl)
2(водн.) → CaCO
3(s) + 2 NaOCl (водн.) - Na
2CO
3(водн.) + CaCl
2(водн.) → CaCO
3(т) + 2 NaCl (водн.) - Na
2CO
3(водн.) + Са (ОН)
2(s) → CaCO
3(т) + 2 NaOH (водн.)
Этот метод обычно использовался для производства растворов гипохлорита для использования в качестве больничного антисептика, который продавался после Первой мировой войны под названием «Eusol», аббревиатура от Edinburgh University Solution Of (хлорированная) известь - ссылка на университетский факультет патологии, где он был разработан. [25]
Электролиз рассола [ править ]
Ближе к концу девятнадцатого века Э. С. Смит запатентовал хлорно-щелочной процесс : метод производства гипохлорита натрия, включающий электролиз рассола для получения гидроксида натрия и газообразного хлора, которые затем смешивались с образованием гипохлорита натрия. [26] [24] [27] Ключевые реакции:
- 2 Cl - → Cl 2 + 2 e - (на аноде )
- 2 ч
2O + 2 e - → H
2+ 2 НО-
(на катоде )
В то время как электроэнергия, так и солевой раствор были в дешевом предложении, и различные предприимчивые маркетологи воспользовались ситуацией, чтобы удовлетворить рыночный спрос на гипохлорит натрия. Растворы гипохлорита натрия в бутылках продавались под многочисленными торговыми наименованиями.
Сегодня улучшенная версия этого метода, известная как процесс Хукера (названный в честь Hooker Chemicals, приобретенного Occidental Petroleum ), является единственным крупномасштабным промышленным методом производства гипохлорита натрия. В процессе, когда хлор переходит в холодный разбавленный раствор гидроксида натрия, образуются гипохлорит натрия (NaClO) и хлорид натрия (NaCl) . Хлор получают промышленным способом путем электролиза с минимальным расстоянием между анодом и катодом . Температура раствора должна быть ниже 40 ° C (с помощью охлаждающих змеевиков), чтобы предотвратить нежелательное образование хлората натрия .
Коммерческие растворы всегда содержат значительные количества хлорида натрия (поваренной соли) в качестве основного побочного продукта , как видно из приведенного выше уравнения.
От хлорноватистой кислоты и соды [ править ]
Патент 1966 г. описывает производство твердого стабильного дигидрата NaOCl · 2 H.
2O путем взаимодействия безхлоридного раствора хлорноватистой кислоты HClO (например, полученного из монооксида хлора ClO и воды) с концентрированным раствором гидроксида натрия. При обычном приготовлении 255 мл раствора с 118 г / л HClO медленно добавляют при перемешивании к раствору 40 г NaOH в воде при температуре 0 ° C. Некоторое количество хлорида натрия выпадает в осадок и удаляется фитингом. Раствор упаривают в вакууме при 40–50 ° C и 1–2 мм рт. Ст. До кристаллизации дигидрата. Кристаллы сушат в вакууме, чтобы получить сыпучий кристаллический порошок. [13]
Тот же принцип был использован в другом патенте 1991 г. для получения концентрированных суспензий пентагидрата NaClO · 5 H.
2O . Обычно 35% -ный (по весу) раствор HClO объединяют с гидроксидом натрия при температуре примерно 25 ° C или ниже. Полученная суспензия содержит около 35% NaClO и относительно стабильна из-за низкой концентрации хлорида. [28]
От озона и соли [ править ]
Гипохлорит натрия может быть легко получен для исследовательских целей путем реакции озона с солью.
- NaCl + O 3 → NaClO + O 2
Эта реакция происходит при комнатной температуре и может быть полезна для окисления спиртов.
Упаковка и продажа [ править ]
Бытовой отбеливатель, продаваемый для стирки одежды, представляет собой 3–8 % раствор гипохлорита натрия на момент производства. Крепость варьируется от одной рецептуры к другой и постепенно уменьшается при длительном хранении. Гидроксид натрия обычно добавляют в небольших количествах в бытовой отбеливатель, чтобы замедлить разложение NaClO. [6]
10–25% раствор гипохлорита натрия, согласно паспорту безопасности Univar, поставляется с синонимами или торговыми названиями отбеливатель, Hypo, Everchlor, Chloros, Hispec, Bridos, Bleacol или Vo-redox 9110. [29]
12% раствор широко используется на гидротехнических сооружениях для хлорирования воды , а 15% раствор чаще [30] используется для обеззараживания сточных вод на очистных сооружениях. Гипохлорит натрия также можно использовать для дезинфекции питьевой воды в местах потребления [31], принимая 0,2–2 мг гипохлорита натрия на литр воды. [32]
Разбавленные растворы (от 50 ppm до 1,5%) содержатся в дезинфицирующих спреях и салфетках, используемых для твердых поверхностей. [33] [34]
Использует [ редактировать ]
Отбеливание [ править ]
Бытовой отбеливатель, как правило, представляет собой раствор, содержащий 3–8% гипохлорита натрия по весу и 0,01–0,05% гидроксида натрия ; гидроксид натрия используется , чтобы замедлить разложение гипохлорита натрия в натрия хлорида и хлората натрия . [35]
Очистка [ править ]
Гипохлорит натрия обладает разрушающими свойствами. [36] Помимо прочего, его можно использовать для удаления пятен плесени , пятен на зубах , вызванных флюорозом , [37] и пятен на посуде, особенно тех, которые вызваны танинами в чае . Он также использовался в моющих средствах для стирки и в качестве очистителя поверхностей.
Его отбеливающее, очищающее, дезодорирующее и едкое действие происходит из-за окисления и гидролиза ( омыления ). Органическая грязь под воздействием гипохлорита становится водорастворимой и нелетучей, что уменьшает ее запах и облегчает ее удаление.
Дезинфекция [ править ]
Гипохлорит натрия в растворе проявляет антимикробную активность широкого спектра и широко используется в медицинских учреждениях в самых разных условиях. [38] Обычно его разбавляют водой в зависимости от предполагаемого использования. «Сильный раствор хлора» - это 0,5% раствор гипохлорита (содержащий примерно 5000 частей на миллион свободного хлора), используемый для дезинфекции участков, загрязненных биологическими жидкостями, включая большие пятна крови (перед дезинфекцией участок сначала очищается с помощью моющего средства). [38] [39] Его можно приготовить путем разбавления бытового отбеливателя по мере необходимости (обычно 1 часть отбеливателя на 9 частей воды). [40] Было продемонстрировано, что такие растворы инактивируют как C. difficile [38], так и ВПЧ .[41] «Слабый раствор хлора» - это 0,05% раствор гипохлорита, используемый для мытья рук, но обычно его готовят изгранул гипохлорита кальция . [39]
« Раствор Дакина » - это дезинфицирующий раствор, содержащий низкую концентрацию гипохлорита натрия и немного борной кислоты или бикарбоната натрия для стабилизации pH. Было обнаружено, что он эффективен при концентрациях NaOCl всего 0,025%. [42]
Постановления правительства США разрешают дезинфекцию оборудования для пищевой промышленности и поверхностей, контактирующих с пищевыми продуктами, с помощью растворов, содержащих отбеливатель, при условии, что раствору дают возможность адекватно стекать до контакта с пищевыми продуктами, и что растворы не превышают 200 частей на миллион (ppm) доступного хлора ( например, одна столовая ложка обычного домашнего отбеливателя, содержащего 5,25% гипохлорита натрия, на галлон воды). [43] Если используются более высокие концентрации, поверхность необходимо промыть питьевой водой после дезинфекции.
Подобная концентрация отбеливателя в теплой воде используется для дезинфекции поверхностей перед приготовлением пива или вина. Поверхности необходимо промыть стерильной (кипяченой) водой, чтобы не придать заварке аромат; Хлорсодержащие побочные продукты дезинфекции поверхностей также вредны. Дезинфицирующее действие гипохлорита натрия аналогично хлорноватистой кислоте.
Растворы, содержащие более 500 частей на миллион доступного хлора, вызывают коррозию некоторых металлов , сплавов и многих термопластов (например, ацеталевой смолы ) и требуют тщательного удаления после дезинфекции отбеливателем, иногда после дезинфекции этанолом . Жидкости, содержащие гипохлорит натрия в качестве основного активного компонента, также используются для бытовой чистки и дезинфекции, например, средства для чистки унитазов . [44] Некоторые чистящие средства имеют вязкую форму, чтобы не стекать быстро с вертикальных поверхностей, таких как внутренняя часть унитаза.
Считается, что недиссоциированная (неионизированная) хлорноватистая кислота реагирует с бактериальными и вирусными ферментами и инактивирует их.
Нейтрофилы иммунной системы человека производят небольшие количества гипохлорита внутри фагосом , которые переваривают бактерии и вирусы.
Дезодорирование [ править ]
Гипохлорит натрия обладает дезодорирующими свойствами, которые идут рука об руку с его очищающими свойствами. [36]
Очистка сточных вод [ править ]
Растворы гипохлорита натрия использовались для обработки разбавленных цианидных сточных вод, таких как гальванические отходы. В периодических операциях обработки гипохлорит натрия использовался для обработки более концентрированных цианидных отходов, таких как растворы для гальваники цианида серебра. Токсичный цианид окисляется до цианата (OCN - ), который не токсичен и идеализируется следующим образом:
- CN - + OCl - → OCN - + Cl -
Гипохлорит натрия обычно используется в качестве биоцида в промышленных применениях для контроля образования слизи и бактерий в водных системах, используемых на электростанциях, целлюлозно-бумажных комбинатах и т. Д., В растворах обычно с 10-15% по весу.
Эндодонтия [ править ]
Гипохлорит натрия - это лекарство выбора из-за его эффективности против патогенных организмов и пищеварения пульпы при эндодонтической терапии . Его концентрация для использования варьируется от 0,5% до 5,25%. В низких концентрациях растворяет в основном некротические ткани; при более высоких концентрациях он также растворяет жизненно важные ткани и другие виды бактерий. Одно исследование показало, что Enterococcus faecalis все еще присутствовал в дентине после 40 минут воздействия 1,3% и 2,5% гипохлорита натрия, тогда как 40 минут при концентрации 5,25% были эффективны при удалении E. faecalis . [45]Помимо более высоких концентраций гипохлорита натрия, более длительное воздействие и нагревание раствора (60 ° C) также увеличивает его эффективность в удалении мягких тканей и бактерий в камере корневого канала. [45] 2% - обычная концентрация, так как меньше риск ятрогенного гипохлорита. [46] Инцидент с гипохлоритом - это немедленная реакция в виде сильной боли, за которой следует отек , гематома и экхимоз в результате того, что раствор выходит за пределы зуба и попадает в периапикальное пространство. Это может быть вызвано заеданием или чрезмерным давлением на шприц для ирригации, или это может произойти, если зуб имеет необычно большое апикальное отверстие.. [47]
Нейтрализация нервно-паралитического агента [ править ]
В этом разделе не процитировать любые источники . ( Март 2020 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
На различных объектах по уничтожению нервно-паралитического агента (химического оружия нервно-паралитического действия) по всей территории Соединенных Штатов 50% -ный гипохлорит натрия используется для удаления всех следов нервно-паралитического агента или волдыря из средств индивидуальной защиты после проникновения персонала в токсичные зоны. 50% гипохлорит натрия также используется для нейтрализации любых случайных выбросов нервно-паралитического агента в токсичные области. Меньшие концентрации гипохлорита натрия используются аналогичным образом в Системе борьбы с загрязнением, чтобы гарантировать, что в дымовые газы печи не попадут нервно-паралитические вещества.
Уменьшение повреждений кожи [ править ]
Ванны с разбавленным отбеливателем десятилетиями использовались для лечения умеренной и тяжелой экземы у людей [48] [49], но неясно, почему они работают. Согласно работе, опубликованной исследователями из Медицинской школы Стэнфордского университета в ноябре 2013 года, очень разбавленный (0,005%) раствор гипохлорита натрия в воде успешно лечил повреждение кожи с воспалительным компонентом, вызванное лучевой терапией , чрезмерным пребыванием на солнце или старением. у лабораторных мышей . Мыши с лучевым дерматитомпри ежедневных 30-минутных ваннах в растворе отбеливателя наблюдалось менее серьезное повреждение кожи, лучшее заживление и рост волос, чем у животных, купающихся в воде. Молекула называется ядерным фактор каппа-легкая цепь-энхансер активированных В - клетки (NF-кВ) , как известна, играет важную роль в воспалительных процессах , старение, и ответ на излучение. Исследователи обнаружили, что если активность NF-κB блокировалась у пожилых мышей путем купания их в отбеливающем растворе, кожа животных начинала выглядеть моложе, становясь от старой и хрупкой, становясь более толстой, с повышенной пролиферацией клеток . Эффект уменьшился после прекращения ванн, что указывало на необходимость регулярного воздействия для поддержания толщины кожи. [48] [50]
Безопасность [ править ]
По оценкам, ежегодно в британских домах происходит около 3300 несчастных случаев, требующих стационарного лечения, вызванных растворами гипохлорита натрия (RoSPA, 2002).
Окисление и коррозия [ править ]
Гипохлорит натрия - сильный окислитель . Реакции окисления вызывают коррозию . Растворы обжигают кожу и вызывают повреждение глаз, особенно при использовании в концентрированных формах. Однако, как признает NFPA, опасными окислителями считаются только растворы, содержащие более 40% гипохлорита натрия по весу. Растворы менее 40% классифицируются как умеренная опасность окисления (NFPA 430, 2000).
Растворы бытовых отбеливателей и хлораторов для бассейнов обычно стабилизируются значительной концентрацией щелока (каустической соды, NaOH) как части производственной реакции. Эта добавка сама по себе вызовет едкое раздражение или ожоги из-за обезжиривания и омыления кожных масел и разрушения тканей. Из-за этого процесса отбеливатель на коже становится скользким.
Опасности при хранении [ править ]
При контакте растворов гипохлорита натрия с металлами может выделяться легковоспламеняющийся водород. Контейнеры могут взорваться при нагревании из-за выделения газообразного хлора. [8]
Растворы гипохлорита вызывают коррозию обычных материалов контейнеров, таких как нержавеющая сталь [5] и алюминий . Немногочисленные совместимые металлы включают титан (который, однако, не совместим с сухим хлором) и тантал . [6] Стеклянная тара безопасна. [5] Также затронуты некоторые пластмассы и каучуки; безопасные варианты включают полиэтилен (PE), полиэтилен высокой плотности (HDPE, PE-HD), полипропилен (PP), [5] некоторые хлорированные и фторированные полимеры, такие как поливинилхлорид (PVC),политетрафторэтилен (ПТФЭ) и поливинилиденфторид (ПВДФ); а также этиленпропиленовый каучук и витон . [6]
Контейнеры должны обеспечивать выход кислорода, образующегося при разложении с течением времени, в противном случае они могут лопнуть. [2]
Реакции с другими распространенными продуктами [ править ]
Смешивание отбеливателя с некоторыми бытовыми чистящими средствами может быть опасным.
Растворы гипохлорита натрия, такие как жидкий отбеливатель, могут выделять токсичный газообразный хлор при нагревании выше 35 ° C [8] или в смеси с кислотой , такой как соляная кислота или уксус .
Исследование 2008 года показало, что гипохлорит натрия и органические химические вещества (например, поверхностно-активные вещества, ароматизаторы), содержащиеся в некоторых бытовых чистящих средствах, могут реагировать с образованием хлорированных летучих органических соединений (ЛОС). [51]Эти хлорированные соединения выделяются при очистке, некоторые из которых являются токсичными и вероятными канцерогенными веществами для человека. Исследование показало, что концентрации в воздухе помещений значительно увеличиваются (в 8–52 раза для хлороформа и в 1–1170 раз для тетрахлорметана, соответственно, по сравнению с базовыми количествами в домашнем хозяйстве) при использовании отбеливателей. Увеличение концентраций хлорированных летучих органических соединений было самым низким для обычного отбеливателя и самым высоким для продуктов в форме «густой жидкости и геля». Наблюдаемое значительное увеличение концентрации в воздухе помещений нескольких хлорированных ЛОС (особенно четыреххлористого углерода и хлороформа) указывает на то, что использование отбеливателя может быть источником, который может быть важным с точки зрения ингаляционного воздействия этих соединений.Авторы предположили, что использование этих чистящих средств может значительно увеличить риск рака.[51]
В частности, при смешивании гипохлоритных отбеливателей с аминами (например, чистящие средства, содержащие или выделяющие аммиак , соли аммония , мочевину или родственные соединения и биологические материалы, такие как моча ) образуются хлорамины. [52] [8] Эти газообразные продукты могут вызвать острое повреждение легких. Хроническое воздействие, например, из воздуха в плавательных бассейнах, где хлор используется в качестве дезинфицирующего средства, может привести к развитию атопической астмы. [53]
Отбеливатель может бурно реагировать с перекисью водорода с образованием газообразного кислорода:
- H 2 O 2 (водн.) + NaOCl (водн.) → NaCl (водн.) + H 2 O (водн.) + O 2 (газ.)
Взрывоопасные реакции или побочные продукты могут также возникать в промышленных и лабораторных условиях, когда гипохлорит натрия смешивают с различными органическими соединениями. [8]
Ограничения в сфере здравоохранения [ править ]
В октябре 2008 года Национальный институт здравоохранения и медицинского обслуживания Великобритании рекомендовал не использовать раствор Дакина при повседневном уходе за ранами. [54]
Воздействие на окружающую среду [ править ]
Несмотря на сильное биоцидное действие, гипохлорит натрия сам по себе оказывает ограниченное воздействие на окружающую среду, поскольку ион гипохлорита быстро разлагается, прежде чем он может быть поглощен живыми существами. [55]
Однако одна из основных проблем, связанных с использованием гипохлорита натрия, заключается в том, что он имеет тенденцию к образованию стойких хлорированных органических соединений , включая известные канцерогены , которые могут абсорбироваться организмами и попадать в пищевую цепь . Эти соединения могут образовываться при хранении в домашних условиях, а также при промышленном использовании. [35] Например, при смешивании бытового отбеливателя и сточных вод было обнаружено, что 1-2% доступного хлора образует органические соединения. [35] По состоянию на 1994 год не все побочные продукты были идентифицированы, но идентифицированные соединения включают хлороформ и четыреххлористый углерод . [35]Предполагаемое воздействие этих химикатов в результате использования находится в пределах профессионального воздействия. [35]
См. Также [ править ]
- Гипохлорит кальция Ca (OCl)
2 («обесцвечивающий порошок») - Гипохлорит калия KOCl (оригинальная «Жавельская вода»).
- Гипохлорит лития LiOCl
Ссылки [ править ]
- ^ Budavari S, О'Неил М, Смит А, Heckelman Р, Obenchain J (1996). «Гипохлорит натрия». Индекс Мерка (12-е изд.). п. 1478. ISBN 978-0-911910-12-4.
- ^ a b c Урбен П. (2006). Справочник Бретерика по опасным реактивным химическим веществам . 1 (7-е изд.). п. 1433. ISBN 978-0-08-052340-8.
- ^ а б в Хамано А (1997). «Образование и разложение безводной соли гипохлорита натрия и его пентагидрата». Наука и технология энергетических материалов . 58 (4): 152–155.
- ^ a b Депутат Эпплби (1919). «Гипохлорит натрия» . Журнал Химического общества, Сделки . 115 (XCVI): 1106–1109. DOI : 10.1039 / CT9191501106 .
- ^ a b c d e f g h i j k Кирихара М., Окада Т., Сугияма Ю., Акиёси М., Мацунага Т., Кимура Ю. (декабрь 2017 г.). «Кристаллы пентагидрата гипохлорита натрия (NaOCl · 5H2O): удобный и экологически безвредный окислитель для органического синтеза» . Исследования и разработки в области органических процессов . 21 (12): 1925–37. DOI : 10.1021 / acs.oprd.7b00288 .
- ^ a b c d e «Справочник по гипохлориту натрия OxyChem» (PDF) . oxy.com . OxyChem.
- ^ "Брошюра 96, Руководство по гипохориту натрия" . www.chlorineinstitute.org . Институт хлора.
- ^ a b c d e f (2013): « Гипохлорит натрия » Стэнфордское руководство по безопасному обращению с линейными ускорителями в лаборатории, глава 53, продукт 202. Доступ осуществлен 12 июня 2018 г.
- ^ Yaws CL (2015). Справочник по физическим свойствам углеводородов и химикатов Yaws (2-е изд.). Издательство Gulf Professional Publishing. п. 734. ISBN 978-0-12-801146-1.
- ^ " " Пентагидрат гипохлорита натрия, NaOCl · 5 H2O ]» . Сайт MatWeb Материал данных недвижимости . Проверено +12 июля +2018 .
- ^ a b «Гипохлорит натрия» . StudFiles . Проверено 14 июня 2018 .
- ^ Окада Т, Т Asawa, Сугияма Y, Иваи Т, Кирихара М, Кимура Y (июнь 2016). «Кристаллы пентагидрата гипохлорита натрия (NaOCl · 5H2O); эффективный реокислитель для окисления TEMPO». Тетраэдр . 72 (22): 2818–27. DOI : 10.1016 / j.tet.2016.03.064 .
- ^ a b c US 3498924 , Walsh RH, Dietz A, «Процесс получения стабильных гипохлоритов натрия», выпущенный в 1966 г.
- ^ «Гипохлорит натрия» . PubChem . Национальная медицинская библиотека США.
- ^ Environment Canada (1985): «Техническая информация о проблемных разливах: гипохлорит натрия (проект)».
- ^ Ван Л., Бассири М., Наджафи Р., Наджафи К., Ян Дж., Хосрови Б. и др. (Апрель 2007 г.). «Хлорноватистая кислота как потенциальное средство для ухода за ранами: часть I. Стабилизированная хлорноватистая кислота: компонент неорганического арсенала врожденного иммунитета» . Журнал ожогов и ран . 6 : e5. PMC 1853323 . PMID 17492050 .
- ^ Б с д е е Sandin S, Karlsson РК, Cornell A (апрель 2015). «Катализируемое и некаталитическое разложение гипохлорита в разбавленных растворах». Промышленные и инженерные химические исследования . 54 (15): 3767–74. DOI : 10.1021 / ie504890a .
- ^ а б Хамано А, Икеда А (1995). «Влияние pH на фоторазложение раствора гипохлорита натрия». Наука и технология энергетических материалов . 56 (2): 59–63.
- ^ Ayres GH, Бут MH (1955). «Каталитическое разложение раствора гипохлорита соединениями иридия. I. Зависимость pH от времени». Журнал Американского химического общества . 77 (4): 825–827. DOI : 10.1021 / ja01609a001 .
- ^ ASC - PT Asahimas Chemical (2009): « Гипохлорит натрия ». Онлайн-описание продукта. Проверено 14 июня 2018 г.
- ^ Мирафзал Г.А., Lozeva AM (1998). «Катализируемое фазовым переносом окисление спиртов гипохлоритом натрия». Буквы тетраэдра . 39 (40): 7263–7266. DOI : 10.1016 / S0040-4039 (98) 01584-6 .
- ^ "Стандартные методы исследования воды и сточных вод" (PDF) . www.umass.edu . Американская ассоциация общественного здравоохранения, Американская ассоциация водопроводных сооружений, Федерация водной среды . Проверено 26 января 2017 года .
- ^ Вет Н, Balej Дж, Беннет JE, Wintzer Р, Шейх С.А., Галлон Р (2007). «Оксиды хлора и хлоркислоты». Энциклопедия промышленной химии Ульмана (7-е изд.). Вайли. п. 2.
- ^ a b «Гипохлорит натрия как дезинфицирующее средство» . Lenntech.com . Проверено 7 августа 2011 года .
- ^ "эусол" . Оксфордский словарь английского языка . Проверено 3 июля 2014 года .
- ^ Мэй П. «Отбеливатель (гипохлорит натрия)» . Бристольский университет. Архивировано 13 декабря 2016 года . Проверено 13 декабря +2016 .
- ^ "Как продукты сделаны Том 2" . Май 2011 г.
- ^ США 5194238 , Дункан Б.Л., Несс RC, «Способ производства особо чистых концентрированных растворов гипохлорита натрия», опубликованном в 1991
- ^ "ПАСПОРТ БЕЗОПАСНОСТИ Гипохлорит натрия" (PDF) . Унивар . 9 августа 2007 г.
- ^ Инженерия сточных вод: обработка, удаление и повторное использование (3-е изд.). Metcalf & Eddy, Inc. 1991. стр. 497.
- ^ Lantagne DS (2018). «Дозировка гипохлорита натрия для бытовой и аварийной очистки воды» . Издательство IWA . 16 (1).
- ^ https://www.safewater.org/fact-sheets-1/2017/1/23/what-is-chlorination
- ^ Виейра Е.Р. (1999). Элементарная наука о питании . Springer. С. 381–382. ISBN 978-0-8342-1657-0.
- ^ Вильгельма N, Кауфман А, Блентон Е, Lantagne D (февраль 2018). «Дозировка гипохлорита натрия для бытовой и экстренной очистки воды: обновленные рекомендации» . Журнал воды и здоровья . 16 (1): 112–125. DOI : 10.2166 / wh.2017.012 . PMID 29424725 .
- ^ а б в г д Смит В. Т.. (1994). Безопасность гипохлорита для человека и окружающей среды. В: Материалы 3-й Всемирной конференции по детергентам: глобальные перспективы , стр. 183–5.
- ^ a b «Преимущества и аспекты безопасности гипохлорита, содержащегося в отечественных продуктах» (PDF) . AISE - Международная ассоциация мыла, моющих средств и средств ухода. Март 1997 г. Архивировано из оригинала (PDF) 30 марта 2014 г.
Это вспомогательное досье содержит информацию об оценке безопасности гипохлорита для окружающей среды и человека, а также о его преимуществах в качестве дезинфицирующего, дезодорирующего и удаляющего пятна агента.
- ^ Карденас Флорес А, Флорес Рейес Н, Гордилло Москосо А, Castanedo Cazares JP, Позос Гильен А (2009). «Клиническая эффективность 5% гипохлорита натрия для удаления пятен, вызванных флюорозом зубов». Журнал клинической детской стоматологии . 33 (3): 187–91. DOI : 10,17796 / jcpd.33.3.c6282t1054584157 . PMID 19476089 .
- ^ a b c Rutala WA, Weber DJ (15 февраля 2017 г.) [2008]. «Руководство по дезинфекции и стерилизации в медицинских учреждениях» (PDF) . www.cdc.gov . Проверено 29 августа 2017 года .
- ^ a b «Для общих медицинских учреждений в Западной Африке: как приготовить и использовать растворы хлора» . Геморрагическая лихорадка Эбола. Центры по контролю и профилактике заболеваний . Проверено 27 апреля 2016 года .
- ^ «Как приготовить крепкий (0,5%) раствор хлора из жидкого отбеливателя» (PDF) . Центры по контролю и профилактике заболеваний .
- ^ Мейерс Дж, Ryndock Е, Конвей МДж, Мейерс С, Робинсон Р (июнь 2014). «Восприимчивость вируса папилломы человека 16 типа высокого риска к клиническим дезинфицирующим средствам» . Журнал антимикробной химиотерапии . 69 (6): 1546–50. DOI : 10,1093 / JAC / dku006 . PMC 4019329 . PMID 24500190 .
- ^ Heggers ДП, Сазы JA, Стенберг BD, Строк Л., МакКоли RL, ХЕРНДОН Д.Н., Robson MC (1991). «Бактерицидные и ранозаживляющие свойства растворов гипохлорита натрия: Премия Линдберга 1991 г.». Журнал ожоговой терапии и реабилитации . 12 (5): 420–4. DOI : 10.1097 / 00004630-199109000-00005 . PMID 1752875 .
- ^ 21 Свода федеральных правил, часть 178
- ^ «Средства для чистки туалетов: узнайте о химических веществах вокруг вашего дома: пестициды: Агентство по охране окружающей среды США» . Агентство по охране окружающей среды США . 9 мая 2012 г.
- ^ a b Ирригенты и дезинфицирующие средства корневых каналов . Эндодонтия: коллеги за превосходство. Опубликовано для профессионального стоматологического сообщества Американской ассоциацией эндодонтов. Зима 2011 года.
- ^ Torabinejad M, Уолтон R (2008). Эндодонтия . VitalBook (4-е изд.). Компания WB Saunders. п. 265.
- ^ Hülsmann M, Hahn W (май 2000). «Осложнения при ирригации корневых каналов - обзор литературы и клинические случаи» (PDF) . Международный эндодонтический журнал . 33 (3): 186–93. DOI : 10.1046 / j.1365-2591.2000.00303.x . PMID 11307434 .
- ^ a b Conger K (15 ноября 2013 г.). «Воспалительное повреждение кожи у мышей заблокировано раствором отбеливателя, - говорится в исследовании» . Стэнфордская медицинская школа. Архивировано из оригинального 7 -го декабря 2013 года .
- ^ Pett K, Batta K, Vlachou C, Nicholls G. "Отбеливающие ванны с использованием стерилизующей жидкости Милтона для рецидивирующей инфицированной атопической экземы" . Архивировано из оригинального 12 декабря 2013 года . Цитировать журнал требует
|journal=( помощь ) - ^ Leung TH, Чжан LF, Ван J, Ning S, Нокс SJ, Ким SK (декабрь 2013). «Местный гипохлорит облегчает кожные заболевания, опосредованные NF-κB, у мышей» . Журнал клинических исследований . 123 (12): 5361–70. DOI : 10.1172 / JCI70895 . PMC 3859383 . PMID 24231355 .
- ^ a b Odabasi M (март 2008 г.). «Галогенированные летучие органические соединения от использования хлорсодержащих бытовых товаров». Наука об окружающей среде и технологии . 42 (5): 1445–51. Bibcode : 2008EnST ... 42.1445O . DOI : 10.1021 / es702355u . PMID 18441786 . Выложите резюме .
- ^ Krieger GR, Салливан - младший JB (2001). Клиническое состояние окружающей среды и токсическое воздействие (2-е изд.). Филадельфия, Пенсильвания [ua]: Липпинкотт Уильямс и Уилкинс. п. 968. ISBN 9780683080278. Проверено 30 августа +2016 .
- ^ Nickmilder M, Carbonnelle S, Bernard A (февраль 2007). «Уборка дома хлорным отбеливателем и риски аллергических и респираторных заболеваний у детей». Детская аллергия и иммунология . 18 (1): 27–35. DOI : 10.1111 / j.1399-3038.2006.00487.x . PMID 17295796 .
- ^ Не используйте Eusol и марлю для лечения хирургических ран, которые заживают вторичным натяжением , октябрь 2008 г., NICE, Лондон. Архивировано 14 июля 2014 г. в Wayback Machine. Доступно 3 июля 2014 г.
- ^ ASC - PT Asahimas Chemical (2009): « Гипохлорит натрия 10% ». Онлайн-паспорт безопасности материала (MSDS). Проверено 14 июня 2018 г.
Библиография [ править ]
- Джонс, Флорида (декабрь 1972 г.). «Отравление хлоридом от смешивания бытовых чистящих средств». ДЖАМА . 222 (10): 1312. DOI : 10,1001 / jama.222.10.1312 . PMID 4678160 .
- Bonnard M, Brondeau MT, Falcy M, Jargot D, Miraval S, Protois J, Schneider O. "Eaux et extraits de Javel Hypochlorite de натрия в растворе". Fiche Toxicologique . 157 .
Внешние ссылки [ править ]
- Международная карта химической безопасности 0482 (растворы <10% активного Cl)
- Международная карта химической безопасности 1119 (растворы> 10% активного Cl)
- Institut national de recherche et de sécurité ( на французском языке )
- Статистика несчастных случаев на дому и в свободное время за 2002 год (UK RoSPA)
- Экстренная дезинфекция питьевой воды ( Агентство по охране окружающей среды США )
- Хлорированная питьевая вода ( Монография МАИР )
- Отчет об исследовании NTP TR-392: Хлорированная и хлорированная вода ( NIH США )
- Руководство по использованию хлорного отбеливателя в качестве дезинфицирующего средства на предприятиях пищевой промышленности (Университет штата Оклахома)