 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Молибдат натрия | |
| Другие названия Динатрий молибдат | |
| Идентификаторы | |
| |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.028.683 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII |
|
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
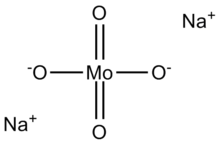
| Na 2 MoO 4 | |
| Молярная масса | 205,92 г / моль (безводный) 241,95 г / моль (дигидрат) |
| Появление | белый порошок |
| Плотность | 3,78 г / см 3 , твердый |
| Температура плавления | 687 ° С (1269 ° F, 960 К) |
| 84 г / 100 мл (100 ° C) | |
Показатель преломления ( n D ) | 1,714 |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материала |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Не воспламеняется |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 4000 мг / кг (крыса, перорально) [1] |
ЛК 50 ( средняя концентрация ) | > 2080 мг / м 3 (крыса, 4 часа) [1] |
| Родственные соединения | |
Другие анионы | Хромат натрия Вольфрамат натрия |
Другие катионы | Молибдат аммония |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Молибдат натрия , Na 2 MoO 4 , полезен в качестве источника молибдена . [2] Часто встречается в виде дигидрата Na 2 MoO 4 · 2H 2 O.
Анион молибдата (VI) тетраэдрический. Два катиона натрия координируются с каждым анионом. [3]
История [ править ]
Молибдат натрия впервые был синтезирован методом гидратации. [4] Более удобный синтез осуществляется путем растворения МоО 3 в гидроксиде натрия при 50–70 ° C и кристаллизации отфильтрованного продукта. [3] Безводную соль получают нагреванием до 100 ° C.
- MoO 3 + 2NaOH + H 2 O → Na 2 MoO 4 · 2H 2 O
Использует [ редактировать ]
В сельском хозяйстве используется 1 миллион фунтов стерлингов в год в качестве удобрений. В частности, его использование было предложено для лечения Хлыстохвостов в брокколи и цветной капусте в молибденовых-дефицитных почвах. [5] [6] Однако следует соблюдать осторожность, потому что при уровне 0,3 ppm молибдата натрия может вызвать дефицит меди у животных, особенно крупного рогатого скота. [3]
Он используется в промышленности для ингибирования коррозии, поскольку является неокисляющим анодным ингибитором. [3] Добавление молибдата натрия значительно снижает потребность в нитрите жидкостей, ингибированных нитритамином, и улучшает защиту от коррозии жидкостей на основе карбоксилатных солей. [7]
В промышленных системах водоподготовки, где возможна гальваническая коррозия из-за биметаллической конструкции, применение молибдата натрия предпочтительнее, чем нитрита натрия. Преимущество молибдата натрия в том, что дозирование молибдата с более низким содержанием в миллионных долях позволяет снизить проводимость циркулирующей воды. Молибдат натрия на уровне 50–100 частей на миллион обеспечивает такие же уровни ингибирования коррозии, что и нитрит натрия при уровнях 800+ частей на миллион. За счет использования более низких концентраций молибдата натрия проводимость сохраняется на минимальном уровне и, таким образом, снижаются потенциалы гальванической коррозии. [8]
Реакции [ править ]
При взаимодействии с боргидридом натрия молибден восстанавливается до оксида молибдена (IV) с более низкой валентностью : [9]
- Na 2 MoO 4 + NaBH 4 + 2H 2 O → NaBO 2 + MoO 2 + 2NaOH + 3H 2
Молибдат натрия реагирует с кислотами дитиофосфатов: [3]
- Na 2 MoO 4 + → [МоО 2 (S 2 P (OR) 2 ) 2 ]
который далее реагирует с образованием [MoO 3 (S 2 P (OR) 2 ) 4 ].
Безопасность [ править ]
Молибдат натрия несовместим с щелочными металлами, наиболее распространенными металлами и окислителями. Он взорвется при контакте с расплавленным магнием. Он будет бурно реагировать с межгалогенами (например, пентафторид брома ; трифторид хлора ). Его реакция с горячим натрием, калием или литием раскалена. [10]
Ссылки [ править ]
- ^ a b «Молибден (растворимые соединения, такие как Мо)» . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1984). Химия элементов . Оксфорд: Pergamon Press . ISBN 978-0-08-022057-4.
- ^ a b c d e Брейтуэйт, ER; Габер, Дж. Молибден: Очерк его химии и использования. 1994. Elsevier Science BV, Амстердам, Нидерланды.
- ^ Спицын, Викт. Я.; Кулешов И.М. Журнал Общей химии 1951. 21. 1701-15.
- ^ Плант, W. (1950). «Использование извести и молибдата натрия для борьбы с« хлыстовым хвостом »в брокколи». Природа . 165 (4196): 533. Bibcode : 1950Natur.165..533P . DOI : 10.1038 / 165533b0 . S2CID 4213274 .
- Перейти ↑ Davies, EB (1945). «Случай дефицита молибдена в Новой Зеландии». Природа . 156 (3961): 392. Bibcode : 1945Natur.156..392D . DOI : 10.1038 / 156392b0 . S2CID 4071159 .
- ^ Vukasovich, Марк С. Смазка Engineering 1980. 36 (12). 708-12.
- ↑ M. Houser, Corrosion Control Services, Inc., Вводное руководство.
- ^ Цанг, Чи Фо; Мантирам, Арумугам (1997). «Синтез низковалентных оксидов молибдена в водных растворах восстановлением Na 2 MoO 4 с помощью NaBH 4 ». Журнал химии материалов . 7 (6): 1003–1006. DOI : 10.1039 / A606389F . ISSN 1364-5501 .
- ^ http://www.mallbaker.com/americas/msds/english/s4394_msds_us_default.pdf [ постоянная мертвая ссылка ]
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме молибдата натрия . |
- Страница Института Линуса Полинга о молибдене .
