Перейти к навигации Перейти к поиску
| Имена | |||
|---|---|---|---|
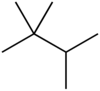
| Название ИЮПАК 2,2,3-триметилбутан [1] | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 1730756 | |||
| ChemSpider | |||
| ECHA InfoCard | 100.006.680 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| UNII | |||
| Номер ООН | 1206 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 7 Н 16 | |||
| Молярная масса | 100,205 г · моль -1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | Без запаха | ||
| Плотность | 0,693 г мл -1 | ||
| Температура плавления | От -26 до -24 ° С; От -15 до -11 ° F; От 247 до 249 К | ||
| Точка кипения | От 80,8 до 81,2 ° С; От 177,3 до 178,1 ° F; От 353,9 до 354,3 К | ||
| Давление газа | 23,2286 кПа (при 37,7 ° C) | ||
Константа закона Генри ( k H ) | 4,1 нмоль Па -1 кг -1 | ||
| -88,36 · 10 −6 см 3 / моль | |||
Показатель преломления ( n D ) | 1,389 | ||
| Термохимия | |||
Теплоемкость ( C ) | 213,51 Дж -1 моль -1 | ||
Стандартная мольная энтропия ( S | 292,25 Дж -1 моль -1 | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | −238,0 - −235,8 кДж моль −1 | ||
Std энтальпии сгорания (Δ с Н ⦵ 298 ) | −4,80449 - −4,80349 МДж моль −1 | ||
| Опасности | |||
| Пиктограммы GHS |     | ||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H225 , H302 , H305 , H315 , H336 , H400 | ||
Меры предосторожности GHS | P210 , P261 , P273 , P301 + 310 , P331 | ||
| NFPA 704 (огненный алмаз) |  0 3 0 | ||
| точка возгорания | -7 ° С (19 ° F, 266 К) | ||
самовоспламенения температуру | 450 ° С (842 ° F, 723 К) | ||
| Пределы взрываемости | 1–7% | ||
| Родственные соединения | |||
Родственные алканы |
| ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Триптан , или 2,2,3-триметилбутан , представляет собой органическое химическое соединение с молекулярной формулой C 7 H 16 или (Н 3 С-) 3 С-С (СН 3 ) 2 H. Это, следовательно , является алкан , в частности , наиболее компактный и сильно разветвленный изомеров гептана , единственный из которых имеет бутановую (C 4 ) основную цепь.
Триптан обычно используется в качестве антидетонационной добавки в авиационное топливо .
Ссылки [ править ]
- ^ «Триптан - Резюме соединения» . PubChem Compound . США: Национальный центр биотехнологической информации. 26 марта 2005 г. Идентификационные и связанные записи . Проверено 11 марта 2012 года .
| Эта статья об углеводородах - незавершенная . Вы можете помочь Википедии, расширив ее . |