 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК цикло [N-окса-D-аланил-D-валил-N-окса-L-валил-D-валил-N-окса-D-аланил-D-валил-N-окса-L-валил-L-валил- N-окса-L-аланил-L-валил-N-окса-L-валил-L-валил] | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.016.270 |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| C 54 H 90 N 6 O 18 | |
| Молярная масса | 1111,32 г / моль |
| Внешность | Белое твердое вещество |
| Температура плавления | 190 ° С (374 ° F, 463 К) |
| Растворимость | Метанол, этанол, этилацетат, петролейный эфир, дихлорметан |
| УФ-видимый (λ макс. ) | 220 нм |
| Опасности | |
| Основные опасности | Нейротоксикант |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 4 мг / кг (перорально, крыса) [1] |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
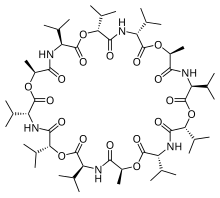
Валиномицин - это встречающийся в природе додекадепсипептид, используемый для транспорта калия и в качестве антибиотика . Валиномицин получают из клеток нескольких видов Streptomyces , примечательным из которых является S. fulvissimus .
Он входит в группу естественных нейтральных ионофоров, поскольку не имеет остаточного заряда. Он состоит из энантиомеров D- и L-валина (Val), D- альфа-гидроксиизовалериановой кислоты и L- молочной кислоты . Структуры попеременно связаны амидными и сложноэфирными мостиками. Валиномицин обладает высокой селективностью в отношении ионов калия по сравнению с ионами натрия внутри клеточной мембраны . [2] Он функционирует как специфический переносчик калия и способствует перемещению ионов калия через липидные мембраны «вниз» по градиенту электрохимического потенциала. [3]Константа стабильности K для комплекса калий-валиномицин почти в 100000 раз больше, чем у комплекса натрий-валиномицин. [4] Это различие важно для поддержания селективности валиномицина в отношении транспорта ионов калия (а не ионов натрия) в биологических системах.
Он классифицируется как чрезвычайно опасное вещество в Соединенных Штатах, как определено в Разделе 302 Закона США о чрезвычайном планировании и праве на информацию (42 USC 11002), и подлежит строгим требованиям отчетности со стороны предприятий, которые производят, хранят, или использовать его в значительных количествах. [5]
Структура [ править ]
Валиномицин представляет собой додекадепсипептид, то есть он состоит из двенадцати чередующихся аминокислот и сложных эфиров, образующих макроциклическую молекулу. Двенадцать карбонильных групп необходимы для связывания ионов металлов, а также для сольватации в полярном растворителе . В изопропиловый и метильные группы ответственны за сольватации в неполярных растворителях .[6] Наряду с формой и размером эта молекулярная двойственность является основной причиной его связывающих свойств. Ионы К должны отказаться от своей гидратной воды, чтобы пройти через поры. K +ионы октаэдрически координированы в квадратной бипирамидальной геометрии 6 карбонильными связями от Val. В этом пространстве 1,33 Ангстрем, Na + с его радиусом 0,95 Ангстрем значительно меньше канала, а это означает, что Na + не может образовывать ионные связи с аминокислотами поры при энергии, эквивалентной той, которую он теряет с молекулами воды. Это приводит к 10,000-кратной селективности для ионов K + по сравнению с Na +.. В случае полярных растворителей валиномицин в основном подвергает карбонилы действию растворителя, а в неполярных растворителях изопропильные группы расположены преимущественно на внешней стороне молекулы. Эта конформация изменяется, когда валиномицин связывается с ионом калия. Молекула «заперта» в конформации с изопропильными группами снаружи. На самом деле он не привязан к конфигурации, потому что размер молекулы делает ее очень гибкой, но ион калия придает макромолекуле некоторую степень координации.
Приложения [ править ]
Недавно сообщалось, что валиномицин является наиболее сильным агентом против коронавируса тяжелого острого респираторного синдрома (SARS-CoV) в инфицированных клетках Vero E6 . [ необходима цитата ]
Валиномицин действует как неметаллический изоформирующий агент в электродах, селективных для калия . [7] [8]
Этот ионофор используется для изучения мембранных везикул , где его можно выборочно применять в экспериментальных целях для уменьшения или устранения электрохимического градиента через мембрану. [ необходима цитата ]
Ссылки [ править ]
- ^ a b «ChemIDplus - 2001-95-8 - FCFNRCROJUBPLU-DNDCDFAISA-N - Валиномицин - Поиск похожих структур, синонимов, формул, ссылок на ресурсы и другой химической информации» . ТОКСНЕТ . Национальная медицинская библиотека США. Архивировано из оригинала 20 декабря 2015 года.
- ^ Ларс, Роуз; Дженкинс АТА (2007). «Влияние ионофора валиномицина на биомиметические твердые липидные мембраны DPPTE / EPC». Биоэлектрохим . 70 (2): 387–393. DOI : 10.1016 / j.bioelechem.2006.05.009 . PMID 16875886 .
- ^ Cammann K (1985). «Ионоселективные объемные мембраны как модели». Вершина. Curr. Chem . Темы современной химии. 128 : 219–258. DOI : 10.1007 / 3-540-15136-2_8 . ISBN 978-3-540-15136-4.
- ^ Роуз, MC; Хенкенс, Р.В. (1974). «Стабильность натриевых и калиевых комплексов валиномицина». Biochimica et Biophysica Acta (BBA) - Общие вопросы . 372 (2): 426–435. DOI : 10.1016 / 0304-4165 (74) 90204-9 .
- ^ "40 CFR: Приложение A к Части 355 - Список чрезвычайно опасных веществ и их планируемые пороговые количества" (PDF) (1 июля 2008 г.). Государственная типография . Проверено 29 октября 2011 года . Цитировать журнал требует
|journal=( помощь ) - ^ Thompson M, Krull UJ (1982). «Электроаналитический ответ двухслойной липидной мембраны на валиномицин: содержание холестерина в мембране». Анальный. Чим. Acta . 141 : 33–47. DOI : 10.1016 / S0003-2670 (01) 95308-5 .
- ^ Сафиулина D, Векслер В, Жарковский А, Kaasik А (2006). «Потеря митохондриального мембранного потенциала связана с увеличением объема митохондрий: физиологическая роль в нейронах». J. Cell. Physiol. 206 (2): 347–353. DOI : 10.1002 / jcp.20476 . PMID 16110491 .
- ^ Бюллетень ионофоров калия
Внешние ссылки [ править ]
- Химические правила техники безопасности из Нью - Джерси Департамента здравоохранения .
- Информация о здоровье на Scorecard .
- Валиномицин от Fermentek .
- Валиномицин в базе данных о свойствах пестицидов (PPDB)