 | |
 | |
| Имена | |
|---|---|
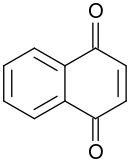
| Предпочтительное название IUPAC Нафталин-1,4-дион | |
| Другие имена 1,4-нафтохинон нафтохинон α-нафтохинон | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.004.526 |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| С 10 Н 6 О 2 | |
| Молярная масса | 158,15 г / моль |
| Плотность | 1,422 г / см 3 |
| Температура плавления | 126 ° С (259 ° F, 399 К) |
| Точка кипения | Начинает возвышаться при 100 ° C |
| 0,09 г / л | |
| -73,5 · 10 −6 см 3 / моль | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
1,4-Нафтохинон или пара-нафтохинон - это органическое соединение, полученное из нафталина . Он образует летучие желтые триклинные кристаллы и имеет резкий запах, похожий на запах бензохинона . Он почти не растворяется в холодной воде, слабо растворяется в петролейном эфире и лучше растворяется в полярных органических растворителях. В щелочных растворах он приобретает красновато-коричневый цвет. Витамин К является производным 1,4-нафтохинона. Это плоская молекула с одним ароматическим кольцом, конденсированным с субъединицей хинона. [2] Это изомер из 1,2-нафтохинона .
Подготовка [ править ]
Промышленный синтез включает аэробное окисление нафталина над катализатором из оксида ванадия: [3]
- С 10 Н 8 + 3/2 О 2 → С 10 Н 6 О 2 + Н 2 О
В лаборатории нафтохинон можно получить путем окисления различных соединений нафталина. Недорогой способ включает окисление нафталина триоксидом хрома . [4]
Реакции [ править ]
1,4-Нафтохинон действует как сильный диенофил в реакции Дильса-Альдера . Его аддукт с 1,3-бутадиеном может быть получен двумя способами: 1) длительная (45 дней) выдержка нафтохинона в чистом жидком бутадиене, взятом в огромном избытке при комнатной температуре в толстостенной стеклянной трубке, или 2) быстрое каталитическое циклоприсоединение при низкая температура в присутствии 1 эквивалента хлорида олова (IV) : [5]
Использует [ редактировать ]
1,4-Нафтохинон в основном используется в качестве предшественника антрахинона при реакции с бутадиеном с последующим окислением. Нитрование дает 5-нитро-1,4-нафталиндион, предшественник аминоантрохинона, который используется в качестве предшественника красителя. [3]
Производные [ править ]
Нафтохинона образует центральную химическую структуру многих природных соединений, прежде всего K витаминов . 2-Метил-1,4-нафтохинон, называемый менадионом , является более эффективным коагулянтом, чем витамин К.
Другие природные нафтохиноны включают юглон , plumbagin , droserone .
Производные нафтохинона обладают значительными фармакологическими свойствами. Они цитотоксичны , обладают значительными антибактериальными , противогрибковыми , противовирусными , инсектицидными , противовоспалительными и жаропонижающими свойствами. Растения с содержанием нафтохинона широко используются в Китае и странах Южной Америки, где их применяют для лечения злокачественных и паразитарных заболеваний. [6]
Нафтохинон действует как лиганд через свои электрофильные двойные связи углерод-углерод. [7]
Дихлон , хлорированное производное 1,4-нафтохинона, используется в качестве фунгицида.
См. Также [ править ]
- Гидроксинафтохинон
- 1,4-бензохинон
- Плумбагин
- Хинон
- Реакция проститутки
Ссылки [ править ]
- Перейти ↑ Merck Index , 11-е издание, 6315 .
- ^ Gaultier, J .; Хау, К. (1965). «Структура альфа-нафтохинона». Acta Crystallographica . 18 (2): 179–183. DOI : 10.1107 / S0365110X65000439 .
- ^ a b Grolig, J .; Вагнер Р. "Нафтохиноны". Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a17_067 .
- ^ Брауде, EA; Фосетт, Дж. С. (1953). «1,4-Нафтохинон» (PDF) . Органический синтез . 33:50 . ; Сборник , 4 , с. 698
- ^ М.А. Филатов; С. Балущев; И.З. Илиева; В. Энкельманн; Т. Митева; К. Ландфестер; С.Е. Алещенков; А.В. Чепраков (2012). «Тетраарилтетраантра [2,3] порфирины: синтез, структура и оптические свойства». J. Org. Chem . 77 (24): 11119–11131. DOI : 10.1021 / jo302135q . PMID 23205621 .
- ^ Бабула, P .; Adam, V .; Гавел, Л .; Кижек, Р. (2007). «Нафтохиноны и их фармакологические свойства». Ceská a Slovenská Farmacie (на чешском языке). 56 (3): 114–120. PMID 17867522 .
- ^ Kündig, EP; Lomberget, T .; Bragg, R .; Poulard, C .; Бернардинелли, Г. (2004). «Десимметризация мезо- диольного комплекса, полученного из [Cr (CO) 3 (η 6 -5,8-нафтохинон)]: использование новых катализаторов ацилирования диамина». Химические коммуникации . 2004 (13): 1548–1549. DOI : 10.1039 / b404006f .