| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC 1 H- подошва | |||
| Другие названия Арсенол Арсациклопентадиен | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
PubChem CID | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 4 H 4 AsH | |||
| Молярная масса | 128,00 г моль -1 | ||
| Родственные соединения | |||
Родственные соединения | Пиррола , phosphole , bismole , stibole | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
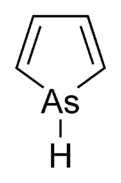
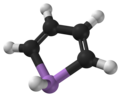
Арсоль , также называемый арсенолом [1] или арсациклопентадиеном , представляет собой мышьякоорганическое соединение с формулой C 4 H 4 AsH. Он классифицируется как металлол, изоэлектронен пирролу и связан с ним, за исключением того, что атом мышьяка замещен атомом азота . В то время как молекула пиррола плоская, молекула арсоли - нет, а атом водорода, связанный с мышьяком, выходит за пределы плоскости молекулы. Арзоль только умеренно ароматичен , около 40% ароматичности пиррола. [2]О самом арсоле не сообщалось в чистом виде, но существует несколько замененных аналогов, называемых арсолами . Arsoles и более сложные производные arsole имеют аналогичные структуры и химические свойства те из phosphole производных. Когда арсоль соединяется с бензольным кольцом, эта молекула называется арсиндолом или бензарзолом. [3]
Номенклатура [ править ]
Арсоль принадлежит к серии гетероциклических пниктогенных соединений. Название циклических мышьякоорганических соединений, таких как арсоль, основано на расширении номенклатурной системы Ханча – Видмана [4], одобренной IUPAC , как кратко изложено ниже: [5]
| Размер кольца | Ненасыщенное кольцо | Насыщенное кольцо |
|---|---|---|
| 3 | Арсирен | Арсиран |
| 4 | Арсет | Арсетан |
| 5 | Арсоль | Арсолан |
| 6 | Арсинин | Арсинан |
| 7 | Арсепин | Арсепан |
| 8 | Арсоцин | Арсокан |
| 9 | Поджог | Arsonane |
| 10 | Arsecine | Arsecane |
Из-за своего сходства с английским сленговым словом « arsehole » (широко используется за пределами Северной Америки), имя «arsole» считалось мишенью для забавы, «глупым именем» [6] [7] и одним из нескольких химические соединения с необычным названием . Однако совпадение с этим «глупым названием» также стимулировало подробные научные исследования. [2] [ неудавшаяся проверка ] [ сомнительно ]
Свойства [ править ]
| M | d (MC), Å | d (MH), Å | α (ККМ), ° | E , кДж / моль |
|---|---|---|---|---|
| N | 1,37 | 1.01 | 110 | 0 |
| п | 1,81 | 1,425 | 90,5 | 67 |
| В виде | 1,94 | 1,53 | 86 | 125 |
| Sb | 2,14 | 1,725 | 80,5 | 160 |
| Би | 2,24 | 1,82 | 78 | 220 |
Сама арсоль еще не изолирована экспериментально, но молекулярная геометрия и электронная конфигурация арсоли изучены теоретически. Расчеты также касались свойств простых производных арсоля, в которых атомы водорода замещены другими атомами или небольшими углеводородными группами, и имеются экспериментальные отчеты о химических свойствах более сложных производных арсоля. Аналогичная ситуация и с другими металлами C 4 H 4 MH, где M = P, As, Sb и Bi.
Планарность [ править ]
Расчеты показывают, что в то время как молекула пиррола (C 4 H 4 NH) плоская, фосфол (C 4 H 4 PH) и более тяжелые металлы - нет, а их атом водорода, связанный с пниктогеном, выходит из плоскости. [9] Аналогичная тенденция прогнозируется для фторированных производных C 4 F 4 MH (M = N, P, As, ..), но барьеры инверсии примерно на 50–100% выше. Плоскостность теряется даже в пирроле, когда его атом водорода, связанный с азотом, замещается, например, фтором.. Однако планарность оценивается в расчетах по энергии, необходимой для преобразования между двумя конфигурациями, в которых связь MH простирается влево или вправо от плоскости молекулы. Однако ненулевое (малое) значение этой энергии не обязательно означает, что молекула имеет низкую симметрию из-за возможности теплового или квантового туннелирования между двумя конфигурациями. [8]
Ароматичность [ править ]
Ароматичность арсоли проявляется в делокализации и резонансе ее кольцевых электронов. Это тесно связано с планарностью в том смысле, что чем планарнее молекула, тем сильнее ее ароматичность. [10] Ароматичность арсоли и ее производных долгие годы обсуждалась как с экспериментальной, так и с теоретической точки зрения. Обзор 2005 года в сочетании с квантово-химическими расчетами пришел к выводу, что арсоль сама по себе «умеренно» ароматична, поскольку ее кольцевой ток составляет 40% от тока пиррола, который, как известно, является ароматическим. Однако сопоставимый кольцевой ток был рассчитан для циклопентадиена , который долгое время считался неароматическим. [2]Другие сообщения предполагают, что ароматичность (и планарность) может варьироваться между производными арсоля. [9]
Химические свойства (производные арсоля) [ править ]
Химические свойства производных арсоля изучены экспериментально; они аналогичны фосфолу и его производным. [1] Замена всех атомов водорода в арсоле фенильными группами дает желтые иглы кристаллического пентафениларзола , температура плавления которого составляет 215 ° C. Этот комплекс может быть получен с выходом 50–93% путем взаимодействия 1,4-дииодо-1,2,3,4-тетрафенилбутадиена [11] или 1,4-дилитио-1,2,3,4- тетрафенилбутадиен с дихлоридом фениларшьяна (C 6 H 5 AsCl 2 ) в эфире .
Замена фениларшьянового дихлорида на трихлорид мышьяка дает 1-хлор-2,3,4,5-тетрафениларзол, который также образует желтые иглы, но с более низкой температурой плавления 182–184 ° C. Пентафениларзол можно дополнительно окислить перекисью водорода, что приведет к образованию желтых кристаллов с температурой плавления 252 ° C. Он также может реагировать с пентакарбонилом железа (Fe (CO) 5 ) в изооктане при 150 ° C с образованием твердого мышьяковистого соединения формулы C 34 H 25 As, Fe (CO) 3 . [1] Взаимодействие пентафениларзола с металлическим литием или калием дает 1,2,3-трифенилнафталин .[12]
Реакция дихлорида фениларшьяна с линейными дифенилами приводит к 1,2,5-трифениларзолу (см. Ниже), твердому веществу с температурой плавления около 170 ° C. [13] Это соединение образует различные анионы при обработке щелочными металлами. [14]
См. Также [ править ]
- Пиррол , аналог азота .
- Фуран , аналог кислорода .
- Тиофен , аналог серы .
- Простые ароматические кольца
- Варсол , нефтяной дистиллят с температурой кипения 150–200 ° C.
Ссылки [ править ]
- ^ a b c Фредерик Джордж Манн (1970). Гетероциклические производные фосфора, мышьяка, сурьмы и висмута . Джон Вили и сыновья. С. 357–360. ISBN 978-0-471-37489-3. Проверено 21 марта 2011 года .
В английском языке эту систему звонков часто называют арсенолом как «благозвучие».
CS1 maint: обескураженный параметр ( ссылка ) - ^ a b c М. П. Йоханссон; Дж. Юселиус (2005). «Возвращение к Arsole Aromaticity». Lett. Орг. Chem . 2 : 469–474. DOI : 10.2174 / 1570178054405968 .
Используя квантово-химическую методологию, мы повторно исследуем ароматичность столь обсуждаемой арсоли, используя недавно разработанный метод измерения магнитно-индуцированных токов (GIMIC). GIMIC обеспечивает количественную оценку силы индуцированного кольцевого тока, показывая, что арсоль умеренно ароматична.
- ^ A. Muranaka; С. Ясуике; C.-Y. Лю; Дж. Курита; Н. Какусава; Т. Цучия; М. Окуда; Н. Кобаяши; Ю. Мацумото; К. Йошида; Д. Хашизуме; М. Учияма (2009). «Влияние периодической замены гетероатома на спектроскопические свойства производных индола и бензофурана». J. Phys. Chem. . 113 (2): 464–473. DOI : 10.1021 / jp8079843 . PMID 19099440 .
- ^ " Пересмотр расширенной системы номенклатуры Ганча-Видмана для гетеромоноциклов " в ИЮПАК, получено 29 сентября 2008 г.
- ^ Николас С. Норман (1998). Химия мышьяка, сурьмы и висмута . Springer. п. 235. ISBN 978-0-7514-0389-3. Проверено 15 марта 2011 года . CS1 maint: обескураженный параметр ( ссылка )
- ↑ Ричард Уотсон Тодд (25 мая 2007 г.). Много шума об английском: вдоль и поперек причудливые закоулки увлекательного языка . Издательство Николаса Брили. п. 138. ISBN 978-1-85788-372-5. Проверено 15 марта 2011 года . CS1 maint: обескураженный параметр ( ссылка )
- ^ Пол Мэй, Молекулы с глупыми или необычными названиями , опубл. 2008 Imperial College Press, ISBN 978-1-84816-207-5 (PBK). См. Также веб-страницу « Молекулы с глупыми или необычными названиями » в Школе химии Бристольского университета (получено 29 сентября 2008 г.)
- ^ a b Пельцер, Силке; Вичманн, Карин; Везендруп, Ральф; Швердтфегер, Питер (2002). "Тенденции инверсионных барьеров IV. Группа 15, аналог пиррола". Журнал физической химии . 106 : 6387. DOI : 10.1021 / jp0203494 .
- ^ a b Тадеуш Марек Крыговски; Михал К. Цирански; М. Агостинья Р. Матос (2009). Ароматичность в гетероциклических соединениях . Springer. С. 47–. ISBN 978-3-540-68329-2. Проверено 21 марта 2011 года . CS1 maint: обескураженный параметр ( ссылка )
- ^ Пеллони, Стефано; Лаззеретти, Паоло (2007). «Магнитотропность фосфола и его аналога мышьяка». Счета теоретической химии . 118 : 89. DOI : 10.1007 / s00214-007-0247-0 .
- ^ Брей, EH; Hubel, W .; Каплиер, И. (1961). «Новые ненасыщенные гетероциклические системы. I». Журнал Американского химического общества . 83 : 4406. DOI : 10.1021 / ja01482a026 .
- ^ CW Bird; Гордон Уильям Генри Чизмен (31 декабря 1973 г.). Ароматическая и гетероатомная химия . Королевское химическое общество. С. 23–. ISBN 978-0-85186-753-3. Проверено 23 марта 2011 года . CS1 maint: обескураженный параметр ( ссылка )
- ^ Готтфрид Markl & Hagen Гауптман (1972). «Необычная замена в кольце арсоля» (PDF) . Angewandte Chemie International Edition на английском языке . 11 : 441. DOI : 10.1002 / anie.197204411 .
- ^ Markl, G (1983). "Синтез 1-фенил-2,5-диарил (диалкил) -арсолена; umsetzung der arsole mit alkalimetallen und lithiumorganylen". Журнал металлоорганической химии . 249 : 335. DOI : 10.1016 / S0022-328X (00) 99433-6 .