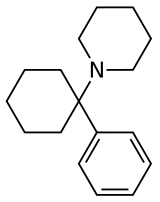
Arylcyclohexylamines , также известный как arylcyclohexamines или arylcyclohexanamines , является химическим классом от фармацевтического , проектировщика и экспериментальных препаратов .
История [ править ]
Фенциклидин (PCP) считается первым арилциклогексиламином с признанными анестезирующими свойствами, но несколько арилциклогексиламинов были описаны до PCP в научной литературе, начиная с PCA (1-фенилциклогексан-1-амин), синтез которого был впервые опубликован в 1907 году. О PCE было сообщено в 1953 году, а о PCMo - в 1954 году, причем последнее соединение было описано как сильнодействующее седативное средство. [1] Анестетики на основе арилциклогексиламина интенсивно изучались в Parke-Davis , начиная с синтеза фенциклидина в 1956 году, а затем и связанного с ним соединения кетамина . [1] В 1970-е годы дебютировали эти соединения, особенно ПХФ и его аналоги., как незаконно используемые рекреационные наркотики из-за их диссоциативных галлюциногенных и эйфориантных эффектов. Так, класс был расширен научными исследованиями в стимулятор , обезболивающий и нейропротекторные агент, а также подпольными химики в поисках новых рекреационных наркотиков . [2] [3] [4]
Структура [ править ]
Арилциклогексиламин состоит из звена циклогексиламина с присоединенным арильным фрагментом . Арильная группа расположена геминально по отношению к амину . В простейших случаях арильный фрагмент обычно представляет собой фенильное кольцо , иногда с дополнительным замещением. Амин обычно не является первичным ; вторичные амины, такие как метиламино или этиламино, или третичные циклоалкиламины, такие как пиперидино и пирролидино , являются наиболее часто встречающимися N -заместителями.
Фармакология [ править ]
Arylcyclohexylamines переменно обладают антагонистической рецептора NMDA , [5] [6] обратного захвата дофамина ингибирующее , [7] и μ-опиатных рецепторов агонистическую [8] свойства. Кроме того, σ - рецептор агонистическим, [9] Нах рецептор антагонистический, [10] и D 2 рецептор агонистический [11] действия были зарегистрированы для некоторых из этих агентов. Антагонизм рецептора NMDA оказывает анестезирующее, противосудорожное, нейрозащитное и диссоциативное действие; блокада переносчика дофаминав больших количествах опосредует стимулирующие и эйфориантные эффекты, а также психоз ; и активация μ-опиоидного рецептора вызывает обезболивающий и эйфориантный эффекты. Стимуляция рецепторов σ и D 2 также может способствовать развитию галлюциногенных и психотомиметических эффектов. [11]
Это универсальные агенты с широким диапазоном возможных фармакологических активностей в зависимости от степени и диапазона, в котором применяются химические модификации. [12] [13] [14] [15] [16] [17] [18] [19] [20] Разнообразный выбор замен, которые производятся, позволяет «точно настроить» получаемый фармакологический профиль ». Например, BTCP является селективным ингибитором обратного захвата дофамина , [7] PCP является главным образом антагонистом NMDA, [5] и BDPC является сильным агонистом μ-опиоидов, [21] в то время как PRE-084 является селективным сигма-рецептором.агонист. [22] Таким образом, радикально разная фармакология возможна благодаря различным структурным комбинациям.
Список арилциклогексиламинов [ править ]
| Структура | Сложный | Арильный заместитель | Группа N | Циклогексильное кольцо |
|---|---|---|---|---|
| PCA [23] | Фенил | NH 2 | - | |
| PCM [23] | Фенил | Метиламино | - | |
| Этициклидин | Фенил | Этиламино | - | |
| PCPr [24] | Фенил | н- пропиламино | - | |
| PCiP | Фенил | Изопропиламино | - | |
| PCAL [25] | Фенил | Аллиламино | - | |
| PCBu | Фенил | н- бутиламино | - | |
| PCEOH | Фенил | Гидроксиэтиламино | - | |
| PCMEA [26] | Фенил | Метоксиэтиламино | - | |
| PCEEA | Фенил | Этоксиэтиламино | - | |
| PCMPA | Фенил | Метоксипропиламино | - | |
| PCDM [23] | Фенил | Диметиламино | - | |
| Диетциклидин | Фенил | Диэтиламино | - | |
| 2-НО-ПХФ [5] | Фенил | Пиперидин | 2-гидрокси | |
| 2-Me-PCP [27] | Фенил | Пиперидин | 2-метил | |
| 2-MeO-PCP [28] | Фенил | Пиперидин | 2-метокси | |
| 2-кето-PCP | Фенил | Пиперидин | 2-Кето | |
| Этициклидон («O-PCE») | Фенил | Этиламино | 2-Кето | |
| 2-кето-PCPr | Фенил | н- пропиламино | 2-Кето | |
| 4-метил-PCP | Фенил | Пиперидин | 4-метил | |
| 4-кето-PCP | Фенил | Пиперидин | 4-кето | |
| 2'-Cl-PCP | о- хлорфенил | Пиперидин | - | |
| 3'-Cl-PCP | м- хлорфенил | Пиперидин | - | |
| 2'-MeO-PCP | о- метоксифенил | Пиперидин | - | |
| 3'-F-PCP [29] | м- фторфенил | Пиперидин | - | |
| 3'-Me-PCP [30] | м- Толил | Пиперидин | - | |
| 3'-Me-PCPy | м- Толил | Пирролидин | - | |
| 3'-NH 2 -PCP | м- аминофенил | Пиперидин | - | |
| 3'-HO-PCP | м- гидроксифенил | Пиперидин | - | |
| 3'-MeO-PCP | м- метоксифенил | Пиперидин | - | |
| 3 ', 4'-МД-ПКП | 3,4-метилендиоксифенил | Пиперидин | - | |
| 3'-MeO-PCE | м- метоксифенил | Этиламино | - | |
| 3'-HO-PCE | м- гидроксифенил | Этиламино | - | |
| 3'-MeO-PCPr | м- метоксифенил | н- пропиламино | - | |
| 3'-HO-PCPr | м- гидроксифенил | н- пропиламино | - | |
| 3 ', 4'-МД-ПКПр | 3,4-метилендиоксифенил | н- пропиламино | - | |
| 3'-MeO-PCPy [30] | м- метоксифенил | Пирролидин | - | |
| 4'-HO-PCP | п -гидроксифенил | Пиперидин | - | |
| Метоксидин (4'-MeO-PCP) | п- метоксифенил | Пиперидин | - | |
| 4'-MeO-PCE | п- метоксифенил | Этиламино | - | |
| 4'-F-PCP [29] | п- фторфенил | Пиперидин | - | |
| 4'-F-PCPy | п- фторфенил | Пирролидин | - | |
| Аркетамин | о- хлорфенил | Метиламино | 2-Кето | |
| Десхлорокетамин | Фенил | Метиламино | 2-Кето | |
| Эскетамин | о- хлорфенил | Метиламино | 2-Кето | |
| Кетамин | о- хлорфенил | Метиламино | 2-Кето | |
| Гидроксиноркетамин | о- хлорфенил | NH 2 | 2-кето, 6-гидрокси | |
| Эткетамин | о- хлорфенил | Этиламино | 2-Кето | |
| NPNK | о- хлорфенил | н- пропиламино | 2-Кето | |
| Метоксикетамин | о- метоксифенил | Метиламино | 2-Кето | |
| oMDCK | о -Толил | Метиламино | 2-Кето | |
| mMDCK | м- Толил | Метиламино | 2-Кето | |
| мета- кетамин | м- хлорфенил | Метиламино | 2-Кето | |
| изо- кетамин | о- хлорфенил | Метиламино | 4-кето | |
| 2-фтордесхлоркетамин | о -Фторфенил | Метиламино | 2-Кето | |
| 3-фтордесхлоркетамин | м- фторфенил | Метиламино | 2-Кето | |
| Бромокетамин | о -Бромфенил | Метиламино | 2-Кето | |
| TFMDCK | о- трифторметилфенил | Метиламино | 2-Кето | |
| SN 35210 [31] | о- хлорфенил | Карбометоксибутиламино | 2-Кето | |
| Метоксетамин | м- метоксифенил | Этиламино | 2-Кето | |
| Метоксметамин | м- метоксифенил | Метиламино | 2-Кето | |
| Метокспропамин | м- метоксифенил | н- пропиламино | 2-Кето | |
| MXiPr | м- метоксифенил | i -Пропиламино | 2-Кето | |
| Этоксетамин | м- этоксифенил | Этиламино | 2-Кето | |
| DMXE (3-Me-2'-Oxo-PCE) | м- Толил | Этиламино | 2-Кето | |
| HXE | м- гидроксифенил | Этиламино | 2-Кето | |
| HXM | м- гидроксифенил | Метиламино | 2-Кето | |
| FXE | м- фторфенил | Этиламино | 2-Кето | |
| Фенциклидин (PCP) | Фенил | Пиперидин | - | |
| PC3MP | Фенил | 3-метилпиперидин | - | |
| PC4MP | Фенил | 4-метилпиперидин | - | |
| Ролициклидин (PCPy) | Фенил | Пирролидин | - | |
| PCDMPy | Фенил | 3,3-диметилпирролидин | - | |
| PCMo | Фенил | Морфолин | - | |
| Метокси-ПКМ [6] (2'-МеО-ПКМо) | о- метоксифенил | Морфолин | - | |
| 3'-MeO-PCMo | м- метоксифенил | Морфолин | - | |
| 4'-MeO-PCMo | п- метоксифенил | Морфолин | - | |
| Метил-ПКМ [32] (4'-Me-PCMo) | п- толил | Морфолин | - | |
| Гидроксиметил-PCM | 2-метил-4-гидроксифенил | Морфолин | - | |
| PYCP [33] | 2-пиридинил | Пиперидин | - | |
| TCM | 2-тиенил | Метиламино | - | |
| ТВК | 2-тиенил | Этиламино | - | |
| TCPr [34] | 2-тиенил | Пропиламино | - | |
| Теноциклидин (TCP) | 2-тиенил | Пиперидин | - | |
| TCPy | 2-тиенил | Пирролидин | - | |
| Тилетамин | 2-тиенил | Этиламино | 2-Кето | |
| Гациклидин | 2-тиенил | Пиперидин | 2-метил | |
| BDPC | п -Бромфенил | Диметиламино | 4-фенэтил-4-гидрокси | |
| С-8813 | п -Бромфенил | Диметиламино | 4- (тиофен-2-ил) этил-4-гидрокси | |
| Диметамин [35] | п- толил | Диметиламино | 4-кето | |
| 3 '' - OH-2'-Me-PCP [36] | о -Толил | 3-гидроксипиперидин | - | |
| 4 '' - Ph-4 '' - OH-PCP [37] | Фенил | 4-фенил-4-гидроксипиперидин | - | |
| BTCP [38] | Бензотиофен-2-ил | Пиперидин | - | |
| BTCPy [39] | Бензотиофен-2-ил | Пирролидин | - | |
| PRE-084 | Фенил | Морфолинилэтилкарбоксилат | - |
Были проведены эксперименты с другими размерами циклоалкановых колец, а не только с точки зрения циклогексиламина. Циклопентильный гомолог PCP активен примерно с 1/10 активности, в то время как циклогептильные и циклооктильные производные неактивны. Необходимый циклоалкилкетон реагирует с PhMgBr; 3 ° спирт затем реагирует с NaN 3 ; азид затем восстанавливается с помощью LAH. Затем на последней стадии пиперидиновое кольцо конструируется из 1-5-дибромпентана. [40]
Жесткий [ править ]
Конформационно ограниченные аналоги были также получены и исследованы Morieti et al. [41]
Ссылки [ править ]
- ^ a b Моррис, H .; Валлах, Дж. (2014). «От PCP к MXE: всесторонний обзор немедицинского использования диссоциативных препаратов». Тестирование и анализ на наркотики . 6 (7–8): 614–32. DOI : 10.1002 / dta.1620 . PMID 24678061 .
- ↑ Valter K, Arrizabalaga P. Справочник дизайнерских лекарств. Elsevier, 1998. ISBN 0-444-20525-X
- ↑ Wallach J, Brandt SD (август 2018). «Новые психоактивные вещества на основе фенциклидина». Новые психоактивные вещества . Справочник по экспериментальной фармакологии. 252 . С. 261–303. DOI : 10.1007 / 164_2018_124 . ISBN 978-3-030-10560-0. PMID 30105474 .
- ^ Уоллах, Джейсон; Брандт, Саймон Д. (2018). «Новые психоактивные вещества на основе 1,2-диарилэтиламина и кетамина». Новые психоактивные вещества . Справочник по экспериментальной фармакологии. 252 . С. 305–352. DOI : 10.1007 / 164_2018_148 . ISBN 978-3-030-10560-0. PMID 30196446 .
- ^ a b c Ахмади, А .; Махмуди, А. (2005). «Синтез и биологические свойства 2-гидрокси-1- (1-фенилтетралил) пиперидина и некоторых его промежуточных соединений как производных фенциклидина». Arzneimittel-Forschung . 55 (9): 528–532. DOI : 10,1055 / с-0031-1296900 . PMID 16229117 .
- ^ а б Ахмади, А .; Халили, М .; Гаджихани, Р .; Насербахт, М. (2011). «Новые морфолиновые аналоги фенциклидина: химический синтез и восприятие боли у крыс». Фармакология, биохимия и поведение . 98 (2): 227–233. DOI : 10.1016 / j.pbb.2010.12.019 . PMID 21215770 . S2CID 24650035 .
- ^ a b Chaudieu, I .; Виньон; Чичепортиче; Каменка; Trouiller; Чичепортиче (1989). «Роль ароматической группы в ингибировании связывания фенциклидина и захвата дофамина аналогами PCP». Фармакология, биохимия и поведение . 32 (3): 699–705. DOI : 10.1016 / 0091-3057 (89) 90020-8 . PMID 2544905 . S2CID 7672918 .
- ^ Itzhak, Y .; Саймон (1984). «Новый аналог фенциклидина избирательно взаимодействует с мю-опиоидными рецепторами». Журнал фармакологии и экспериментальной терапии . 230 (2): 383–386. PMID 6086884 .
- ^ Он, XS; Раймон, LP; Маттсон, М.В. Эльдефрави, Мэн; Де Коста, Б. Р. (1993). «Синтез и биологическая оценка гомологов 1-1- (2-бензобтиенил) циклогексилпиперидина на сайтах связывания дофамина и фенциклидин- и сигма-связывания». Журнал медицинской химии . 36 (9): 1188–1193. DOI : 10.1021 / jm00061a009 . PMID 8098066 .
- ^ Eterović, VA; Lu, R .; Икин, AE; Родригес, AD; Ферчмин, П.А. (1999). «Детерминанты активности фенциклидина на никотиновые рецепторы ацетилхолина из мышц и электрических органов». Клеточная и молекулярная нейробиология . 19 (6): 745–757. DOI : 10,1023 / A: 1006905106834 . PMID 10456235 . S2CID 22266452 .
- ^ a b Seeman, P .; Ko, F .; Таллерико, Т. (2005). «Вклад допаминовых рецепторов в действие психотомиметиков PCP, LSD и кетамина» . Молекулярная психиатрия . 10 (9): 877–883. DOI : 10.1038 / sj.mp.4001682 . PMID 15852061 .
- ^ аль-Диб, О.А. (май 1996 г.). «Новые анальгетики на основе аналога фенциклидина тиенилциклидина». Arzneimittelforschung . 46 (5): 505–8. PMID 8737636 .
- ^ Ахмади, А; Халили, М; Гаджихани, Р; Хоссейни, Н; Афшин, Н; Нари-Никнафс, Б. (2012). «Синтез и изучение обезболивающих эффектов новых аналогов кетамина на самках крыс линии Вистар». Лекарственная химия . 8 (2): 246–51. DOI : 10.2174 / 157340612800493683 . PMID 22385170 . S2CID 42842315 .
- ^ Ахмади, А; Халили, М; Аббасси, S; Джавади, М. Махмуди, А; Гаджихани, Р. (2009). «Синтез и исследование анальгетических эффектов 1-1- (4-метилфенил) (циклогексил) 4-пиперидинола и 1-1- (4-метоксифенил) (циклогексил) 4-пиперидинола как двух новых производных фенциклидина». Arzneimittel-Forschung . 59 (4): 202–6. DOI : 10,1055 / с-0031-1296386 . PMID 19517897 . S2CID 5402425 .
- ^ Ахмади, А; Халили, М; Марами, S; Гадири, А; Нари-Никнафс, Б. (2014). «Синтез и восприятие боли новых аналогов фенциклидина у мышей-самцов NMRI». Миниобзоры по медицинской химии . 14 (1): 64–71. DOI : 10.2174 / 1389557513666131119203551 . PMID 24251803 .
- ^ Ахмади, А; Солати, Дж; Гаджихани, Р; Пакзад, S (2011). «Синтез и обезболивающие эффекты новых пиррольных производных фенциклидина у мышей». Arzneimittel-Forschung . 61 (5): 296–300. DOI : 10,1055 / с-0031-1296202 . PMID 21755813 . S2CID 24287727 .
- ^ Ахмади, А; Халили; Гаджихани; Барги; Михандуст (2010). «Синтез и определение активности хронической и острой термической и химической боли нового производного фенциклидина у крыс» . Иранский журнал фармацевтических исследований . 9 (4): 379–85. PMC 3870061 . PMID 24381602 .
- ^ Ахмади, А; Халили, М; Михандуст, Ф; Барги, Л. (2010). «Синтез и определение активности острой и хронической боли 1-1- (3-метилфенил) (тетралил) пиперидина как нового производного фенциклидина с помощью иммерсии хвоста и формалиновых тестов». Arzneimittel-Forschung . 60 (1): 30–5. DOI : 10,1055 / с-0031-1296245 . PMID 20184224 . S2CID 23966936 .
- ^ Гаджихани, R; Ахмади, А; Надери, N; Yaghoobi, K; Ширазизанд, З; Rezaee, NM; Никнафс, Б.Н. (2012). «Влияние производных фенциклидина на тревожное поведение с использованием теста приподнятого крестообразного лабиринта на мышах». Успехи клинической и экспериментальной медицины . 21 (3): 307–12. PMID 23214193 .
- ^ Ахмади, А; Халили, М; Мирза, Б; Мохаммади-Диз, М. Азами-Лорестани, Ф; Ghaderi, P; Нари-Никнафс, Б. (2017). «Синтез и антиноцицепционная активность некоторых новых производных фенциклидина с замещенными аминобензотиазолами». Mini Rev Med Chem . 17 (1): 78–84. DOI : 10.2174 / 1389557516666160428112532 . PMID 27121715 .
- ^ Lednicer, D .; Вонвойгтландер, П. Ф. (1979). «4- (п-Бромфенил) -4- (диметиламино) -1-фенэтилциклогексанол, чрезвычайно мощный представитель новой серии анальгетиков». Журнал медицинской химии . 22 (10): 1157–1158. DOI : 10.1021 / jm00196a001 . PMID 513062 .
- ^ Морис, Т .; Вс, ТП; Приход, DW; Nabeshima, T .; Приват, А. (1994). «PRE-084, сигма-селективное производное PCP, ослабляет вызванное MK-801 нарушение обучения у мышей» . Фармакология, биохимия и поведение . 49 (4): 859–869. DOI : 10.1016 / 0091-3057 (94) 90235-6 . PMID 7886099 . S2CID 54306053 .
- ^ a b c Thurkauf, A .; De Costa, B .; Yamaguchi, S .; Маттсон, М.В. Якобсон, AE; Рис, KC; Рогавский, М.А. (1990). «Синтез и противосудорожная активность аналогов 1-фенилциклогексиламина». Журнал медицинской химии . 33 (5): 1452–8. DOI : 10.1021 / jm00167a027 . PMID 2329567 .
- ^ Sauer, C .; Peters, F .; Staack, R .; Fritschi, G .; Маурер, Х. (2008). «Метаболизм и токсикологическое обнаружение нового дизайнерского препарата, N- (1-фенилциклогексил) пропанамина, в моче крысы с использованием газовой хроматографии-масс-спектрометрии». Журнал хроматографии A . 1186 (1–2): 380–390. DOI : 10.1016 / j.chroma.2007.11.002 . PMID 18035363 .
- ^ Калир, А; Теомы, S; Амир, А; Fuchs, P; Lee, SA; Holsztynska, EJ; Роки, Вт; Домино, EF (октябрь 1984 г.). «N-аллильные аналоги фенциклидина: химический синтез и фармакологические свойства». J Med Chem . 27 (10): 1267–71. DOI : 10.1021 / jm00376a006 . PMID 6481761 .
- ^ Sauer, C .; Peters, F .; Schwaninger, A .; Мейер, М .; Маурер, Х. (2009). «Исследования изоферментов цитохрома P450 (CYP), участвующих в метаболизме дизайнерских наркотиков N- (1-фенилциклогексил) -2-этоксиэтанамина и N- (1-фенилциклогексил) -2-метоксиэтанамина». Биохимическая фармакология . 77 (3): 444–450. DOI : 10.1016 / j.bcp.2008.10.024 . PMID 19022226 .
- ^ Иорио, Массачусетс; Tomassini, L .; Маттсон, М.В. Джордж, С .; Якобсон, AE (1991). «Синтез, стереохимия и биологическая активность 1- (1-фенил-2-метилциклогексил) пиперидинов и 1- (1-фенил-4-метилциклогексил) пиперидинов. Абсолютная конфигурация сильнодействующих транс - (-) - 1- (1-фенил-2-метилциклогексил) пиперидин ». Журнал медицинской химии . 34 (8): 2615–2623. DOI : 10.1021 / jm00112a041 . PMID 1875352 .
- ^ Ахмади, А .; Махмуди, А. (2006). «Синтез с улучшенным выходом и исследование анальгетического эффекта 2-метоксифенциклидина». Arzneimittel-Forschung . 56 (5): 346–350. DOI : 10,1055 / с-0031-1296732 . PMID 16821645 .
- ^ а б Огунбадений AM; Адехаре, А. (2002). «Синтезы фторированных аналогов фенциклидина». Журнал химии фтора . 114 : 39–42. DOI : 10.1016 / S0022-1139 (01) 00565-6 .
- ^ a b Wallach, J .; Paoli, GD; Adejare, A .; Брандт, SD (2013). «Получение и аналитическая характеристика аналогов 1- (1-фенилциклогексил) пиперидина (PCP) и 1- (1-фенилциклогексил) пирролидина (PCPy)». Тестирование и анализ на наркотики . 6 (7–8): 633–50. DOI : 10.1002 / dta.1468 . PMID 23554350 .
- ^ Харви, М; Сани, Дж; Voss, L; Pruijn, F; Jose, J; Gamage, S; Денни, W (2015). "Определение гипнотической активности нового аналога сложного эфира кетамина SN 35210 у крыс". Фармакология . 96 (5–6): 226–32. DOI : 10.1159 / 000439598 . PMID 26352278 . S2CID 36017002 .
- ^ Ахмади А, Халили М, Hajikhani R, Naserbakht M (2011). «Синтез и определение активности острой и хронической боли 1- [1- (4-метилфенил) (циклогексил)] морфолина как нового производного фенциклидина у крыс». Arzneimittel-Forschung . 61 (2): 92–7. DOI : 10,1055 / с-0031-1296173 . PMID 21428243 .
- ^ Zarantonello, P; Bettini, E; Пайо, А; Simoncelli, C; Террени, S; Кардулло, Ф (апрель 2011 г.). «Новые аналоги кетамина и фенциклидина как антагонисты рецепторов NMDA». Bioorg Med Chem Lett . 21 (7): 2059–63. DOI : 10.1016 / j.bmcl.2011.02.009 . PMID 21334205 .
- ^ Wallach, J; Колсток, Т; Cicali, B; Elliott, SP; Кавана, П.В. Adejare, A; Демпстер, Нью-Мексико; Брандт, SD (2016). «Синтезы и аналитические характеристики N-алкил-арилциклогексиламинов» (PDF) . Анальный тест на наркотики . 8 (8): 801–815. DOI : 10.1002 / dta.1861 . PMID 26360516 .
- ^ Lednicer, D; VonVoigtlander, PF; Emmert, DE (апрель 1980 г.). «4-Амино-4-арилциклогексаноны и их производные, новый класс анальгетиков. 1. Модификация арильного кольца». J Med Chem . 23 (4): 424–30. DOI : 10.1021 / jm00178a014 . PMID 7381841 .
- ^ Ахмади, А; Солати, Дж; Гаджихани, Р; Онаг, М; Джавади, М. (2010). «Синтез и обезболивающие эффекты 1-1- (2-метилфенил) (циклогексил) -3-пиперидинола как нового производного фенциклидина у мышей». Arzneimittel-Forschung . 60 (8): 492–6. DOI : 10,1055 / с-0031-1296317 . PMID 20863005 . S2CID 24803623 .
- ^ Ицхак, Y; Калир, А; Weissman, BA; Коэн, S (1981). «Новые обезболивающие на основе фенциклидина». J Med Chem . 24 (5): 496–9. DOI : 10.1021 / jm00137a004 . PMID 7241506 .
- ^ Vignon, J .; Pinet, V .; Cerruti, C .; Каменка, Ю.М.; Chicheportiche, R. (1988). «3HN-1- (2-бензо (b) тиофенил) циклогексилпиперидин (3HBTCP): новый аналог фенциклидина, селективный для комплекса захвата дофамина». Европейский журнал фармакологии . 148 (3): 427–436. DOI : 10.1016 / 0014-2999 (88) 90122-7 . PMID 3384005 .
- ^ Он, XS; Раймон, LP; Маттсон, М.В. Эльдефрави, Мэн; de Costa, BR (апрель 1993 г.). «Синтез и биологическая оценка гомологов 1- [1- (2-бензо [b] тиенил) циклогексил] пиперидина на сайтах связывания дофамина и фенциклидин- и сигма-связывания»). J Med Chem . 36 (9): 1188–93. DOI : 10.1021 / jm00061a009 . PMID 8098066 .
- ^ Маккуинн, Рой Л. (1981). «Взаимосвязь между структурой и активностью циклоалкильного кольца фенциклидина». Журнал медицинской химии . 24 (12): 1429–1432. DOI : 10.1021 / jm00144a011 . PMID 7310819 .
- ^ Мориарти, R .; Enache, L .; Zhao, L .; Gilardi, R .; Mattson, M .; Пракаш О. (1998). «Жесткие аналоги фенциклидина. Связывание с рецепторами фенциклидина и сигма-1». Журнал медицинской химии . 41 (4): 468–477. DOI : 10.1021 / jm970059p . PMID 9484497 .
Внешние ссылки [ править ]
- Моррис, H; Уоллах, Дж (2014). «От PCP к MXE: всесторонний обзор немедицинского использования диссоциативных препаратов». Анальный тест на наркотики . 6 (7–8): 614–32. DOI : 10.1002 / dta.1620 . PMID 24678061 .
- Синтез и эффекты аналогов ПХФ
- Интервью с химиком по кетамину
