| |||
| Клинические данные | |||
|---|---|---|---|
| Торговые наименования | Олумиант, Барициникс | ||
| Другие имена | INCB28050, LY3009104 | ||
| AHFS / Drugs.com | Монография | ||
| MedlinePlus | a618033 | ||
| Данные лицензии |
| ||
Категория беременности |
| ||
| Пути администрирования | Внутрь ( таблетки ) | ||
| Код УВД | |||
| Легальное положение | |||
| Легальное положение |
| ||
| Фармакокинетические данные | |||
| Биодоступность | 79% | ||
| Связывание с белками | 50% | ||
| Метаболизм | CYP3A4 (<10%) | ||
| Ликвидация Период полураспада | 12,5 часов | ||
| Экскреция | 75% мочи, 20% фекалий | ||
| Идентификаторы | |||
| |||
| Количество CAS | |||
| PubChem CID | |||
| DrugBank | |||
| ChemSpider | |||
| UNII | |||
| КЕГГ | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| Лиганд PDB |
| ||
| CompTox Dashboard ( EPA ) |
| ||
| ECHA InfoCard | 100.219.080 | ||
| Химические и физические данные | |||
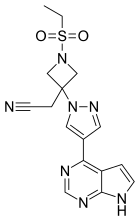
| Формула | C 16 H 17 N 7 O 2 S | ||
| Молярная масса | 371,42 г · моль -1 | ||
| 3D модель ( JSmol ) |
| ||
Улыбки
| |||
ИнЧИ
| |||
Барицитиниб , продаваемый, среди прочего, под торговой маркой Olumiant , представляет собой препарат для лечения ревматоидного артрита (РА) у взрослых, заболевание которых не контролировалось с помощью лекарств от РА, называемых антагонистами фактора некроза опухоли (TNF). [2] Он действует как ингибитор янус-киназы (JAK), блокируя подтипы JAK1 и JAK2 . [3] Препарат разрешен к применению в Европейском Союзе [4] и США. [2] [5]
Медицинское использование [ править ]
В феврале 2017 года барицитиниб был одобрен для использования в ЕС в качестве терапии второй линии при умеренном и тяжелом активном ревматоидном артрите у взрослых, отдельно или в комбинации с метотрексатом . [6] [4]
В апреле 2017 года барицитиниб получил полное ответное письмо (CRL) от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), 2017. В письме указывалось, что FDA не смогло одобрить заявку в существующей форме. В частности, FDA указало, что необходимы дополнительные клинические данные для определения наиболее подходящих доз и что дополнительные данные необходимы для дальнейшей характеристики проблем безопасности во всех группах лечения. [7]
23 апреля 2018 года Консультативный комитет FDA рекомендовал одобрить 2 мг барицитиниба для лечения ревматоидного артрита, но не рекомендовал дозу 4 мг, ссылаясь на серьезные побочные эффекты. [8] 31 мая 2018 года FDA одобрило бариктиниб для лечения взрослых пациентов с умеренно или сильно активным ревматоидным артритом, у которых был неадекватный ответ на один или несколько видов терапии антагонистами TNF. [5] [2] [9]
В ноябре 2020 года FDA выдало разрешение на использование в экстренных случаях (EUA) для комбинации барицитиниба с ремдесивиром для лечения подозреваемого или лабораторно подтвержденного COVID-19 у госпитализированных людей в возрасте двух лет и старше, которым требуется дополнительный кислород, инвазивная механическая вентиляция легких, или экстракорпоральная мембранная оксигенация (ЭКМО). [10]
Противопоказания [ править ]
Во время беременности применение барицитиниба противопоказано. [1] [6]
Побочные эффекты [ править ]
Согласно исследованиям, инфекции верхних дыхательных путей и высокий уровень холестерина в крови ( гиперхолестеринемия ) наблюдались более чем у 10% пациентов. Менее распространенные побочные эффекты включали другие инфекции, такие как опоясывающий лишай , простой герпес , инфекции мочевыводящих путей и гастроэнтерит . [6]
Взаимодействия [ править ]
Будучи усвоен лишь в небольшой степени, вещество обладает низким потенциалом взаимодействия. В исследованиях ингибиторы ферментов печени CYP3A4 , CYP2C19 и CYP2C9 , а также индуктор CYP3A4 рифампицин не оказали значимого влияния на концентрацию барицитиниба в кровотоке. Хотя барицитиниб блокирует ряд белков-переносчиков in vitro , клинически значимые взаимодействия через этот механизм считаются очень маловероятными, за исключением, возможно, переносчика катионов SLC22A1 (OCT1). [6]
Не исключен аддитивный эффект с другими иммунодепрессантами . [6]
Фармакология [ править ]
Механизм действия [ править ]
Барицитиниб представляет собой ингибитор янус-киназы (JAK), который обратимо ингибирует янус-киназу 1 с половинной максимальной ингибирующей концентрацией (IC 50 ) 5,9 нМ и янус-киназу 2 с IC 50 5,7 нМ. Тирозинкиназа 2 , принадлежащая к тому же семейству ферментов, подвержена меньшему влиянию (IC 50 = 53 нМ), а киназа Януса 3 гораздо меньше (IC 50 > 400 нМ). Через путь передачи сигнала с участием белков STAT это в конечном итоге модулирует экспрессию генов в иммунологических клетках. [6]
Другие ингибиторы JAK включают тофацитиниб , который показан для лечения ревматоидного артрита, псориатического артрита и язвенного колита; [11] [12] федратиниб , [13] и руксолитиниб . [14] [15]
Фармакокинетика [ править ]
Вещество быстро всасывается из кишечника с абсолютной биодоступностью 79%. Он достигает наивысшего уровня в плазме крови примерно через час; у разных людей время достижения этого уровня колеблется от 0,5 до 3 часов. Прием пищи не оказывает существенного влияния на фармакокинетику препарата. 50% циркулирующего барицитиниба связывается с белками плазмы крови . [6]
Менее 10% этого вещества метаболизируется CYP3A4 до четырех различных продуктов окисления; остальное оставлено без изменений. Период полувыведения составляет в среднем 12,5 часов. Около 75% выводится с мочой и 20% с фекалиями . [6]
История [ править ]
По состоянию на август 2016 г. [Обновить]было зарегистрировано 31 клиническое испытание барицитиниба, из которых 24 были завершены [16] и 4 из 6 испытаний фазы 3 завершены. [17] [ требуется обновление ]
COVID-19 [ править ]
В апреле 2020 года Lilly объявила, что исследует возможность использования барицитиниба для лечения пациентов с COVID-19 . Ожидается, что противовоспалительная активность препарата будет влиять на воспалительный каскад, связанный с COVID-19. [18]
В ноябре 2020 года опубликованное исследование показало, что барцитиниб эффективен при лечении пациентов с COVID-19. Согласно статье, «механистические действия ингибитора Янус-киназы-1/2, направленные на проникновение вируса, репликацию и цитокиновый шторм, связаны с благоприятными исходами, в том числе у тяжело больных пожилых пациентов». [19]
В клиническом исследовании госпитализированных пациентов с COVID-19 было показано, что барицитиниб в комбинации с ремдесивиром сокращает время до выздоровления в течение 29 дней после начала лечения по сравнению с пациентами, которые получали плацебо с ремдесивиром. [10] Безопасность и эффективность этой экспериментальной терапии для лечения COVID-19 продолжают оцениваться. [10] Барицитиниб не разрешен и не одобрен в качестве самостоятельного средства для лечения COVID-19. [10]
Данные, подтверждающие разрешение FDA на экстренное использование барицитиниба в сочетании с ремдесивиром, основаны на рандомизированном двойном слепом плацебо-контролируемом клиническом исследовании (ACTT-2), проведенном Национальным институтом аллергии и инфекционных заболеваний США. Заболевания (НИАЗД). [10] В этом клиническом исследовании оценивалось, влияет ли барицитиниб на то, сколько времени требуется пациентам, которые также принимали ремдесивир, на выздоровление от COVID-19. [10] В испытании наблюдали за пациентами в течение 29 дней и включили 1033 пациента с умеренным или тяжелым COVID-19; 515 пациентов получали барицитиниб плюс ремдесивир и 518 пациентов получали плацебо плюс ремдесивир. [10]Выздоровление определялось как выписка из больницы или госпитализация, но без дополнительного кислорода и постоянной медицинской помощи. [10] Среднее время выздоровления от COVID-19 составляло семь дней для барицитиниба и ремдесивира и восемь дней для плацебо и ремдесивира. [10] Вероятность прогрессирования состояния пациента до смерти или искусственной вентиляции легких на 29 день была ниже в группе барицитиниба плюс ремдесивир по сравнению с группой плацебо плюс ремдесивир. [10] Вероятность клинического улучшения на 15-й день была выше в группе барицитиниба плюс ремдесивир по сравнению с группой плацебо плюс ремдесивир. [10] Для всех этих конечных точек эффекты были статистически значимыми. [10]EUA была выдана Eli Lilly and Company . [10]
В ноябре 2020 года Всемирная организация здравоохранения (ВОЗ) обновила свое руководство по лечению COVID-19, включив в него условную рекомендацию против использования ремдесивира, основанную на результатах исследования ВОЗ Solidarity . [20] [21]
Общество и культура [ править ]
Правовой статус [ править ]
В январе 2016 года Eli Lilly подала новую заявку на лекарство в Управление по контролю за продуктами и лекарствами США (FDA) для одобрения барицитиниба для лечения умеренно-тяжелого активного ревматоидного артрита. [22]
В декабре 2016 года Комитет по лекарственным средствам для человека (CHMP) Европейского агентства по лекарственным средствам (EMA) рекомендовал одобрить барицитиниб в качестве средства лечения ревматоидного артрита. [3] Разрешение Европейского Союза было получено в феврале 2017 года. [4]
Несмотря на широко распространенные ожидания, что FDA одобрит барицитиниб для лечения ревматоидного артрита [23] в апреле 2017 года, FDA выпустило отказ, сославшись на опасения по поводу дозировки и безопасности. [24] [25]
В мае 2018 года барицитиниб был одобрен в США для лечения ревматоидного артрита. [8] [2] [5]
В марте 2020 года FDA США присвоило барицитинибу статус прорывной терапии для лечения очаговой алопеции . [26]
Торговые марки [ править ]
В Бангладеш препарат продается, среди прочего, под торговыми марками Baricinix и Baricent (Incepta Pharma). [ необходима цитата ]
Ссылки [ править ]
- ^ a b c «Использование барицитиниба (олумианта) во время беременности» . Drugs.com . 8 ноября 2019 . Дата обращения 16 марта 2020 .
- ^ a b c d "Снимки испытаний лекарств: Olumiant" . США пищевых продуктов и медикаментов (FDA) . 31 мая 2018 . Дата обращения 16 марта 2020 .
 Эта статья включает текст из этого источника, который находится в общественном достоянии .
Эта статья включает текст из этого источника, который находится в общественном достоянии . - ^ a b "Краткое изложение мнения Olumiant" (PDF) . Европейское агентство по лекарственным средствам (EMA). 15 декабря 2016 г.
- ^ a b c "Olumiant EPAR" . Европейское агентство по лекарственным средствам (EMA). 3 декабря 2019.Текст был скопирован из этого источника © European Medicines Agency. Воспроизведение разрешено при условии указания источника.
- ^ a b c «Пакет одобрения лекарств: Olumiant (барицитиниб)» . США пищевых продуктов и медикаментов (FDA) . 5 июля 2018 . Дата обращения 16 марта 2020 .
- ^ a b c d e f g h "Olumiant: EPAR - Информация о продукте" (PDF) . Европейское агентство по лекарственным средствам . 13 февраля 2017.
- ^ Тхань Хай, Мэри Т. «ПОЛНЫЙ ОТВЕТ» (PDF) . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов . Проверено 14 декабря 2020 года .
- ^ a b Информационный документ FDA - Заседание Консультативного комитета по артриту
- ^ «Олумиант - таблетка барицитиниба, покрытая пленочной оболочкой» . DailyMed . 13 ноября 2019 . Дата обращения 16 марта 2020 .
- ^ a b c d e f g h i j k l m «Обновление коронавируса (COVID-19): FDA разрешает комбинацию лекарств для лечения COVID-19» . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (пресс-релиз). 19 ноября 2020 . Дата обращения 19 ноября 2020 .
 Эта статья включает текст из этого источника, который находится в общественном достоянии .
Эта статья включает текст из этого источника, который находится в общественном достоянии . - ^ "Ксельянц-тофацитиниб таблетка, покрытая пленкой Таблетка Ксельянц XR-тофацитиниб, покрытая пленкой, пролонгированного высвобождения" . DailyMed . 20 декабря 2019 . Проверено 28 апреля 2020 .
- ^ «FDA одобряет Xeljanz для лечения ревматоидного артрита» (пресс-релиз). 6 ноября 2012 г.
- ^ «Инребик-федратиниб гидрохлорид в капсулах» . DailyMed . 16 августа 2019 . Проверено 28 апреля 2020 .
- Перейти ↑ Mesa RA (июнь 2010 г.). «Руксолитиниб, селективный ингибитор JAK1 и JAK2 для лечения миелопролиферативных новообразований и псориаза». ID наркотиков . 13 (6): 394–403. PMID 20506062 .
- ^ «Таблетка Джакафируксолитиниба» . DailyMed . 26 февраля 2020 . Проверено 28 апреля 2020 .
- ^ «Клинические испытания барицитиниба» . ClinicalTrials.gov .
- ^ «Фаза 3 клинических испытаний барицитиниба» . ClinicalTrials.gov .
- ^ «Eli Lilly для изучения барицитиниба для лечения Covid-19» . Арена клинических испытаний .
- ^ Стеббинг Дж., Санчес Ниевас Дж., Фальконе М, Юханна С., Ричардсон П., Оттавиани С. и др. (Ноябрь 2020 г.). «Ингибирование JAK снижает инфекционность печени SARS-CoV-2 и модулирует воспалительные реакции для снижения заболеваемости и смертности» . Sci Adv : eabe4724. DOI : 10.1126 / sciadv.abe4724 . PMID 33187978 .
- ^ Всемирная организация здравоохранения (2020). Терапия и COVID-19: руководство по жизни, 20 ноября 2020 г. Всемирная организация здравоохранения (ВОЗ) (отчет). ЛВП : 10665/336729 . WHO / 2019-nCov / remdesivir / 2020.1.
- ^ Lamontagne F, Agoritsas T, Macdonald H, Leo YS, Diaz J, Agarwal A и др. (Сентябрь 2020 г.). «Действующее руководство ВОЗ по лекарствам от covid-19» . BMJ . 370 : m3379. DOI : 10.1136 / bmj.m3379 . PMID 32887691 . Выложите резюме .
- ^ «Lilly и Incyte объявляют о подаче NDA в FDA для перорального приема барицитиниба один раз в день для лечения от умеренного до тяжелого ревматоидного артрита» . Drugs.com . 19 января 2016 г.
- ^ Кэрролл J (13 апреля 2017 г.). «Мы не знаем, когда (точно) Lilly объявит о решении FDA по барицитинибу, но остерегайтесь надвигающейся споры о ценах» . Новости конечных точек.
- ↑ Ramsey L (17 апреля 2017 г.). «FDA уничтожило новое лекарство от ревматоидного артрита, и компании, производящие это лекарство, падают» . Business Insider.
- ↑ Grant C (14 апреля 2017 г.). «Неожиданный отказ FDA укусит эту биотехнологию» . The Wall Street Journal .
- ^ «Lilly получает от Управления по контролю за продуктами и лекарствами США назначение барицитиниба для лечения очаговой алопеции» (пресс-релиз). Эли Лилли и компания. 16 марта 2020 . Проверено 16 марта 2020 г. - через PR Newswire.
Дальнейшее чтение [ править ]
- Cingolani A, Tummolo AM, Montemurro G, Gremese E, Larosa L, Cipriani MC и др. (2020). «Барицитиниб в качестве терапии спасения у пациента с COVID-19 без полного ответа на сарилумаб» . Инфекция . 48 (5): 767–771. DOI : 10.1007 / s15010-020-01476-7 . PMC 7340855 . PMID 32642806 .
- Jorgensen SCJ, Tse CLY, Burry L, Dresser LD (2020). «Барицитиниб: обзор фармакологии, безопасности и нового клинического опыта лечения COVID-19» . Фармакотерапия . 40 (8): 843–856. DOI : 10.1002 / phar.2438 . PMC 7323235 . PMID 32542785 .
- Калил А.С., Паттерсон Т.Ф., Мехта А.К., Томашек К.М., Вулф К.Р., Казарян В. и др. (2020). «Барицитиниб плюс ремдесивир для госпитализированных взрослых с Covid-19» . Медицинский журнал Новой Англии . DOI : 10.1056 / NEJMoa2031994 . PMC 7745180 . PMID 33306283 .
- Сеиф Ф., Аазами Х., Хошмирсафа М., Камали М., Мохсензадеган М., Порнур М. и др. (2020). «Ингибирование JAK как новая стратегия лечения пациентов с COVID-19» . Международный архив аллергии и иммунологии . 181 (6): 467–475. DOI : 10.1159 / 000508247 . PMC 7270061 . PMID 32392562 .
- Стеббинг Дж., Кришнан В., Де Боно С., Оттавиани С., Казалини Дж., Ричардсон П. Дж. И др. (2020). «Механизм барицитиниба поддерживает предсказанное искусственным интеллектом тестирование у пациентов с COVID-19» . EMBO Молекулярная медицина . 12 (8): e12697. DOI : 10.15252 / emmm.202012697 . PMC 7300657 . PMID 32473600 .
- Чжан X, Чжан И, Цяо В., Чжан Дж, Ци З (2020). «Барицитиниб, лекарство с потенциальным эффектом для предотвращения проникновения SARS-COV-2 в клетки-мишени и контроля цитокинового шторма, вызванного COVID-19» . Международная иммунофармакология . 86 : 106749. дои : 10.1016 / j.intimp.2020.106749 . PMC 7328558 . PMID 32645632 .
Внешние ссылки [ править ]
- «Барицитиниб» . Информационный портал о наркотиках . Национальная медицинская библиотека США.