| Перестановка Бекмана | |
|---|---|
| Названный в честь | Эрнст Отто Бекманн |
| Тип реакции | Реакция перестановки |
| Идентификаторы | |
| Портал органической химии | перестановка Бекмана |
| Идентификатор онтологии RSC | RXNO: 0000026 |
Перегруппировки Бекмана , названные в честь немецкого химика Эрнста Отто Бекман (1853-1923), является перегруппировкой из оксима функциональной группы в замещенные амиды . [1] [2] Перегруппировка также была успешной выполнена на haloimines и нитронах . Циклические оксимы и галоимины дают лактамы .
Перегруппировка Бекмана часто катализируется кислотой, однако известно, что другие реагенты способствуют перегруппировке. Они включают тозил хлорид , тионил хлорид , пентахлорид фосфора , пентаоксид фосфора , триэтиламин , гидроксид натрия , триметилсилил йодида среди других. [3] фрагментации Бекман еще одна реакция , которая часто конкурирует с перестройкой, хотя тщательный отбор продвижения реагента и условий растворителей может способствовать образованию одного над другим, иногда дает почти исключительно один продукт. Перестройка происходит стереоспецифично.для кетоксимов и N-хлор / N-фториминов, при этом мигрирующая группа является антиперипланарной по отношению к уходящей группе на азоте. Известно, что определенные условия рацемизируют геометрию оксима, приводя к образованию обоих региоизомеров . Перегруппировка альдоксимов происходит со стереоспецифичностью в газовой фазе и без стереоспецифичности в фазе раствора. Несколько методологий позволяют перегруппировать альдоксимы в первичные амиды, но в этих системах обычно конкурирует фрагментация. Перегруппировка нитронов также происходит без стереоспецифичности; образованный региоизомер имеет амидный азот, замещенный группой, обладающей наибольшиммиграционная способность .
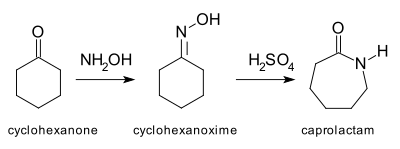
Типичной перегруппировкой Бекмана [4] является превращение циклогексанона в капролактам через оксим. Капролактам является сырьем для производства нейлона 6 . [5]
Раствор Бекмана состоит из уксусной кислоты , соляной кислоты и уксусного ангидрида , и широко используется в качестве катализатора перегруппировки. Были использованы другие кислоты, такие как серная кислота , полифосфорная кислота и фтороводород . Серная кислота является наиболее часто используемой кислотой для промышленного производства лактама из-за образования побочного продукта сульфата аммония при нейтрализации аммиаком . Сульфат аммония - обычное сельскохозяйственное удобрение, обеспечивающее азот и серу.
Механизм реакции [ править ]
Наиболее распространенный механизм реакции перегруппировки Бекмана состоит, как правило, из антиперипланарной миграции алкила с вытеснением уходящей группы с образованием иона нитрилия . За этим следует сольволиз до имидата и затем таутомеризация до амида: [6]
Этот ион нитрилия, как известно, перехватывается другими нуклеофилами, включая уходящую группу из оксима. [3]
Предположительно, после того, как фенильная группа мигрирует и вытесняет цианат , она атакует образовавшийся ион нитриллия. В четыреххлористе углерода изоцианат может быть выделен, тогда как в этаноле уретан образуются после сольволиза изоцианата.
Одно вычислительное исследование установило механизм, учитывающий молекулы растворителя и заместители. [7] В перегруппировке оксима ацетона в растворе Бекмана участвовали три молекулы уксусной кислоты и один протон (присутствующий как ион оксония ). В переходном состоянии, ведущем к иону иминия (σ-комплекс), метильная группа мигрирует к атому азота в согласованной реакциипоскольку гидроксильная группа удаляется. Атом кислорода в гидроксильной группе стабилизирован тремя молекулами уксусной кислоты. На следующем этапе электрофильный атом углерода в ионе нитрилия подвергается атаке воды, и протон возвращается обратно в уксусную кислоту. В переходном состоянии, ведущем к имидату, атом кислорода воды координирован с 4 другими атомами. На третьей стадии стадия изомеризации протонирует атом азота, приводящий к амиду .
Тот же расчет с ионом гидроксония и 6 молекулами воды дает тот же результат, но когда мигрирующий заместитель представляет собой фенильную группу, механизм способствует образованию промежуточного трехчленного π-комплекса. Этот π-комплекс не находится в H 3 O + (H 2 O) 6 .
С циклогексаноноксимом снятие напряжения кольца приводит к третьему механизму реакции, ведущему непосредственно к протонированному капролактаму за одну согласованную стадию без промежуточного образования π-комплекса или σ-комплекса.
Цианур хлорид помог реакции Бекмана [ править ]
Перегруппировка Бекмана может быть сделана каталитической с использованием хлорида циануровой кислоты и хлорида цинка в качестве сокатализатора . Например, циклододеканон можно превратить в соответствующий лактам , мономер, используемый при производстве нейлона 12 . [8] [9]
Механизм реакции для данной реакции основан на каталитическом цикл с цианурхлоридом активации гидроксильной группы с помощью нуклеофильного ароматического замещения . Продукт реакции вытесняется и заменяется новым реагентом через промежуточный комплекс Мейзенгеймера .
Фрагментация Бекмана [3] [ править ]
Фрагментация Бекмана - это реакция, которая часто конкурирует с перегруппировкой Бекмана. Когда группа α оксима способна стабилизировать образование карбокатиона , фрагментация становится жизнеспособным путем реакции. В результате реакции образуются нитрил и карбокатион, которые быстро перехватываются с образованием различных продуктов. Нитрил также можно гидролизовать в условиях реакции с образованием карбоновых кислот . Различные условия реакции могут способствовать фрагментации, а не перегруппировке.
Центры четвертичного углерода способствуют фрагментации, стабилизируя образование карбокатиона посредством гиперконъюгации . Как показано на рисунке выше, образуется «стабильный» карбокатион, который затем теряет водород, образуя участок ненасыщенности . Атомы кислорода и азота также способствуют фрагментации за счет образования кетонов и иминов соответственно.
Сера также способна способствовать фрагментации, хотя и в более длительном диапазоне, чем кислород или азот.
Кремний способен направлять фрагментацию через эффект бета-кремния .
Промежуточный карбокатион в этой реакции перехватывается нуклеофильным фторидом из трифторида диэтиламиносеры ( DAST ): [10]
Реакция Семмлера – Вольфа [ править ]
Оксим циклогексенона с кислотой образует анилин в реакции дегидратации- ароматизации, называемой реакцией Семмлера-Вольфа или ароматизацией Вольфа [11] [12] [13] [14]
Механизм можно представить следующим образом:
По сути, реакция является частным случаем перегруппировки Бекмана в сочетании с участием соседней группы .
Применение в синтезе лекарств [ править ]
В этом разделе не процитировать любые источники . ( Декабрь 2017 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
- Этот маршрут также включает перестановку Бекмана.
Промышленный синтез парацетамола , разработанный Hoechst - Celanese предполагает превращение метилового эфира кетона к ацетанилидному через перегруппировку Бекмана. [15]
Перегруппировка Бекмана также используется в синтезе DHEA , беназеприла , цефоранида , эланзепина , 17-азапрогестерона , элантрина , празепина , энпразепина и этазепина .
См. Также [ править ]
- Перестановка Курция
- Реакция Дакина
- Реакция Шмидта
- Перестановка Штиглица
- Перегруппировка Лоссена
Ссылки [ править ]
- ^ Бекманн, Э. (1886). "Zur Kenntniss der Isonitrosoverbindungen" [О [наших] знаниях изонитрозосоединений]. Berichte der Deutschen Chemischen Gesellschaft . 19 : 988–993. DOI : 10.1002 / cber.188601901222 .
- ^ Донарума, LG; Heldt, WZ (1960). «Перестановка Бекмана. (Рецензия)». Орг. Реагировать . 11 : 1–156.
- ^ a b c Гоули, RE (1988). «Реакции Бекмана: перегруппировка, добавление отщепления, фрагментация и перегруппировка-циклизация. (Обзор)». Орг. Реагировать . 35 : 14–24.
- ^ Эк, JC; Марвел, CS (1939). «Ε-Бензоиламинокапроновая кислота» . Органический синтез . 19 : 20. DOI : 10,15227 / orgsyn.019.0020 . Архивировано из оригинала на 2012-09-28 . Проверено 18 августа 2005 .Eck, JC; Марвел, CS (1943). «Ε-Бензоиламинокапроновая кислота» . Органический синтез . 2 : 76. Архивировано из оригинала на 2012-09-28 . Проверено 18 августа 2005 .
- ↑ Йозеф Ритц; Хьюго Фукс; Хайнц Кечка; Уильям С. Моран. «Капролактам». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a05_031.pub2 .
- ^ Лескано-Гонсалес, Инес; Боронат, Мерседес; Бласко, Тереза (апрель 2009 г.). «Исследование реакции перегруппировки Бекмана, катализируемой пористыми твердыми телами: MAS ЯМР и теоретические расчеты». Ядерный магнитный резонанс твердого тела . 35 (2): 120–129. DOI : 10.1016 / j.ssnmr.2009.02.001 . PMID 19286355 .
- ^ Yamabe, S .; Tsuchida, N .; Ямазаки, С. (2005). «Является ли перестановка Бекмана согласованной или ступенчатой реакцией? Вычислительное исследование» . Журнал органической химии . 70 (26): 10638–10644. DOI : 10.1021 / jo0508346 . PMID 16355980 .
- ^ Furuya, Y .; Ishihara, K .; Ямамото, Х. (2005). «Хлорид циануровой кислоты как мягкий и активный катализатор перегруппировки Бекмана» . Журнал Американского химического общества . 127 (32): 11240–11241. DOI : 10.1021 / ja053441x . PMID 16089442 .
- ^ Табер, Дуглас Ф .; Стрейни, Патрик Дж. (2010). «Синтез лауролактама из циклододеканона с помощью перегруппировки Бекмана». J. Chem. Educ . 87 (12): 1392. Bibcode : 2010JChEd..87.1392T . DOI : 10.1021 / ed100599q . S2CID 96699202 .
- ^ Кирихара, Масаюки; Ниими, Канако; Момосе, Такефуми (1997). «Фторирование-расщепление циклических кетоксимов трифторидом диэтиламиносеры: эффективный синтез фторированных карбонитрилов». Химические коммуникации . 6 (6): 599–600. DOI : 10.1039 / a607749h .
- ^ W. Semmler, Ber. 25, 3352 (1892)
- ↑ L. Wolff, Amp. 322, 351 (1902)
- ^ Назовите реакции и реагенты в органическом синтезе , Брэдфорд П. Манди, Майкл Г. Эллерд, Фрэнк Г. Фавалоро
- ^ Перестройки Бекмана. Расследование особых случаев EC Horning, VL Stromberg, HA Lloyd J. Am. Chem. Soc. , 1952 , 74 (20), стр 5153-5155 DOI : 10.1021 / ja01140a048
- ^ Патент США 5155273 , Fritch , John R. (Corpus Christi, TX); Фручи, Стэнли О. (Бад-Соден / ТС, Германия); Хорленко, Теодор (Корпус-Кристи, Техас); Агилар, Даниэль А. (Корпус-Кристи, Техас); Хилтон, Чарльз Б. (Корпус-Кристи, Техас); Снайдер, Филип С. (Рок-Хилл, Южная Каролина); Силигер, Уильям Дж. (Корпус-Кристи, Техас), «Производство парацетамола», опубликовано 13 октября 1992 г., передано Hoechst Celanese Corporation (Сомервилль, Нью-Джерси)
Внешние ссылки [ править ]
- Анимация перестановки Бекмана
- Анимация перегруппировки Бекмана (капролактам)