 | |
 | |
| Имена | |
|---|---|
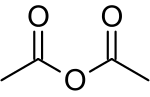
| Предпочтительное название IUPAC Уксусный ангидрид | |
| Систематическое название ИЮПАК Этановый ангидрид | |
| Другие имена Этаноил этаноат Уксусного ангидрид кислота Ацетил ацетат Ацетил оксид Уксусной оксида | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.003.241 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1715 |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| С 4 Н 6 О 3 | |
| Молярная масса | 102,089 г · моль -1 |
| Внешность | бесцветная жидкость |
| Плотность | 1,082 г см −3 , жидкость |
| Температура плавления | -73,1 ° С (-99,6 ° F, 200,1 К) |
| Точка кипения | 139,8 ° С (283,6 ° F, 412,9 К) |
| 2,6 г / 100 мл, см. Текст | |
| Давление газа | 4 мм рт. Ст. (20 ° C) [1] |
| -52,8 · 10 −6 см 3 / моль | |
Показатель преломления ( n D ) | 1,3901 |
| Фармакология | |
| Легальное положение | |
| Опасности | |
| Паспорт безопасности | ICSC 0209 |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасность |
Формулировки опасности GHS | H226 , H302 , H314 , H332 |
Меры предосторожности GHS | Р210 , Р233 , Р240 , Р241 , P242 , P243 , P260 , P261 , P264 , P270 , P271 , P280 , P301 + 312 , P301 + 330 + 331 , P303 + 361 + 353 , Р304 + 312 , Р304 + 340 , P305 + 351 + 338 , P310 , P312 , P321 , P330 , P363 , P370 + 378 , P403 + 235 |
| NFPA 704 (огненный алмаз) |  2 3 1 W |
| точка возгорания | 49 ° С (120 ° F, 322 К) |
самовоспламенения температуру | 316 ° С (601 ° F, 589 К) |
| Пределы взрываемости | 2,7–10,3% |
| Смертельная доза или концентрация (LD, LC): | |
ЛК 50 ( средняя концентрация ) | 1000 частей на миллион (крыса, 4 часа) [2] |
| NIOSH (пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 5 частей на миллион (20 мг / м 3 ) [1] |
REL (рекомендуется) | C 5 частей на миллион (20 мг / м 3 ) [1] |
IDLH (Непосредственная опасность) | 200 страниц в минуту [1] |
| Родственные соединения | |
Родственные ангидриды кислот | Пропионовый ангидрид |
Родственные соединения | Уксусная кислота Ацетилхлорид |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Уксусный ангидрид , или этановая ангидрид , является химическое соединение с формулой (СН 3 СО) 2 О. Обычно сокращенно Ас 2 О, это самый простой выдел емый ангидрид из карбоновой кислоты и широко используется в качестве реагента в органическом синтезе . Это бесцветная жидкость с сильным запахом уксусной кислоты , которая образуется в результате реакции с влагой в воздухе.
Структура и свойства [ править ]
Уксусный ангидрид, как и большинство ангидридов кислот, представляет собой гибкую молекулу с неплоской структурой. [3] пи система связи через центральные предложения кислорода очень слабая стабилизация резонанса по сравнению с диполь-дипольного отталкивания между двумя карбонильными атомами кислорода. Энергетические барьеры для вращения связи между каждой из оптимальных апланарных конформаций довольно низки. [4]
Как и большинство ангидридов кислот, карбонильный атом углерода уксусного ангидрида имеет электрофильный характер , так как уходящей группой является карбоксилат . Внутренняя асимметрия может способствовать сильной электрофильности уксусного ангидрида, поскольку асимметричная геометрия делает одну сторону карбонильного атома углерода более реакционной, чем другую, и при этом имеет тенденцию консолидировать электроположительность карбонильного атома углерода с одной стороны (см. Диаграмму электронной плотности ).
Производство [ править ]
Уксусный ангидрид был впервые синтезирован в 1852 году французским химиком Шарлем Фредериком Герхардтом (1816-1856) путем нагревания ацетата калия с бензоилхлоридом . [5]
Уксусный ангидрид получают путем карбонилирования из метилацетата : [6]
- CH 3 CO 2 CH 3 + CO → (CH 3 CO) 2 O
Процесс с уксусным ангидридом Tennessee Eastman включает превращение метилацетата в метилиодид и ацетатную соль. Карбонилирование метилиодида, в свою очередь, дает ацетилиодид , который реагирует с солями ацетата или уксусной кислотой с образованием продукта. В качестве катализаторов используется хлорид родия в присутствии иодида лития . Поскольку уксусный ангидрид нестабилен в воде, превращение проводят в безводных условиях.
В меньшей степени уксусный ангидрид получают также реакцией кетена ( этенона ) с уксусной кислотой при 45–55 ° C и низком давлении (0,05–0,2 бар). [7]
- H 2 C = C = O + CH 3 COOH → (CH 3 CO) 2 O (Δ H = −63 кДж / моль)
Путь от уксусной кислоты до уксусного ангидрида через кетен был разработан Wacker Chemie в 1922 году [8], когда потребность в уксусном ангидриде увеличилась из-за производства ацетата целлюлозы .
Из-за низкой стоимости уксусный ангидрид обычно покупается, а не готовится для использования в исследовательских лабораториях.
Реакции [ править ]
Уксусный ангидрид - универсальный реагент для ацетилирования , введения ацетильных групп в органические субстраты. [9] В этих преобразованиях уксусный ангидрид рассматривается как источник CH 3 CO + .
Ацетилирование спиртов и аминов [ править ]
Спирты и амины легко ацетилируются. [10] Например, реакция уксусного ангидрида с этанолом дает этилацетат :
- (CH 3 CO) 2 O + CH 3 CH 2 OH → CH 3 CO 2 CH 2 CH 3 + CH 3 COOH
Часто для функционирования в качестве катализатора добавляют основание, такое как пиридин . В специализированных областях применения кислотные соли скандия Льюиса также оказались эффективными катализаторами. [11]
Ацетилирование ароматических колец [ править ]
Ароматические кольца ацетилированы уксусным ангидридом. Обычно для ускорения реакции используют кислотные катализаторы. Показательными являются превращения бензола в ацетофенон [12] и ферроцена в ацетилферроцен: [13]
- (C 5 H 5 ) 2 Fe + (CH 3 CO) 2 O → (C 5 H 5 ) Fe (C 5 H 4 COCH 3 ) + CH 3 CO 2 H
Получение других ангидридов кислот [ править ]
Дикарбоновые кислоты превращаются в ангидриды при обработке уксусным ангидридом. [14] Он также используется для приготовления смешанных ангидридов, таких как ангидриды с азотной кислотой и ацетилнитратом .
Предшественник геминальных диацетатов [ править ]
Альдегиды реагируют с уксусным ангидридом в присутствии кислотного катализатора с образованием геминальных диацетатов. [15] Прежний промышленный путь получения винилацетата включал промежуточный этилидендиацетат , геминальный диацетат, полученный из ацетальдегида и уксусного ангидрида: [16]
- CH 3 CHO + (CH 3 CO) 2 O → (CH 3 CO 2 ) 2 CHCH 3
Гидролиз [ править ]
Уксусный ангидрид растворяется в воде примерно до 2,6% по весу. [17] Водные растворы обладают ограниченной стабильностью, поскольку, как и большинство ангидридов кислот, уксусный ангидрид гидролизуется с образованием карбоновых кислот. В этом случае образуется уксусная кислота, продукт реакции полностью смешивается с водой: [18]
- (CH 3 CO) 2 O + H 2 O → 2 CH 3 CO 2 H
Приложения [ править ]
Как показывает его органический химический состав, уксусный ангидрид в основном используется для ацетилирования, что приводит к получению коммерчески значимых материалов. Его наибольшее применение - преобразование целлюлозы в ацетат целлюлозы , который является компонентом фотопленки и других материалов с покрытием и используется при производстве сигаретных фильтров. Точно так же он используется при производстве аспирина (ацетилсалициловой кислоты), который получают ацетилированием салициловой кислоты . [19] Он также используется в качестве консерванта для древесины путем пропитки в автоклаве, чтобы сделать древесину более долговечной.
В крахмальной промышленности уксусный ангидрид является распространенным соединением ацетилирования, используемым для производства модифицированных крахмалов (E1414, E1420, E1422).
Из-за его использования для синтеза героина путем диацетилирования морфина уксусный ангидрид внесен в список предшественников US DEA List II и ограничен во многих других странах. [20]
Безопасность [ править ]
Уксусный ангидрид - раздражающая и горючая жидкость. Из-за его реакционной способности к воде для тушения пожара предпочтительны спиртовая пена или диоксид углерода. [21] Пары уксусного ангидрида вредны. [22]
Ссылки [ править ]
- ^ a b c d Карманный справочник NIOSH по химической опасности. «# 0003» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ «Уксусный ангидрид» . Немедленно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Зайдель, RW; Goddard, R .; Nöthling, N .; Леман, CW (2016), "Уксусный ангидрид при 100 К: при первом определении кристаллической структуры", Acta Crystallographica секции С , 72 (10): 753-757, DOI : 10.1107 / S2053229616015047 , PMID 27703123 .
- ^ Ву, Гуан; Van Alsenoy, C .; Geise, HJ; Слуйц, Э .; Ван Дер Векен, Б. Дж.; Шишков И.Ф .; Христенко (2000), «Уксусный ангидрид в газовой фазе, изученный методами электронной дифракции и инфракрасной спектроскопии, дополненный расчетами геометрии и силовых полей ab Initio», The Journal of Physical Chemistry A , 104 (7): 1576–1587, doi : 10.1021 / jp993131z .
- ^ Чарльз Герхардт (1852) «Recherches sur les acides organiques anhydres» (Исследования ангидридов органических кислот), Comptes rendus …, 34 : 755-758.
- ^ Zoeller, JR; Agreda, VH; Cook, SL; Лафферти, Нидерланды; Полихновский, SW; Pond, DM (1992), "Процесс уксусного ангидрида компании Eastman Chemical", Catal. Сегодня , 13 (1): 73–91, doi : 10.1016 / 0920-5861 (92) 80188-S
- ^ Arpe, Hans-Jürgen (2007-01-11), Industrielle Organische Chemie: Bedeutende vor- унд Zwischenprodukte (6 - е изд.), Weinheim: Wiley-VCH, стр 200-1,. ISBN 978-3-527-31540-6.
- ↑ Вехи в истории WACKER , Wacker Chemie AG , данные получены 27 августа 2009 г..
- ^ "Acid Anhydrides" , Understanding Chemistry , извлечено 25 марта 2006 г..
- ^ Shakhashiri, Bassam З., «уксусная кислота и уксусный ангидрид» , Наука Fun ... , Химический факультет, Университет штата Висконсин, архив с оригинала на 2006-03-03 , извлекаться 2006-03-25.
- ^ Макор, Джон; Сампоньяро, Энтони Дж .; Верхоест, Патрик Р .; Мак, Роберт А. (2000). «( R ) - (+) - 2-гидрокси-1,2,2-трифенилэтил ацетат» . Органический синтез . 77 : 45. DOI : 10,15227 / orgsyn.077.0045 .; Сборник , 10 , стр. 464
- ^ Роджер Адамс и CR Noller "p-Bromoacetophenone" Org. Synth. 1925, т. 5, стр. 17. doi : 10.15227 / orgsyn.005.0017
- ^ Табер, Дуглас Ф., Колоночная хроматография: Получение ацетил-ферроцена , Департамент химии и биохимии, Университет Делавэра, заархивировано из оригинала 02 мая 2009 г. , извлечено 27 августа 2009 г..
- ^ BH Nicolet и JA Bender "3-нитрофталевый ангидрид" Org. Synth. 1927, т. 7, 74. doi : 10.15227 / orgsyn.007.0074
- ^ RT Bertz "Furfuryl Diacetate" Org. Synth. 1953 года, 33, 39. DOI : 10,15227 / orgsyn.033.0039
- ^ Г. Рошер "Виниловые эфиры" в Энциклопедии химической технологии Ульмана , 2007 г. John Wiley & Sons: Нью-Йорк. DOI : 10.1002 / 14356007.a27_419
- ^ Уксусный ангидрид: часто задаваемые вопросы (PDF) , British Petroleum, заархивировано из оригинала (PDF) 11 октября 2007 г. , извлечено 03 мая 2006 г. .
- ^ Уксусный ангидрид: паспорт безопасности материала (PDF) (PDF) , Celanese, заархивировано из оригинала (PDF) 27 сентября 2007 г. , извлечено 03 мая 2006 г. .
- ^ Уксусный ангидрид (PDF) , Отчет об оценке SIDS, Женева: Программа ООН по окружающей среде, стр. 5 .
- ^ ООН перехватывает героиновый химикат талибов в редкой афганской победе , Bloomberg , заархивировано из оригинала 22 октября 2012 г. , извлечено 07 октября 2008 г..
- ^ "Таблицы данных" . Международный информационный центр по охране труда . Проверено 13 апреля 2006 .
- ^ "НИОШ" . Карманный справочник по химической опасности . Архивировано 22 апреля 2006 года . Проверено 13 апреля 2006 .
Внешние ссылки [ править ]
- ICSC 0209
- Карманный справочник NIOSH по химической опасности