 | |
| Имена | |
|---|---|
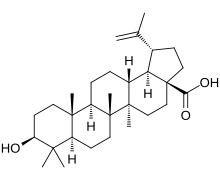
| Название ИЮПАК (3β) -3-Гидрокси-lup-20 (29) -ен-28-овая кислота | |
| Предпочтительное название IUPAC (1 R , 3a S , 5a R , 5b R , 7a R , 9 S , 11a R , 11b R , 13a R , 13b R ) -9-Гидрокси-5a, 5b, 8,8,11a-пентаметил-1- (проп-1-ен-1-ил) икозагидро-3a H -циклопента [ a ] хризен-3a-карбоновая кислота | |
| Другие имена Бетулиновая кислота Майрин | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.006.773 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| С 30 Н 48 О 3 | |
| Молярная масса | 456,711 г · моль -1 |
| Температура плавления | От 316 до 318 ° C (от 601 до 604 ° F; от 589 до 591 K) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Бетулиновая кислота представляет собой встречающийся в природе пентациклический тритерпеноид, который обладает антиретровирусными , противомалярийными и противовоспалительными свойствами, а также недавно обнаруженным потенциалом в качестве противоракового агента путем ингибирования топоизомеразы . [2] Он содержится в коре нескольких видов растений, в основном березы белой ( Betula pubescens ) [3], от которой и получило свое название, а также берёзы ( Ziziphus mauritiana ), самолечения ( Prunella vulgaris ), тропические плотоядные растения Triphyophyllum peltatum и Ancistrocladus heyneanus , Diospyros leucomelas , член хурмы семьи, Tetracera boiviniana , тем Джамбул ( Syzygium formosanum ), [4] цветения айвы ( айва китайская Синенсис , бывший Chaenomeles Sinensis Koehne ), [5] розмарина , [6] и Pulsatilla chinensis . [7]
Противоопухолевое действие [ править ]
Эта статья нуждается в дополнительных медицинских справочниках для проверки или слишком сильно полагается на первоисточники , в частности: Раздел . ( сентябрь 2014 г. ) |
В 1995 году о бетулиновой кислоте сообщили как о селективном ингибиторе меланомы человека . [8] Затем было продемонстрировано, что он индуцирует апоптоз в нейробластоме человека in vitro и in vivo в модельных системах. [9] В свое время он находился в процессе разработки лекарств при поддержке программы Rapid Access to Intervention Development Национального института рака . [3] Также было обнаружено, что бетулиновая кислота активна in vitro против нейроэктодермальных ( нейробластома , медуллобластома , саркома Юинга) [10]) И опухоли головного мозга , злокачественные, [4] [11] карциномы яичника , [4] в человеческой лейкемии HL-60 клеток , [7] и злокачественных клеточных линий SCC25 и SCC9 головы и шеи плоскоклеточный рак. [12] Напротив, эпителиальные опухоли, такие как опухоли молочной железы , толстой кишки , мелкоклеточные легкие и почечно-клеточные карциномы , а также клетки Т-клеточного лейкоза полностью не реагировали на лечение бетулиновой кислотой. [10]
Установлено, что действие бетулиновой кислоты как противоракового агента при раке груди зависит от каннабиноидного рецептора . Бетулиновая кислота действует как антагонист CB 1 и агонист CB 2 . [13]
Способ действия [ править ]
Что касается механизма действия бетулиновой кислоты, мало что известно о ее антипролиферативном и индуцирующем апоптоз механизмах. В нейроэктодермальных опухолевых клетках апоптоз, вызванный бетулиновой кислотой, сопровождается активацией каспаз , изменениями митохондриальной мембраны и фрагментацией ДНК . [10] [12] Каспазы продуцируются как неактивные проферменты , которые протеолитически процессируются до их активных форм. Эти протеазы могут взаимодействовать в протеолитических каскадах, в которых каспазы активируют себя и друг друга. Инициирование каскада каспаз может привести к активации эндонуклеаз.такие как ДНКаза, активируемая каспазой (CAD). После активации CAD способствует деградации ДНК. [12] Бетулиновая кислота вызывает апоптоз путем прямого воздействия на митохондрии, что приводит к высвобождению цитохрома-С, который, в свою очередь, регулирует активацию каспазы «ниже по течению». [12] Бетулиновая кислота обходит резистентность к CD95 и доксорубицин- опосредованному апоптозу из-за другого молекулярного механизма апоптоза, индуцированного бетулиновой кислотой.
Роль p53 в апоптозе, вызванном бетулиновой кислотой, противоречива. Фульда предположил p53-независимый механизм апоптоза, основанный на отсутствии накопления p53 дикого типа, обнаруженного при обработке бетулиновой кислотой, тогда как белок p53 дикого типа сильно увеличился после обработки доксорубицином. [10] Это предположение подтверждается исследованиями Раисовой. [14] С другой стороны, Рибер предположил, что бетулиновая кислота оказывает ингибирующее действие на метастатическую меланому человека частично за счет увеличения p53. [15]
Исследование также продемонстрировало преимущественный апоптотический эффект бетулиновой кислоты на метастатические клетки меланомы C8161 с большей фрагментацией ДНК и остановкой роста и более ранней потерей жизнеспособности, чем их неметастатический аналог C8161 / neo 6.3. [15] Сравнивая бетулиновую кислоту с другими методами лечения, Зуко продемонстрировал, что она менее чем на 10% эффективнее доксорубицина и продемонстрировала антипролиферативную активность in vitro в отношении линий клеток меланомы и немеланомы, включая те, которые устойчивы к доксорубицину. В нормальной линии клеток дерматобласта человека бетулиновая кислота была от половины до одной пятой токсичнее доксорубицина. [4] Способность бетулиновой кислоты вызывать два разных эффекта (цитотоксический и цитостатический) на два клона, происходящих от одного и того же метастаза меланомы человека, предполагает, что развитие клонов, устойчивых к этому агенту, будет более маловероятным, чем к обычным цитотоксическим препаратам. Более того, несмотря на более низкую эффективность по сравнению с доксорубицином, бетулиновая кислота, по-видимому, является селективной в отношении опухолевых клеток с минимальной токсичностью в отношении нормальных клеток. [4] Эффект бетулиновой кислоты на клеточные линии меланомы сильнее, чем ее ингибирующий рост эффект на первичные меланоциты. [16] Исследование комбинации бетулиновой кислоты с γ-облучением явно показало аддитивные эффекты и показало, что они различаются по способам действия. [16]
Этерификация бетулиновой кислоты C-3 привела к открытию бевиримата , ингибитора созревания ВИЧ-1 , запатентованного Rhone-Poulenc (теперь Sanofi-Aventis). Однако клиническая разработка была остановлена из-за плохих фармакодинамических свойств. [17]
Биосинтез [ править ]
Saccharomyces cerevisiae был разработан для производства бетулиновой кислоты мевалонатным путем со сквален-2,3-эпоксидом в качестве промежуточного продукта. Ацетил-СоА превращается в сквален посредством использования редуктазы 3-гидрокси-3-метилглутарил-КоА (HMGR) и бифункциональным фарнезил-дифосфат фарнезилтрансферазы и сквален - синтазы (ERG9) и окисление NADPH в NADP + . Это затем дополнительно окисленный с помощью сквален монооксигеназной (ERG1) к сквален - 2,3-эпоксида. Это циклизуют лупеола по thaliana Arabidopsisлупеолсинтаза (AtLUP1). Наконец, лупеол превращается в бетулиновую кислоту через монооксигеназу P450 (CrAO) Catharanthus roseus при окислении НАДФН до НАДФ + . [18]
Противоопухолевые производные [ править ]
Основное неудобство для будущей клинической разработки бетулиновой кислоты и аналогов заключается в их плохой растворимости в водных средах, таких как сыворотка крови и полярные растворители, используемые для биоанализов. Чтобы обойти эту проблему водорастворимости и улучшить фармакологические свойства, многие производные были синтезированы и оценены на цитотоксическую активность. Одно исследование показало, что модификации C-20 приводят к потере цитотоксичности. Другое исследование продемонстрировало важность присутствия группы -COOH, поскольку соединения, замещенные в этом положении, такие как лупеоли метил бетулинат были менее активны в отношении меланомы человека, чем бетулиновая кислота. Более того, некоторые производные C-28 аминокислот и фталатов C-3 проявляли более высокую цитотоксическую активность против линий раковых клеток с улучшенной селективной токсичностью и растворимостью в воде. Чаттерджи и др. получили 28-O-β-D-глюкопиранозид бетулиновой кислоты путем микробной трансформации с использованием видов Cunninghamella , тогда как Baglin et al. получил его путем органического синтеза. Этот глюкозид не проявлял какой-либо значительной активности in vitro на клеточных линиях меланомы человека (MEL-2) и колоректальной аденокарциномы человека (HT-29), что подтверждает важность функции карбоновой кислоты для сохранения цитотоксичности. Недавно Gauthier et al.синтезировал серию 3- O- гликозидов бетулиновой кислоты, которые проявляли сильную противораковую активность in vitro против линий раковых клеток человека. [19]
См. Также [ править ]
- Олеаноловая кислота
- Урсоловая кислота
- Мороновая кислота
Ссылки [ править ]
- ^ https://echa.europa.eu
- ^ Чоудхури AR, Мандал S, Миттро B, S Шарма, Mukhopadhyay S, Majumder HK (июль 2002). «Бетулиновая кислота, мощный ингибитор эукариотической топоизомеразы I: определение стадии ингибирования, основной ответственной функциональной группы и разработка более мощных производных» . Монитор медицинской науки . 8 (7): BR254–65. PMID 12118187 .
- ^ a b Tan Y, Yu R, Pezzuto JM (июль 2003 г.). «Индуцированная бетулиновой кислотой запрограммированная гибель клеток в клетках меланомы человека включает активацию митоген-активированной протеинкиназы» . Клинические исследования рака . 9 (7): 2866–75. PMID 12855667 .
- ^ a b c d e Zuco V, Supino R, Righetti SC, Cleris L, Marchesi E, Gambacorti-Passerini C, Formelli F (январь 2002 г.). «Избирательная цитотоксичность бетулиновой кислоты на линиях опухолевых клеток, но не на нормальных клетках». Письма о раке . 175 (1): 17–25. DOI : 10.1016 / S0304-3835 (01) 00718-2 . PMID 11734332 .
- Перейти ↑ Gao H, Wu L, Kuroyanagi M, Harada K, Kawahara N, Nakane T, Umehara K, Hirasawa A, Nakamura Y (ноябрь 2003 г.). «Противоопухолевые компоненты из Chaenomeles sinensis KOEHNE и их активность в эпидермальных клетках мышей JB6» . Химико-фармацевтический бюллетень . 51 (11): 1318–21. DOI : 10,1248 / cpb.51.1318 . PMID 14600382 . ( Chaenomeles sinensis KOEHNE теперь называется Pseudocydonia sinensis )
- ↑ Abe F, Yamauchi T, Nagao T, Kinjo J, Okabe H, Higo H, Akahane H (ноябрь 2002 г.). «Урсоловая кислота как трипаноцидный компонент розмарина» . Биологический и фармацевтический бюллетень . 25 (11): 1485–7. DOI : 10.1248 / bpb.25.1485 . PMID 12419966 .
- ^ а б Цзи З. Н., Е В. К., Лю Г. Г., Сяо В. Л. (ноябрь 2002 г.). «Апоптоз, опосредованный 23-гидроксибетулиновой кислотой, сопровождается снижением экспрессии bcl-2 и теломеразной активности в клетках HL-60». Науки о жизни . 72 (1): 1–9. DOI : 10.1016 / S0024-3205 (02) 02176-8 . PMID 12409140 .
- ^ Pisha E, Chai H, Ли, Chagwedera TE, Фарнсворт NR, Корделл Г.А., Бичер CW, Фонг HH, Kinghorn Д., Браун Д. (октябрь 1995). «Открытие бетулиновой кислоты в качестве селективного ингибитора меланомы человека, который действует путем индукции апоптоза». Природная медицина . 1 (10): 1046–51. DOI : 10.1038 / nm1095-1046 . PMID 7489361 . S2CID 24752850 .
- ^ Schmidt ML, Kuzmanoff KL, Линг-Indeck L, Pezzuto JM (октябрь 1997). «Бетулиновая кислота индуцирует апоптоз клеточных линий нейробластомы человека». Европейский журнал рака . 33 (12): 2007–10. DOI : 10.1016 / S0959-8049 (97) 00294-3 . PMID 9516843 .
- ^ a b c d Fulda S, Friesen C, Los M, Scaffidi C, Mier W, Benedict M, Nuñez G, Krammer PH, Peter ME, Debatin KM (ноябрь 1997 г.). «Бетулиновая кислота запускает CD95 (APO-1 / Fas) - и p53-независимый апоптоз через активацию каспаз в нейроэктодермальных опухолях» . Исследования рака . 57 (21): 4956–64. PMID 9354463 .
- ^ Фитиль Вт, Гриммель С, Вагенкнехтом В, Dichgans Дж, Weller М (июнь 1999 г.). «Индуцированный бетулиновой кислотой апоптоз в клетках глиомы: последовательное требование для синтеза нового белка, образования активных форм кислорода и процессинга каспазы» . Журнал фармакологии и экспериментальной терапии . 289 (3): 1306–12. PMID 10336521 .
- ^ a b c d Thurnher D, Turhani D, Pelzmann M, Wannemacher B, Knerer B, Formanek M, Wacheck V, Selzer E (сентябрь 2003 г.). «Бетулиновая кислота: новое цитотоксическое соединение против злокачественных клеток рака головы и шеи». Голова и шея . 25 (9): 732–40. DOI : 10.1002 / hed.10231 . PMID 12953308 .
- ^ Лю X, Jutooru I, Lei P, Kim K, Lee SO, Brents LK, Prather PL, Safe S (июль 2012 г.). «Бетулиновая кислота нацелена на YY1 и ErbB2 посредством каннабиноидного рецептора-зависимого разрушения микроРНК-27a: ZBTB10 при раке груди» . Молекулярная терапия рака . 11 (7): 1421–31. DOI : 10.1158 / 1535-7163.MCT-12-0026 . PMC 4924623 . PMID 22553354 .
- ^ Raisova М, Hossini А.М., Eberle Дж, Riebeling С, Т Wieder, Штурм я, Даниил PT, Орфанос CE, Geilen CC (август 2001 г.). «Отношение Bax / Bcl-2 определяет восприимчивость клеток меланомы человека к CD95 / Fas-опосредованному апоптозу». Журнал следственной дерматологии . 117 (2): 333–40. DOI : 10,1046 / j.0022-202x.2001.01409.x . PMID 11511312 .
- ^ a b Рибер М, Страсберг Рибер М (май 1998 г.). «Индукция p53 без увеличения p21WAF1 при гибели клеток, опосредованной бетулиновой кислотой, является предпочтительной для метастатической меланомы человека». ДНК и клеточная биология . 17 (5): 399–406. DOI : 10.1089 / dna.1998.17.399 . PMID 9628583 .
- ^ a b Зельцер Э, Пиментел Э, Вачек В., Шлегель В., Пехамбергер Х, Янсен Б., Кодым Р. (май 2000 г.). «Эффекты бетулиновой кислоты отдельно и в сочетании с облучением на клетки меланомы человека». Журнал следственной дерматологии . 114 (5): 935–40. DOI : 10.1046 / j.1523-1747.2000.00972.x . PMID 10771474 .
- ^ Роман 3,28-Дизамещенные производные бетулиновой кислоты как мощные анти-ВИЧ-агенты Цели / гипотеза Отсутствие лицензии. iptechex Pharmalicensing, Обмен IP-технологиями (2013 г.)
- ^ а б Ли, Цзин; Чжан, Яньшэн (19 июня 2014 г.). «Регулирование производства бетулиновой кислоты в Saccharomyces cerevisiae путем управления внутриклеточными поставками кофактора НАДФН и кислорода». Журнал биологии и биоинженерии . 119 (1): 77–81. DOI : 10.1016 / j.jbiosc.2014.06.013 . PMID 25043336 .
- ^ Готье С, Лего Дж, Лебрён М, Дюфор Р, Pichette А (октябрь 2006 г.). «Гликозидирование тритерпеноидов лупанового типа в качестве сильнодействующих цитотоксических агентов in vitro». Биоорганическая и медицинская химия . 14 (19): 6713–25. DOI : 10.1016 / j.bmc.2006.05.075 . PMID 16787747 .