Химические символы - это сокращения, используемые в химии для обозначения химических элементов , функциональных групп и химических соединений. Символы элементов для химических элементов обычно состоят из одной или двух букв латинского алфавита и пишутся с заглавной буквы. В китайском языке каждый химический элемент имеет специальный символ , обычно созданный для этой цели (см. Химические элементы на языках Восточной Азии ). Однако латинские символы также используются, особенно в формулах.
Ранние символы химических элементов происходят из классического латинского и греческого словаря. Для некоторых элементов это связано с тем, что материал был известен в древние времена, в то время как для других это название является более поздним изобретением. Например, Pb - это символ свинца ( на латыни - свинец ); Hg - символ ртути ( по-гречески hydrargyrum ); и Он - символ гелия ( новое латинское название), потому что гелий не был известен в древнеримские времена. Некоторые символы взяты из других источников, например W для вольфрама ( по-немецки Wolfram ), который не был известен во времена Римской империи.
Трехбуквенный временный символ может быть назначен вновь синтезированному (или еще не синтезированному) элементу. Например, «Уно» было временным символом для хасиума (элемент 108), который имел временное название уннилоктиум , основанное на цифрах его атомного номера. Есть также некоторые исторические символы, которые больше не используются официально.
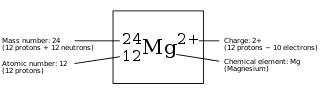
В дополнение к буквам, обозначающим сам элемент, к символу могут быть добавлены дополнительные детали в виде надстрочных или подстрочных индексов для конкретного изотопа , состояния ионизации или окисления или других атомных деталей. [1] У некоторых изотопов есть свои собственные специфические символы, а не просто изотопная деталь, добавленная к их символу элемента.
Прилагаемые индексы или надстрочные индексы, обозначающие нуклид или молекулу, имеют следующие значения и положения:
- Число нуклонов ( массовое число ) показано в левом верхнем индексе (например, 14 N). Это число определяет конкретный изотоп. Различные буквы, такие как «m» и «f», также могут использоваться здесь для обозначения ядерного изомера (например, 99m Tc ). В качестве альтернативы, число здесь может представлять конкретное состояние вращения (например, 1 O 2 ). Эти детали могут быть опущены, если они не актуальны в определенном контексте.
- Номер протона ( атомный номер ) может быть указан в левом нижнем индексе (например, 64 Gd). Атомный номер является избыточным для химического элемента, но иногда используется, чтобы подчеркнуть изменение числа нуклонов в ядерной реакции.
- При необходимости состояние ионизации или возбужденное состояние может быть указано в правом верхнем индексе (например, состояние ионизации Ca 2+ ).
- Число атомов элемента в молекуле или химическом соединении показано в правом нижнем индексе (например, N 2 или Fe 2 O 3 ). Если это число единица, оно обычно опускается - число один подразумевается неявно, если не указано.
- Радикал обозначен точкой на правой стороне (например, Cl • для нейтрального атома хлора). Это часто опускается, если это не относится к определенному контексту, потому что это уже можно вывести из заряда и атомного номера, что обычно верно для несвязанных валентных электронов в скелетных структурах .
Многие функциональные группы также имеют свой собственный химический символ, например Ph для фенильной группы и Me для метильной группы .
Список текущих, датированных, а также предполагаемых и исторических знаков и символов включен сюда с их значением . Также указан атомный номер каждого элемента , атомный вес или атомная масса наиболее стабильного изотопа , номера групп и периодов в периодической таблице , а также этимология символа.
Пиктограммы опасности - это еще один тип символов, используемых в химии.
Символы химических элементов [ править ]
| Z [I] | Символ | Имя | Происхождение имени [2] [3] | Группа | Период | Атомный вес [4] [5] ( u (±) ) |
|---|---|---|---|---|---|---|
| 1 | ЧАС | Водород | Греческие элементы гидро- и -gen , что означает « вода образующую» | 1 | 1 | 1.008 [II] [III] [IV] [V] |
| 2 | Он | Гелий | Греческий Helios « ВС » | 18 | 1 | 4.002602 (2) [II] [IV] |
| 3 | Ли | Литий | Греческий LITHOS , « камень » | 1 | 2 | 6.94 [II] [III] [IV] [VI] [V] |
| 4 | Быть | Бериллий | берилл , минерал (в конечном счете, от названия Белура на юге Индии) | 2 | 2 | 9.0121831 (5) |
| 5 | B | Бор | бура , минерал (от арабского bawraq ) | 13 | 2 | 10,81 [II] [III] [IV] [V] |
| 6 | C | Углерод | Latin карбо « уголь » | 14 | 2 | 12.011 [II] [IV] [V] |
| 7 | N | Азот | Греческий нитрон и -gen , что означает « селитра образующую» | 15 | 2 | 14.007 [II] [IV] [V] |
| 8 | О | Кислород | Греческий окси- и -ген , что означает « образующий кислоту ». | 16 | 2 | 15,999 [II] [IV] [V] |
| 9 | F | Фтор | Латинское fluere , «течь» | 17 | 2 | 18.998403163 (6) |
| 10 | Ne | Неон | Греческое néon , "новый" | 18 | 2 | 20.1797 (6) [II] [III] |
| 11 | Na | Натрий | Английский газированный напиток (символ Na происходит от нового латинского natrium , от немецкого Natron , « натрон ») | 1 | 3 | 22.98976928 (2) |
| 12 | Mg | Магний | Магнезия , район Восточной Фессалии в Греции. | 2 | 3 | 24.305 [В] |
| 13 | Al | Алюминий | глинозем , от латинского alumen (род. выпускники ), 'горькая соль, квасцы ' | 13 | 3 | 26.9815384 (3) |
| 14 | Si | Кремний | Латинское silx , ' кремень ' (первоначально кремний ) | 14 | 3 | 28.085 [IV] [V] |
| 15 | п | Фосфор | Греческое phōsphóros , "светоносный" | 15 | 3 | 30.973761998 (5) |
| 16 | S | Сера | Латинское сера , сера | 16 | 3 | 32.06 [II] [IV] [V] |
| 17 | Cl | Хлор | Греческий chlōrós , "зеленовато-желтый" | 17 | 3 | 35,45 [II] [III] [IV] [V] |
| 18 | Ar | Аргон | Греческие Argos , «простаивает» (из - за своей инертности ) | 18 | 3 | 39,948 [II] [IV] [V] |
| 19 | K | Калий | Новая латинская potassa , поташ (символ K происходит от латинского kalium ). | 1 | 4 | 39,0983 (1) |
| 20 | Ca | Кальций | Latin окалины , « лайм » | 2 | 4 | 40.078 (4) [II] |
| 21 год | Sc | Скандий | Латинская Скандия , ' Скандинавия ' | 3 | 4 | 44.955908 (5) |
| 22 | Ti | Титана | Титаны , сыновья богини земли из греческой мифологии | 4 | 4 | 47,867 (1) |
| 23 | V | Ванадий | Ванадис , древнескандинавское имя скандинавской богини Фрейи. | 5 | 4 | 50,9415 (1) |
| 24 | Cr | Хром | Греческий Chroma , « цвет » | 6 | 4 | 51,9961 (6) |
| 25 | Mn | Марганец | испорченный от магнезии негры ; см. Магний | 7 | 4 | 54.938043 (2) |
| 26 год | Fe | Утюг | Английское слово (символ Fe происходит от латинского ferrum ) | 8 | 4 | 55,845 (2) |
| 27 | Co | Кобальт | Немецкий Kobold , « Гоблин » | 9 | 4 | 58.933194 (3) |
| 28 год | Ni | Никель | Никель, озорной спрайт немецкой шахтерской мифологии | 10 | 4 | 58,6934 (4) |
| 29 | Cu | Медь | Английское слово, от латинского cuprum , от древнегреческого Kýpros ' Кипр '. | 11 | 4 | 63,546 (3) [IV] |
| 30 | Zn | Цинк | Скорее всего, от немецкого Zinke , «зубец» или «зуб», хотя некоторые предполагают, что персидский пел , «камень». | 12 | 4 | 65,38 (2) |
| 31 год | Ga | Галлий | Латинское Gallia , ' Франция ' | 13 | 4 | 69,723 (1) |
| 32 | Ge | Германий | Латинская Германия , ' Германия ' | 14 | 4 | 72,630 (8) |
| 33 | В качестве | Мышьяк | Французский мышьяк , от греческого arsenikón «желтый мышьяк» (под влиянием arsenikós , «мужской» или «мужской»), из западноазиатского странствующего слова, в конечном счете, от древнеиранского * zarniya-ka , «золотой». | 15 | 4 | 74.921595 (6) |
| 34 | Se | Селен | Греческое selḗnē , ' луна ' | 16 | 4 | 78.971 (8) [IV] |
| 35 год | Br | Бром | Греческие brômos , «вонь» | 17 | 4 | 79,904 [В] |
| 36 | Kr | Криптон | Греческие Kryptos , «скрытый» | 18 | 4 | 83,798 (2) [II] [III] |
| 37 | Руб. | Рубидий | Латинское rubidus , глубокий красный | 1 | 5 | 85.4678 (3) [II] |
| 38 | Sr | Стронций | Стронтиан , деревня в Шотландии. | 2 | 5 | 87,62 (1) [II] [IV] |
| 39 | Y | Иттрий | Иттерби , деревня в Швеции. | 3 | 5 | 88,90584 (1) |
| 40 | Zr | Цирконий | циркон , минерал | 4 | 5 | 91.224 (2) [II] |
| 41 год | Nb | Ниобий | Ниоба , дочь царя Тантала из греческой мифологии | 5 | 5 | 92.90637 (1) |
| 42 | Пн | Молибден | Греческое molýbdaina , «кусок свинца », от mólybdos , «свинец» | 6 | 5 | 95,95 (1) [II] |
| 43 год | Tc | Технеций | Греческие tekhnētós , «искусственный» | 7 | 5 | [97] [VII] |
| 44 год | RU | Рутений | Новая Латинская Малороссия , ' Россия ' | 8 | 5 | 101.07 (2) [II] |
| 45 | Rh | Родий | Греческое rhodóeis , « цвет розы », от rhódon , « роза ». | 9 | 5 | 102,90549 (2) |
| 46 | Pd | Палладий | астероид Паллада , который в то время считался планетой | 10 | 5 | 106,42 (1) [II] |
| 47 | Ag | Серебро | Английское слово (символ происходит от латинского argentum ) | 11 | 5 | 107.8682 (2) [II] |
| 48 | CD | Кадмий | Новая латинская кадмия от короля Кадмоса | 12 | 5 | 112.414 (4) [II] |
| 49 | В | Индий | Латинское indicum , ' индиго ' (цвет в его спектре) | 13 | 5 | 114,818 (1) |
| 50 | Sn | Банка | Английское слово (символ происходит от латинского stannum ) | 14 | 5 | 118,710 (7) [II] |
| 51 | Sb | Сурьма | Латинский антимоний , происхождение которого неясно: народные этимологии предполагают, что оно происходит от греческого antí («против») + mónos («одинокий») или старофранцузского anti- moine , «проклятие монаха», но вполне вероятно, что оно произошло от или связано с арабским ʾiṯmid , «сурьма», переформатированное как латинское слово. (Символ происходит от латинского сурьма « Стибнит ».) | 15 | 5 | 121,760 (1) [II] |
| 52 | Te | Теллур | Латинское tellus , "земля, земля" | 16 | 5 | 127.60 (3) [II] |
| 53 | я | Йод | Французское iode , от греческого ioeidḗs , 'фиолетовый' | 17 | 5 | 126,90447 (3) |
| 54 | Xe | Ксенон | Греческий xénon , средний род от xénos 'странный' | 18 | 5 | 131.293 (6) [II] [III] |
| 55 | CS | Цезий | Латинское caesius , "небесно-голубой" | 1 | 6 | 132.90545196 (6) |
| 56 | Ба | Барий | Греческое barýs , тяжелый | 2 | 6 | 137,327 (7) |
| 57 | Ла | Лантан | Греческий lanthánein «врать скрытый» | 6 | 138.90547 (7) [II] | |
| 58 | Ce | Церий | карликовая планета Церера , считавшаяся в то время планетой | 6 | 140.116 (1) [II] | |
| 59 | Pr | Празеодим | Греческие prásios Didymos , «зеленый близнец» | 6 | 140,90766 (1) | |
| 60 | Nd | Неодим | Греческие ОСЗ Didymos , «новый близнец» | 6 | 144.242 (3) [II] | |
| 61 | Вечера | Прометий | Прометей из греческой мифологии | 6 | [145] [VII] | |
| 62 | См | Самарий | самарскит , минерал, названный в честь полковника Василия Самарского-Быховца , российского шахтёра | 6 | 150,36 (2) [II] | |
| 63 | Европа | Европий | Европа | 6 | 151.964 (1) [II] | |
| 64 | Б-г | Гадолиний | гадолинит , минерал, названный в честь Йохана Гадолина , финского химика, физика и минералога | 6 | 157,25 (3) [II] | |
| 65 | Tb | Тербий | Иттерби , деревня в Швеции. | 6 | 158.925354 (8) | |
| 66 | Dy | Диспрозий | Греческий dysprósitos , "трудно достать" | 6 | 162 500 (1) [II] | |
| 67 | Хо | Гольмий | Новая латинская Holmia , ' Стокгольм ' | 6 | 164.930328 (7) | |
| 68 | Э | Эрбий | Иттерби , деревня в Швеции. | 6 | 167.259 (3) [II] | |
| 69 | Тм | Тулий | Туле , древнее название неясного северного местоположения | 6 | 168.934218 (6) | |
| 70 | Yb | Иттербий | Иттерби , деревня в Швеции. | 6 | 173.045 (10) [II] | |
| 71 | Лу | Лютеций | Латинская лютеция , ' Париж ' | 3 | 6 | 174.9668 (1) [II] |
| 72 | Hf | Гафний | Новая латинская Hafnia , ' Копенгаген ' (от датского havn ) | 4 | 6 | 178,49 (2) |
| 73 | Та | Тантал | Царь Тантал , отец Ниобы из греческой мифологии | 5 | 6 | 180.94788 (2) |
| 74 | W | Вольфрам | Шведский дун Стен , «тяжелый камень» (Символ из вольфрама , старое название вольфрама минеральной вольфрамите ) | 6 | 6 | 183,84 (1) |
| 75 | Re | Рений | Латинское Rhenus , ' Рейн ' | 7 | 6 | 186.207 (1) |
| 76 | Операционные системы | Осмий | Греческий osmḗ , « запах » | 8 | 6 | 190,23 (3) [II] |
| 77 | Ir | Иридий | Ирис , греческая богиня радуги | 9 | 6 | 192,217 (2) |
| 78 | Pt | Платина | Платина испанская , серебрянка, от plata silver | 10 | 6 | 195.084 (9) |
| 79 | Au | Золото | Английское слово (символ происходит от латинского aurum ) | 11 | 6 | 196.966570 (4) |
| 80 | Hg | Меркурий | Меркурий , римский бог торговли, общения и удачи, известный своей скоростью и подвижностью (символ происходит от латинского названия элемента hydrargyrum , производного от греческого hydrágeryros , « вода - серебро »). | 12 | 6 | 200,592 (3) |
| 81 год | Tl | Таллий | Греческий талло , «зеленый побег или веточка» | 13 | 6 | 204,38 [В] |
| 82 | Pb | Вести | Английское слово (символ происходит от латинского plumbum ) | 14 | 6 | 207,2 (1) [II] [IV] |
| 83 | Би | Висмут | Немецкий Wismut , от weiß Masse 'белая масса', если не арабский | 15 | 6 | 208.98040 (1) [VII] |
| 84 | По | Полоний | Латинская Полония , ' Польша ' (родина Марии Кюри ) | 16 | 6 | [209] [VII] |
| 85 | В | Астатин | Греческое ástatos , нестабильный | 17 | 6 | [210] [VII] |
| 86 | Rn | Радон | радий | 18 | 6 | [222] [VII] |
| 87 | Пт | Франций | Франция | 1 | 7 | [223] [VII] |
| 88 | Ра | Радий | Французский радий , от латинского радиуса , ' луч ' | 2 | 7 | [226] [VII] |
| 89 | Ac | Актиний | Греческое aktís , луч | 7 | [227] [VII] | |
| 90 | Чт | Торий | Тор , скандинавский бог грома | 7 | 232.0377 (4) [VII] [II] | |
| 91 | Па | Протактиний | прото- (от греч. prôtos , «первый, до») + актиний , который образуется в результате радиоактивного распада протактиния. | 7 | 231.03588 (1) [VII] | |
| 92 | U | Уран | Уран , седьмая планета Солнечной системы | 7 | 238.02891 (3) [VII] | |
| 93 | Np | Нептуний | Нептун , восьмая планета Солнечной системы | 7 | [237] [VII] | |
| 94 | Пу | Плутоний | карликовая планета Плутон , считавшаяся девятой планетой Солнечной системы в то время | 7 | [244] [VII] | |
| 95 | Являюсь | Америций | Америка , поскольку элемент был впервые синтезирован на континенте по аналогии с европием | 7 | [243] [VII] | |
| 96 | См | Кюрий | Пьер Кюри и Мария Кюри , французские физики и химики | 7 | [247] [VII] | |
| 97 | Bk | Берклиум | Беркли , Калифорния, где элемент был впервые синтезирован по аналогии с тербием. | 7 | [247] [VII] | |
| 98 | Cf | Калифорний | Калифорния , где впервые был синтезирован элемент | 7 | [251] [VII] | |
| 99 | Es | Эйнштейний | Альберт Эйнштейн , немецкий физик | 7 | [252] [VII] | |
| 100 | FM | Фермий | Энрико Ферми , итальянский физик | 7 | [257] [VII] | |
| 101 | Мкр | Менделевий | Дмитрий Менделеев , русский химик и изобретатель, предложивший периодическую таблицу | 7 | [258] [VII] | |
| 102 | Нет | Нобелий | Альфред Нобель , шведский химик и инженер | 7 | [259] [VII] | |
| 103 | Lr | Лоуренсий | Эрнест О. Лоуренс , американский физик | 3 | 7 | [266] [VII] |
| 104 | Rf | Резерфордий | Эрнест Резерфорд , британский химик и физик | 4 | 7 | [267] [VII] |
| 105 | Db | Дубний | Дубна , Россия, где Объединенный институт ядерных исследований расположен | 5 | 7 | [268] [VII] |
| 106 | Sg | Сиборгий | Гленн Т. Сиборг , американский химик | 6 | 7 | [269] [VII] |
| 107 | Bh | Бориум | Нильс Бор , датский физик | 7 | 7 | [270] [VII] |
| 108 | Hs | Калий | Новый латинский Hassia « Гесс » (государство в Германии) | 8 | 7 | [270] [VII] |
| 109 | Mt | Мейтнерий | Лиз Мейтнер , австрийский физик | 9 | 7 | [278] [VII] |
| 110 | Ds | Дармштадтиум | Дармштадт , Германия, где элемент был впервые синтезирован. | 10 | 7 | [281] [VII] |
| 111 | Rg | Рентгений | Вильгельм Конрад Рентген , немецкий физик | 11 | 7 | [282] [VII] |
| 112 | Cn | Копернициум | Николай Коперник , польский астроном | 12 | 7 | [285] [VII] |
| 113 | Nh | Нихоний | Японский Nihon , ' Япония ' (где элемент был впервые синтезирован) | 13 | 7 | [286] [VII] |
| 114 | Fl | Флеровий | Лаборатория ядерных реакций , часть ОИЯИ , где был синтезирован элемент; Сама названа в честь Георгия Флёрова , российского физика. | 14 | 7 | [289] [VII] |
| 115 | Mc | Московиум | Московская область , Россия, где элемент был впервые синтезирован | 15 | 7 | [290] [VII] |
| 116 | Ур. | Ливерморий | Ливерморская национальная лаборатория Лоуренса в Ливерморе, Калифорния , которая сотрудничала с ОИЯИ в его синтезе. | 16 | 7 | [293] [VII] |
| 117 | Ц | Tennessine | Теннесси , США | 17 | 7 | [294] [VII] |
| 118 | Og | Оганессон | Юрий Оганесян , российский физик | 18 | 7 | [294] [VII] |
Заметки [ править ]
- ^ Z - стандартный символ атомного номера
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al Изотопный состав этого элемента варьируется в некоторых геологических образцах , и отклонение может превышать неопределенность, указанную в таблице.
- ^ a b c d e f g Изотопный состав элемента может варьироваться в коммерческих материалах, что может привести к значительному отклонению атомного веса от заданного значения.
- ^ a b c d e f g h i j k l m n o Изотопный состав в земном материале варьируется, поэтому более точный атомный вес не может быть дан.
- ^ a b c d e f g h i j k l m Указанное значение является условным значением атомного веса, подходящим для торговли и коммерции. Фактическое значение может отличаться в зависимости от изотопного состава образца. С 2009 года ИЮПАК предоставляет стандартные значения атомных весов для этих элементов, используя обозначение интервалов. Соответствующие стандартные атомные веса:
- Водород: [1.00784, 1.00811]
- Литий: [6,938, 6,997]
- Бор: [10,806, 10,821]
- Углерод: [12.0096, 12.0116]
- Азот: [14.00643, 14.00728]
- Кислород: [15.99903, 15.99977]
- Магний: [24.304, 24.307]
- Кремний: [28.084, 28.086]
- Сера: [32,059, 32,076]
- Хлор: [35,446, 35,457]
- Аргон: [39,792, 39,963]
- Бром: [79,901, 79,907]
- Таллий: [204,382, 204,385]
- ^ Атомный вес коммерческого лития может варьироваться от 6,939 до 6,996 - для получения более точного значения необходим анализ конкретного материала.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al Элемент не имеет стабильных нуклидов, а значение в скобках, например [209], указывает массовое число наиболее долгоживущего изотопа элемента. Однако четыре таких элемента, висмут, торий, протактиний и уран, имеют характерный земной изотопный состав, и поэтому дан их стандартный атомный вес.
Антиматерии атомов обозначается чертой над символом их материи коллегой, так , например , H является символом для антиводорода .
Символы и названия в настоящее время не используются [ править ]
Этот раздел требует дополнительных ссылок для проверки . ( май 2018 г. ) ( Узнайте, как и когда удалить это сообщение-шаблон ) |
Ниже приводится список символов и названий, которые ранее использовались или предлагались для элементов, включая символы для имен заполнителей и имена, данные дискредитированными заявителями для обнаружения.
| Символ | Имя | Атомный номер | Примечания | Почему не использовал | Ссылки |
|---|---|---|---|---|---|
| А | Аргон | 18 | A использовался для аргона до 1957 года. Текущее обозначение - Ar . | [nb 1] | [6] |
| Ab | Алабамин | 85 | Опровергнутые претензии на открытие астата . | [nb 2] | [7] [8] |
| Объявление | Альдебаран | 70 | Прежнее название иттербия . | [nb 2] | |
| Ах | Англохельвеций | 85 | Опровергнутые претензии на открытие астата . | [nb 2] | [9] |
| Ак | Щелочь | 87 | Опровергнутые претензии на открытие франция . | [nb 2] | [7] |
| Являюсь | Алабамин | 85 | Опровергнутые претензии на открытие астата . Этот символ теперь используется для америция . | [nb 2] | [7] [8] |
| An | Афений | 99 | Предлагаемое название для эйнштейния . | [№ 3] | |
| АО | Аусониум | 93 | Опровергнутые претензии на открытие нептуния . | [nb 2] | [7] |
| В | Austriacum | 84 | Опровергнутые претензии на открытие полония . Этот символ теперь используется для астатина . | [nb 2] | |
| Аз | Азоте | 7 | Прежнее название азота . | [nb 1] | |
| Бо | Богемий | 93 | Опровергнутые претензии на открытие нептуния . | [nb 2] | |
| Бо | Бор | 5 | Текущий символ B . | [nb 1] | |
| Bv | Brevium | 91 | Прежнее название протактиниума . | [nb 1] | |
| Bz | Берзелий | 90 | Баскервиль ошибочно считал берселий новым элементом. Фактически был торий . | [9] | |
| Cb | Колумбий | 41 год | Прежнее название ниобия . | [nb 1] | [7] [9] |
| Ch | Хром | 24 | Текущий символ - Cr . | [nb 1] | |
| Cl | Колумбий | 41 год | Прежнее название ниобия . Этот символ теперь используется для хлора . | [nb 1] | |
| См | Catium | 87 | Предлагаемое название для франция . Этот символ теперь используется для кюрия . | [№ 3] | |
| Cn | Каролиниум | 90 | Баскервиль ошибочно считал каролиний новым элементом. Фактически был торий . Этот символ теперь используется для копернициума . | [9] | |
| Cp | Кассиопей | 71 | Прежнее название лютеция . | [nb 1] | |
| Cp | Копернициум | 112 | Текущий символ - Cn . | [nb 1] | |
| Кт | Кельтий | 72 | Опровергнутые претензии на открытие гафния . | [nb 2] | |
| Кт | Центуриум | 100 | Предлагаемое название для фермия . | [№ 3] | |
| Сай | Циклониум | 61 | Предлагаемое название прометия . | [№ 3] | |
| D | Didymium | 59/60 | Смесь элементов празеодима и неодима . Мосандер ошибочно считал дидимий элементом. | [10] | |
| Да | Давьюм | 43 год | Опровергнутые претензии на открытие технеция . | [nb 2] | [7] |
| Db | Дубхиум | 69 | Эдер ошибочно считал дубиум новым элементом. Фактически был тулий . Этот символ теперь используется для дубниума . | ||
| Db | Дубний | 104 | Предлагаемое название резерфордия . Вместо этого символ и имя использовались для элемента 105. | [nb 1] [nb 3] | [7] |
| Округ Колумбия | Decipium | 62 | Делафонтен ошибочно считал деципий новым элементом. Фактически был самарий . | ||
| Округ Колумбия | Двицезий | 87 | Имя, данное Менделеевым какому-то еще неоткрытому элементу. Когда было обнаружено, франций полностью соответствовал предсказанию. | [№ 3] [№ 4] | |
| Де | Денебиум | 69 | Эдер ошибочно считал денебий новым элементом. Фактически был тулий . | ||
| Ди | Didymium | 59/60 | Смесь элементов празеодима и неодима . Мосандер ошибочно считал дидимий элементом. | [10] | |
| Делать | Дор | 85 | Опровергнутые претензии на открытие астата . | [nb 2] | [9] |
| Dn | Дубнадиум | 118 | Предлагаемое название для оганессона . | [№ 3] | |
| Дп | Decipium | 62 | Делафонтен ошибочно считал деципий новым элементом. Фактически был самарий . | ||
| Ds | Диспрозий | 66 | Текущий символ - Dy . Этот символ теперь используется для дармштадтиума . | [nb 1] | |
| Dt | Двителлуриум | 84 | Имя, данное Менделеевым какому-то еще неоткрытому элементу. Когда обнаруженный полоний полностью соответствовал предсказанию. | [№ 3] [№ 4] | |
| E | Эйнштейний | 99 | Текущий символ - Es . | [nb 1] | |
| E | Эрбий | 68 | Текущий символ - Er . | [nb 1] | |
| Ea | Экаалюминий | 31 год | Имя, данное Менделеевым какому-то еще неоткрытому элементу. Когда обнаруженный галлий полностью соответствовал предсказанию. | [№ 3] [№ 4] | |
| Eb | Екаборон | 21 год | Имя, данное Менделеевым какому-то еще неоткрытому элементу. Когда обнаруженный скандий полностью соответствовал предсказанию. | [№ 3] [№ 4] | [7] |
| Eb | Эребодиум | 42 | Александр Прингл ошибочно считал эребодиум новым элементом. Фактически был молибден . | ||
| Эль | Экаалюминий | 31 год | Имя, данное Менделеевым какому-то еще неоткрытому элементу. Когда обнаруженный галлий полностью соответствовал предсказанию. | [№ 3] [№ 4] | [7] |
| Эм | Экаманганец | 43 год | Имя, данное Менделеевым какому-то еще неоткрытому элементу. Когда обнаруженный технеций полностью соответствовал предсказанию. | [№ 3] [№ 4] | [7] |
| Эм | Эманация | 86 | Также называемый «излучением радия», это название было первоначально дано Фридрихом Эрнстом Дорном в 1900 году. В 1923 году этот элемент официально стал радоном (одно время так называли 222 Rn, изотоп, идентифицированный в цепи распада радия ). | [nb 1] | [7] |
| Эм | Эманий | 89 | Альтернативное название, ранее предложенное для актиния . | [№ 3] | |
| Es | Экасиликон | 32 | Имя, данное Менделеевым еще не обнаруженному элементу. Когда обнаруженный германий полностью соответствовал предсказанию. Этот символ теперь используется для обозначения эйнштейния . | [№ 3] [№ 4] | [7] |
| Es | Эспериум | 94 | Опровергнутые претензии на открытие плутония . Этот символ теперь используется для обозначения эйнштейния . | [nb 2] | [7] |
| Et | Экатантал | 91 | Имя, данное Менделеевым какому-то еще неоткрытому элементу. Когда обнаруженный протактиний полностью соответствовал предсказанию. | [№ 3] [№ 4] | |
| Бывший | Эвксениум | 72 | Опровергнутые претензии на открытие гафния . | [nb 2] | |
| Fa | Франций | 87 | Текущий символ Fr . | [nb 1] | |
| Fl | Флорентий | 61 | Опровергнутые претензии на открытие прометия . Этот символ теперь используется для флеровиума . | [nb 2] | |
| Fl | Фтор | 9 | Текущий символ F . Этот символ теперь используется для флеровиума . | [nb 1] | |
| Пт | Флорентий | 61 | Опровергнутые претензии на открытие прометия . Этот символ теперь используется для франция . | [nb 2] | [7] |
| грамм | Глюциний | 4 | Прежнее название бериллия . | [nb 1] | |
| Gh | Гиорсиум | 118 | Опроверженная претензия на открытие оганессона . | [nb 2] | |
| Gl | Глюциний | 4 | Прежнее название бериллия . | [nb 1] | [7] |
| Ха | Hahnium | 105 | Предлагаемое название для дубниума . | [№ 3] | |
| Hn | Hahnium | 108 | Предлагаемое название для хасиума . | [№ 3] | [7] |
| Hv | Гельвеций | 85 | Опровергнутые претензии на открытие астата . | [nb 2] | [9] |
| Hy | Меркурий | 80 | Hy от греческого hydrargyrum для «жидкого серебра». Текущий символ - Hg . | [nb 1] | [6] |
| я | Иридий | 77 | Текущий символ - Ir . Этот символ теперь используется для йода . | [nb 1] | |
| IC | Инкогнитиум | 65 | Демарчай ошибочно считал инкогнитум новым элементом. На самом деле был тербий . | ||
| Il | Иллиний | 61 | Опровергнутые претензии на открытие прометия . | [nb 2] | [7] |
| Il | Ильмениум | 41/73 | Смесь элементов ниобия и тантала . Р. Германн ошибочно считал ильмений элементом. | ||
| Ио | Ионий | 65 | Демарса ошибочно считал ионий новым элементом. На самом деле был тербий . | ||
| J | Джодиум | 53 | Прежнее название йода . | [nb 1] | |
| Jg | Жаргониум | 72 | Опровергнутые претензии на открытие гафния . | [nb 2] | [7] |
| Jl | Joliotium | 105 | Предлагаемое название для дубниума . | [№ 3] | [7] |
| Jp | Японский | 113 | Предлагаемое название для нихония . | [№ 3] | |
| Ка | Калий | 19 | Текущий символ K . | [nb 1] | |
| Ку | Курчатовий | 104 | Предлагаемое название резерфордия . | [№ 3] | [7] |
| L | Литий | 3 | Текущий символ - Ли . | [nb 1] | |
| Lw | Лоуренсий | 103 | Текущий символ - Lr . | [nb 1] | |
| M | Муриатикум | 17 | Прежнее название хлора . | [nb 1] | |
| Ма | Марганец | 25 | Текущий символ - Mn . | [nb 1] | |
| Ма | Мазурий | 43 год | Оспариваемая претензия на открытие технеция . | [nb 2] | [7] |
| Мкр | Менделевий | 97 | Предлагаемое название для беркелиума . Позже символ и название использовались для элемента 101. | [nb 1] [nb 3] | |
| Мл | Молдавиум | 87 | Опровергнутые претензии на открытие франция . | [nb 2] | [9] |
| РС | Магний | 12 | Текущее обозначение - Mg . | [nb 1] | |
| РС | Масриум | 88 | Опровергнутые претензии на открытие радия . | [nb 2] | |
| РС | Мазурий | 43 год | Оспариваемая претензия на открытие технеция . | [nb 2] | |
| РС | Мосандриум | 65 | Смит ошибочно считал мозандрий новым элементом. На самом деле был тербий . | ||
| Мв | Менделевий | 101 | Текущий символ - Md . | [nb 1] | |
| Нг | Норвегия | 72 | Опровергнутые претензии на открытие гафния . | [nb 2] | |
| Нет | Норий | 72 | Опровергнутые претензии на открытие гафния . Этот символ теперь используется для обозначения нобелия . | [nb 2] | |
| Np | Нептуний | 91 | Опровергнутые претензии на открытие протактиния . Позже символ и название использовались для элемента 93. | [nb 2] | [11] |
| Np | Ниппониум | 43 год | Опровергнутые претензии на открытие технеция . Этот символ теперь используется для обозначения нептуния . | [nb 2] | [7] |
| Ns | Nielsbohrium | 105 | Предлагаемое название для дубниума . | [№ 3] | [7] |
| Ns | Nielsbohrium | 107 | Предлагаемое название бориума . | [№ 3] | [7] |
| Nt | Нитон | 86 | Прежнее название радона . | [nb 1] | [7] |
| Нью-Йорк | Неойттербий | 70 | Прежнее название иттербия . | [nb 1] | |
| п | Вести | 82 | Текущий символ - Pb . Этот символ теперь используется для фосфора . | [nb 1] | |
| Па | Палладий | 46 | Текущий символ - Pd . Этот символ теперь используется для протактиниума . | [nb 1] | |
| Pe | Пелопиум | 41 год | Прежнее название ниобия . | [nb 1] | |
| Ph | Фосфор | 15 | Текущий символ P . | [nb 1] | |
| Pl | Палладий | 46 | Текущий символ - Pd . | [nb 1] | |
| Вечера | Полимнестум | 33 | Александр Прингл ошибочно считал полиместум новым элементом. На самом деле был мышьяк . Этот символ теперь используется для прометия . | ||
| По | Калий | 19 | Текущий символ K . Этот символ теперь используется для обозначения полония . | [nb 1] | |
| Пп | Филиппий | 67 | Делафонтен ошибочно считал филиппиум новым элементом. Фактически был гольмий . | ||
| р | Родий | 45 | Текущий символ - Rh . (Этот символ сейчас иногда используется для обозначения алкильной группы.) | [nb 1] | |
| Rd | Радий | 88 | Текущий символ - Ра . | [nb 1] | |
| Rf | Резерфордий | 106 | Предлагаемое название сиборгиума . Вместо этого символ и имя использовались для элемента 104. | [nb 1] [nb 3] | [7] |
| Ro | Родий | 45 | Текущий символ - Rh . | [nb 1] | |
| Сб | Самарий | 62 | Текущий символ - Sm . | [nb 1] | [7] |
| Так | Натрий | 11 | Текущий символ - Na . | [nb 1] | |
| Кв. | Sequanium | 93 | Опровергнутые претензии на открытие нептуния . | [nb 2] | |
| Ул. | Сурьма | 51 | Текущий символ - Sb . | [nb 1] | |
| Ул. | Банка | 50 | Текущий символ - Sn . | [nb 1] | |
| Тм | Триманганец | 75 | Имя, данное Менделеевым какому-то еще неоткрытому элементу. Когда он был обнаружен, рений полностью совпал с предсказанием. Этот символ теперь используется для тулия . | [№ 3] [№ 4] | |
| Тн | Вольфрам | 74 | Текущий символ W . | [nb 1] | |
| Тр | Тербий | 65 | Текущий символ - Tb . | [nb 1] | |
| Вт | Тулий | 69 | Текущий символ - Tm . | [nb 1] | |
| Вт | Вольфрам | 74 | Текущий символ W . | [nb 1] | |
| Unb | Уннильбиум | 102 | Временное название, данное нобелиуму, пока он не получил постоянного названия от IUPAC. | [№ 4] | |
| Une | Unnilennium | 109 | Временное название, данное мейтнерию, до тех пор, пока оно не будет присвоено ему постоянное название IUPAC. | [№ 4] | |
| Ун | Уннилгексий | 106 | Временное название сиборгиума до тех пор, пока он не получил постоянного названия от IUPAC. | [№ 4] | |
| Уно | Unniloctium | 108 | Временное название, присвоенное хасиуму, пока оно не было присвоено постоянное название ИЮПАК. | [№ 4] | |
| Unp | Unnilpentium | 105 | Временное имя, присвоенное дубниуму, пока ИЮПАК не присвоил ему постоянное имя. | [№ 4] | |
| Unq | Unnilquadium | 104 | Временное название резерфордия, пока он не получил постоянного названия ИЮПАК. | [№ 4] | |
| Uns | Unnilseptium | 107 | Временное название, данное бориуму, до тех пор, пока оно не было окончательно названо ИЮПАК. | [№ 4] | |
| Нет | Уннильтриум | 103 | Временное название было присвоено лоуренсиуму, пока оно не было присвоено постоянное название ИЮПАК. | [№ 4] | |
| Уну | Уннилуниум | 101 | Временное название, данное менделевию, до тех пор, пока оно не было окончательно названо ИЮПАК. | [№ 4] | |
| Ууб | Унунбиум | 112 | Временное название, данное copernicium, до тех пор, пока оно не будет присвоено ему постоянное название IUPAC. | [№ 4] | |
| Уу | Унунгексий | 116 | Временное название, данное ливермориуму, до тех пор, пока ИЮПАК не присвоил ему постоянное название. | [№ 4] | |
| Уун | Унуннилиум | 110 | Временное название, данное дармштадтиуму, пока оно не было присвоено постоянное название ИЮПАК. | [№ 4] | |
| Ууо | Ununoctium | 118 | Временное имя, присвоенное оганессону, пока оно не было присвоено ему постоянное название IUPAC. | [№ 4] | |
| Uup | Унунпентиум | 115 | Временное название московий, пока он не получил постоянного названия ИЮПАК. | [№ 4] | |
| Uuq | Ununquadium | 114 | Временное название, данное флеровию, пока оно не было присвоено ему постоянное название ИЮПАК. | [№ 4] | |
| Uus | Ununseptium | 117 | Временное название, данное теннессину, до тех пор, пока ИЮПАК не присвоил ему постоянное название. | [№ 4] | |
| Уут | Ununtrium | 113 | Временное название, данное имонию, до тех пор, пока ИЮПАК не присвоил ему постоянное название. | [№ 4] | |
| Ууу | Унунниум | 111 | Временное название, данное рентгениуму, до тех пор, пока оно не будет присвоено ему постоянное название ИЮПАК. | [№ 4] | |
| Ура | Урал | 75 | Опровергнутые претензии на открытие рения . | [nb 2] | |
| Ура | Уран | 92 | Текущий символ U . | [nb 1] | |
| Vc | Викториум | 64 | Крукс ошибочно полагал, что победа - это новый элемент. Фактически был гадолиний . | ||
| Vi | Викториум | 64 | Крукс ошибочно полагал, что победа - это новый элемент. Фактически был гадолиний . | ||
| Vi | Вирджиния | 87 | Опровергнутые претензии на открытие франция . | [nb 2] | [7] |
| Vm | Вирджиния | 87 | Опровергнутые претензии на открытие франция . | [nb 2] | [7] |
| Ва | Ванадий | 23 | Текущий символ V . | [nb 1] | |
| Wo | Вольфрам | 74 | Текущий символ W . | [nb 1] | |
| Икс | Ксенон | 54 | Текущий символ - Xe . Этот символ теперь используется для галогенов . | [nb 1] | |
| Yt | Иттрий | 39 | Текущий символ Y . | [nb 1] | [7] |
Пиктографические символы [ править ]
Ниже приводится список пиктографических символов, используемых для обозначения элементов, известных с древних времен (например, алхимиков ). В этот список не включены символические изображения веществ, ранее называвшихся элементами (таких как смеси некоторых редкоземельных минералов и классических элементов огня и воды древней философии), которые сегодня известны как многоатомные. Также не включены символические представления, используемые в настоящее время для элементов на других языках, такие как китайские иероглифы для элементов . Современные буквенные обозначения были введены в 1814 году Йенсом Якобом Берцелиусом . [12]
| Химический символ | Оригинальное название | Современное название | Атомный номер | Происхождение символа |
|---|---|---|---|---|
| ☉ | Водород | Водород | 1 | Дальтонский символ около 1808 года. |
| ⬤ | Углерод | Углерод | 6 | Дальтонский символ около 1808 года. |
| ⦶ | Азоте | Азот | 7 | Дальтонский символ около 1808 года. |
| ◯ | Кислород | Кислород | 8 | Дальтонский символ около 1808 года. |
| ⦷ | Газировка | Натрий | 11 | Дальтонский символ около 1808 года. |
| ⊛ | Магний | Магний | 12 | Алхимический символ. Также принят в качестве символа магния Дальтоном в 1808 году. |
| 🟕 | Кремний | Кремний | 14 | Дальтонский символ около 1808 года. |
| Сера | Сера | 16 | Алхимический символ. | |
| Паллада | Сера | 16 | Алхимический символ. | |
| 🜍 | Сера | Сера | 16 | Алхимический символ. |
| ⴲ | Сера | Сера | 16 | Дальтонский символ около 1808 года. |
| ⦾ | Кальций | Кальций | 20 | Дальтонский символ около 1808 года. |
| ♂ | Марс | Утюг | 26 год | Алхимический символ. |
| Ⓘ | Утюг | Утюг | 26 год | Дальтонский символ около 1808 года. |
| Ⓝ | Никель | Никель | 28 год | Дальтонский символ около 1808 года. |
| Stellae Fixae | Медь | 29 | Алхимический символ до XVI века . | |
| ♀ | Венера | Медь | 29 | Алхимический символ. |
| Медь | Медь | 29 | Алхимический символ. | |
| Ⓒ | Медь | Медь | 29 | Дальтонский символ около 1808 года. |
| Ⓩ | Цинк | Цинк | 30 | Дальтонский символ около 1808 года. |
| Мышьяк | Мышьяк | 33 | Алхимический символ. | |
| 🜺 | Мышьяк | Мышьяк | 33 | Алхимический символ. |
| ⊕ | Иттрий | Иттрий | 39 | Дальтонский символ около 1808 года. |
| ☽ | Луна | Серебро | 47 | Алхимический символ. |
| 🜛 | Серебро | Серебро | 47 | Алхимический символ. |
| Ⓢ | Серебро | Серебро | 47 | Дальтонский символ около 1808 года. |
| ♃ | Юпитер | Банка | 50 | Алхимический символ. |
| Ⓣ | Банка | Банка | 50 | Дальтонский символ около 1808 года. |
| ♁ | Сурьма | Сурьма | 51 | Алхимический символ. |
| ☉☾ | Платина | Платина | 78 | Алхимический символ. |
| ⛢ | Уран | Платина | 78 | Алхимический символ. |
| Ⓟ | Платина | Платина | 78 | Дальтонский символ около 1808 года. |
| ☼ | Sol | Золото | 79 | Алхимический символ 16 века. |
| ☉ | Sol | Золото | 79 | Алхимический символ с 1700 по 1783 год. |
| 🜚 | Золото | Золото | 79 | Алхимический символ. |
| Ⓖ | Золото | Золото | 79 | Дальтонский символ около 1808 года. |
| ♓︎ | Рыбы | Меркурий | 80 | Алхимический символ до XVI века . |
| ♆ | Нептун | Меркурий | 80 | Алхимический символ 17 века. |
| ☿ | Меркурий | Меркурий | 80 | Алхимический символ с 1700 по 1783 год. |
| ♄ | Сатурн | Вести | 82 | Алхимический символ около 1783 года. |
| Ⓛ | Вести | Вести | 82 | Дальтонский символ около 1808 года. |
| ♉︎ | Телец | Висмут | 83 | Алхимический символ. |
| Ⓑ | Висмут | Висмут | 83 | Дальтонский символ около 1808 года. |
| Ⓤ | Уран | Уран | 92 | Дальтонский символ около 1808 года. |
Символы названных изотопов [ править ]
Ниже приводится список изотопов элементов, приведенных в предыдущих таблицах, которые обозначены уникальными символами. Это означает, что исчерпывающий список текущих систематических символов (в форме u Atom) не включен в список и вместо этого может быть найден в таблице индекса изотопов . Символы названных изотопов водорода , дейтерия (D) и трития (T) все еще используются сегодня, как и торон (Tn) для радона-220 (но не актинона ; An обычно используется вместо общего актинида ). . Тяжелая вода и другие дейтерированные растворителиобычно используются в химии, и в этих случаях удобно использовать одиночный символ, а не символ с нижним индексом. Эта практика продолжается и с соединениями трития. Когда дается название растворителя, иногда используется буква d в нижнем регистре. Например, d 6 -бензол и C 6 D 6 можно использовать вместо [ 2 H 6 ] C 6 H 6 . [13]
Символы для изотопов элементов, отличных от водорода и радона, больше не используются в научном сообществе. Многие из этих символов были назначены в первые годы радиохимии и несколько изотопов (а именно в цепочках распада из актиний , радий и торий ) медведь экземплификант с использованием системы раннего именовании изобретенный Эрнест Резерфорд . [14]
| Химический символ | Имя | Атомный номер | Происхождение символа |
|---|---|---|---|
| Ac | Актиний | 89 | От греческого актинос . Одно время название ограничивалось 227 Ac, изотопом актиния . Этот названный изотоп позже стал официальным названием элемента 89 . |
| AcA | Актиний А | 84 | От актиния и A. Название-заполнитель, данное когда-то 215 Po, изотопу полония, идентифицированному в цепи распада актиния . |
| AcB | Актиний B | 82 | От актиния и B. Имя-заполнитель, данное когда-то 211 Pb, изотопу свинца, идентифицированному в цепи распада актиния . |
| AcC | Актиний С | 83 | От актиния и C. Название-заполнитель, данное когда-то 211 Bi, изотопу висмута, идентифицированному в цепи распада актиния . |
| AcC ' | Актиний C ' | 84 | Из актиния и C ' . Имя-заполнитель, данное когда-то 211 Po, изотопу полония, идентифицированному в цепи распада актиния . |
| AcC " | Актиний C " | 81 год | От актиния и C " . Имя-заполнитель, данное когда-то 207 Tl, изотопу таллия, идентифицированному в цепи распада актиния . |
| AcK | Актиний К | 87 | Название, данное когда-то 223 Fr, изотопу франция, идентифицированному в цепи распада актиния . |
| AcU | Актино-урановый | 92 | Название, данное когда-то 235 U, изотопу урана . |
| AcX | Актиний X | 88 | Название, данное когда-то 223 Ra, изотопу радия, идентифицированному в цепи распада актиния . |
| An | Актинон | 86 | Из актина мика и emanati на . Название, данное когда-то 219 Rn, изотопу радона, идентифицированному в цепи распада актиния . |
| D | Дейтерий | 1 | От греческого deuteros . Название дано 2 H. |
| Ио | Ионий | 90 | Название дано 230 Th, изотопу тория, идентифицированному в цепи распада урана . |
| MsTh 1 | Мезоторий 1 | 88 | Название, данное когда-то 228 Ra, изотопу радия . |
| MsTh 2 | Мезоторий 2 | 89 | Название, данное когда-то 228 Ас, изотопу актиния . |
| Па | Протактиний | 91 | От греческих протос и актиний . Одно время название ограничивалось 231 Па, изотопом протактиния . Этот названный изотоп позже стал официальным названием элемента 91 . |
| Ра | Радий | 88 | От латинского радиуса . Одно время название ограничивалось 226 Ra, изотопом радия . Этот названный изотоп позже стал официальным названием элемента 88 . |
| RaA | Радий А | 84 | От радия и A. Название-заполнитель, данное когда-то 218 Po, изотопу полония, идентифицированному в цепи распада радия . |
| RaB | Радий B | 82 | От радия и B. Имя-заполнитель, данное когда-то 214 Pb, изотопу свинца, идентифицированному в цепи распада радия . |
| RaC | Радий C | 83 | От радия и C. Название-заполнитель, данное когда-то 214 Bi, изотопу висмута, идентифицированному в цепи распада радия . |
| RaC ' | Радий C ' | 84 | Из радия и C ' . Имя-заполнитель, данное когда-то 214 Po, изотопу полония, идентифицированному в цепи распада радия . |
| RaC " | Радий C " | 81 год | От радия и C » . Имя-заполнитель, данное когда-то 210 Tl, изотопу таллия, идентифицированному в цепи распада радия . |
| RaD | Радий D | 82 | От радия и D. Название-заполнитель, данное когда-то 210 Pb, изотопу свинца, идентифицированному в цепи распада радия . |
| RaE | Радий E | 83 | От радия и E. Название-заполнитель, данное когда-то 210 Bi, изотопу висмута, идентифицированному в цепочке распада радия . |
| RaE " | Радий E " | 81 год | От радия и E » . Имя-заполнитель, данное когда-то 206 Tl, изотопу таллия, идентифицированному в цепи распада радия . |
| RaF | Радий F | 84 | От радия и F. Название-заполнитель, данное когда-то 210 Po, изотопу полония, идентифицированному в цепи распада радия . |
| RdAc | Радиоактиний | 90 | Одно время было названо 227 Th, изотоп тория . |
| RdTh | Радиоторий | 90 | Одно время было дано название 228 Th, изотопу тория . |
| Rn | Радон | 86 | От радиан мика и emanati на . Название ограничивалось когда-то 222 Rn, изотопом радона, идентифицированным в цепочке распада радия . Этот названный изотоп позже стал официальным названием элемента 86 в 1923 году. |
| Т | Тритий | 1 | От греческого тритоса . Название дано 3 H. |
| Чт | Торий | 90 | После Тора . Одно время название ограничивалось 232 Th, изотопом тория . Этот названный изотоп позже стал официальным названием элемента 90 . |
| ThA | Торий А | 84 | От тория и A. Название-заполнитель, данное когда-то 216 Po, изотопу полония, идентифицированному в цепи распада тория . |
| ThB | Торий B | 82 | От тория и B. Название-заполнитель, данное когда-то 212 Pb, изотопу свинца, идентифицированному в цепи распада тория . |
| ThC | Торий C | 83 | От тория и C. Название-заполнитель, данное когда-то 212 Bi, изотопу висмута, идентифицированному в цепи распада тория . |
| ThC ' | Торий C ' | 84 | Из тория и C ' . Имя-заполнитель, данное когда-то 212 Po, изотопу полония, идентифицированному в цепи распада тория . |
| ThC " | Торий C " | 81 год | От тория и C " . Имя-заполнитель, данное когда-то 208 Tl, изотопу таллия, идентифицированному в цепи распада тория . |
| Спасибо | Торий X | 88 | Название, данное когда-то 224 Ra, изотопу радия, идентифицированному в цепи распада тория . |
| Тн | Торон | 86 | От Thor мика и emanati на . Одно время было присвоено имя 220 Rn, изотопу радона, идентифицированному в цепи распада тория . |
| UI | Уран I | 92 | Название, данное когда-то 238 U, изотопу урана . |
| UII | Уран II | 92 | Название, данное когда-то 234 U, изотопу урана . |
| UX 1 | Уран X 1 | 90 | Название, данное когда-то 234 Th, изотопу тория, идентифицированному в цепи распада урана . |
| UX 2 | Уран X 2 | 91 | Одно время было присвоено имя 234 млн Па, изотопа протактиния, идентифицированного в цепи распада урана . |
| UY | Уран Y | 90 | Название, данное когда-то 231 Th, изотопу тория, идентифицированному в цепи распада урана . |
| UZ | Уран Z | 91 | Одно время было присвоено имя 234 Па, изотопу протактиния, идентифицированному в цепи распада урана . |
Другие символы [ править ]
Общий:
- A: Депротонированная кислота или анион
- An: любой актинид
- B: основание , часто в контексте Льюиса кислотно-основной теории или Бренстеда-Лоури теории кислотно-щелочного
- E: любой элемент или электрофил
- L: любой лиганд
- Ln: любой лантаноид
- М: любой металл
- Мм: мишметалл (иногда используется) [15]
- Ng: любой благородный газ (иногда используется Rg, но он также используется для элемента рентгений : см. Выше)
- Nu: любой нуклеофил
- R: любой неуказанный радикал ( фрагмент ), не важный для обсуждения.
- St: сталь (иногда используется)
- X: любой галоген (или иногда псевдогалоген )
Из органической химии:
- Ac: ацетил - (также используется для элемента актиний : см. Выше)
- Ad: 1- адамантил
- Все: allyl
- Am: амил ( пентил ) - (также используется для элемента америций : см. Выше)
- Ar: арил - (также используется для элемента аргон : см. Выше)
- Bn: бензил
- BS : брошил или (устаревший) бензолсульфонил
- Bu: бутил ( префиксы i -, s - или t - могут использоваться для обозначения изо -, втор - или трет - изомеров, соответственно)
- Bz: бензоил
- Cp: циклопентадиенил
- Cp *: пентаметилциклопентадиенил
- Cy: циклогексил
- Цип: циклопентил
- Et: этил
- Я: метил
- Mes: мезитил (2,4,6-триметилфенил)
- Ms: мезил (метилсульфонил)
- Np: неопентил - (также используется для элемента нептуний : см. Выше)
- Ns: нозил
- Пент: пентил
- Ph, Φ : фенил
- Pr: пропил - ( префикс i - может использоваться для обозначения изопропила. Также используется для элемента празеодим : см. Выше)
- R: В контексте органической химии неопределенный "R" часто понимается как алкильная группа.
- Tf: трифлил (трифторметансульфонил)
- Tr, Trt: тритил (трифенилметил)
- Ts, Tos: тозил ( пара- толуолсульфонил) - (Ts также используется для элемента теннессин : см. Выше)
- Vi: винил
Экзотические атомы:
- Mu: мюоний
- Pn: протоний
- Ps: позитроний
См. Также [ править ]
- Список химических элементов, называющих споры
- Список элементов
- Ядерная запись
Заметки [ править ]
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw топор ay az ba bb Имя изменено в связи со стандартизацией, модернизацией или обновлением старого ранее использовавшегося символа.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae Имя, указанное дискредитированным / оспариваемым заявителем.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y Имя, предложенное до открытия / создания элемента или до официального переименования имени заполнителя.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa Имя временного заполнителя.
Ссылки [ править ]
- ^ Предварительные рекомендации ИЮПАК: IR-3: Элементы и группы элементов (PDF) (Отчет). ИЮПАК . Март 2004 г.
- ^ "Периодическая таблица - Королевское химическое общество" . www.rsc.org .
- ^ "Интернет-словарь этимологии" . etymonline.com .
- ^ Визер, Майкл Э .; и другие. (2013). Атомный вес элементов 2011 (Технический отчет IUPAC). Pure Appl. Chem. (Отчет). 85 . С. 1047–1078. DOI : 10.1351 / PAC-REP-13-03-02 . (для стандартных атомных весов элементов)
- ^ Sonzogni, Алехандро. «Интерактивная карта нуклидов» . Национальный центр ядерных данных: Брукхейвенская национальная лаборатория . Проверено 6 июня 2008 . (для атомных масс элементов с атомными номерами 103–118)
- ↑ a b Holden, NE (12 марта 2004 г.). «История происхождения химических элементов и их первооткрывателей» . Национальный центр ядерных данных .
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad Leal, João P. (2013). «Забытые названия химических элементов». Основы науки . 19 (2): 175–183. DOI : 10.1007 / s10699-013-9326-у .
- ^ а б "Фред Эллисон" . Энциклопедия Алабамы .
- ^ Б с д е е г Fontani, Marco ; Коста, Мариагразия; Орна, Мэри Вирджиния (2014). Утраченные элементы: теневая сторона периодической таблицы . Издательство Оксфордского университета . ISBN 9780199383344.
- ^ a b Празеодим на was.chemistryexplained.com.
- ^ Ранг, Ф. (1895). «Периодическая таблица». Химические новости и журнал физических наук . 72 : 200–201.
- ^ Берцелиус, Йенс Якоб. «Очерк о причине химических пропорций и некоторых связанных с ними обстоятельствах: вместе с кратким и простым методом их выражения». Анналы философии 2, стр. 443–454 (1813); 3, С. 51–52, 93–106, 244–255, 353–364 (1814); (Впоследствии переиздано в "A Source Book in Chemistry, 1400-1900", ред. Leicester, Henry M. & Herbert S. Klickstein. 1952 г.)
- ^ ИЮПАК. «Изотопно модифицированные соединения» . ИЮПАК . Проверено 31 марта 2015 года .
- ^ Морган, GT, изд. (1905). «Годовые отчеты о развитии химии за 1904 год». Журнал химического общества . Герни и Джексон. 1 : 268.
Ввиду чрезвычайно сложной природы более поздних изменений, происходящих в Radium, Резерфорд предложил новую и удобную систему номенклатуры.
Первый продукт изменения эманации радия называется радием A, следующий - радием B и так далее.
- ^ Юрчик, М .; Rajewski, W .; Majchrzycki, W .; Вуйчик, Г. (30 августа 1999 г.). «Механически легированные материалы типа MmNi 5 для металлогидридных электродов». Журнал сплавов и соединений . 290 (1–2): 262–266. DOI : 10.1016 / S0925-8388 (99) 00202-9 .
- Elementymology & Elements Multidict , этимологии названий элементов. Проверено 15 июля 2005 года.
- Атомный вес элементов 2001, Pure Appl. Chem. 75 (8), 1107–1122, 2003 . Получено 30 июня 2005 г. Атомные веса элементов с атомными номерами от 1 до 109 взяты из этого источника.
- Стандартные атомные веса ИЮПАК пересмотрены (2005 г.).
- Периодическая таблица WebElements . Получено 30 июня 2005 г. Атомные веса элементов с атомными номерами 110–116 взяты из этого источника.
- Лапп, Ральф Э. Материя . Библиотека наук о жизни. Нью-Йорк: Time, Inc., 1963.
- Лейтон, Роберт Б. Принципы современной физики . Нью-Йорк: Макгроу-Хилл. 1959 г.
- Scerri, ER "Периодическая таблица, ее история и ее значение". Нью-Йорк, издательство Оксфордского университета. 2007 г.
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме химических символов . |
- Список элементов Берцелиуса
- История значений атомной массы ИЮПАК (1883-1997 гг.)
- Комитет по номенклатуре, терминологии и символам , Американское химическое общество