| |||
| Имена | |||
|---|---|---|---|
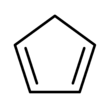
| Предпочтительное название IUPAC Циклопента-1,3-диен | |||
| Другие имена | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| Сокращения | CPD, HCp | ||
| 471171 | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.008.033 | ||
| Номер ЕС |
| ||
| 1311 | |||
| MeSH | 1,3-циклопентадиен | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 5 Н 6 | |||
| Молярная масса | 66,103 г · моль -1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | раздражающим, терпен -как [1] | ||
| Плотность | 0,786 г см −3 | ||
| Температура плавления | −90 ° С; -130 ° F; 183 К | ||
| Точка кипения | От 39 до 43 ° С; От 102 до 109 ° F; От 312 до 316 К | ||
| нерастворимый [1] | |||
| Давление газа | 400 мм рт. Ст. (53 кПа) [1] | ||
| Кислотность (p K a ) | 16 | ||
| Основание конъюгата | Циклопентадиенил анион | ||
| −44,5 × 10 −6 см 3 моль −1 | |||
| Структура | |||
Молекулярная форма | Планарный [3] | ||
| Термохимия | |||
Теплоемкость ( C ) | 115,3 Дж -1 моль -1 | ||
Стандартная мольная энтропия ( S | 182,7 Дж -1 моль -1 | ||
| Опасности | |||
| точка возгорания | 25 ° С (77 ° F, 298 К) | ||
| Смертельная доза или концентрация (LD, LC): | |||
ЛК 50 ( средняя концентрация ) | 14 182 частей на миллион (крыса, 2 часа) 5091 частей на миллион (мышь, 2 часа) [4] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 75 частей на миллион (200 мг / м 3 ) [1] | ||
REL (рекомендуется) | TWA 75 частей на миллион (200 мг / м 3 ) [1] | ||
IDLH (Непосредственная опасность) | 750 частей на миллион [1] | ||
| Родственные соединения | |||
Связанные углеводороды | Бензол Циклобутадиен Циклопентен | ||
Родственные соединения | Дициклопентадиен | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Циклопентадиен представляет собой органическое соединение с формулой C 5 H 6 . [5] Его часто называют сокращенно CpH, потому что циклопентадиенильный анион сокращенно называют Cp - .
Эта бесцветная жидкость имеет сильный неприятный запах . При комнатной температуре этот циклический диен димеризуется в течение нескольких часов с образованием дициклопентадиена посредством реакции Дильса-Альдера . Этот димер можно восстановить нагреванием до мономера.
Соединение в основном используется для производства циклопентена и его производных. Он широко используется в качестве предшественника циклопентадиенильного аниона (Cp - ), важного лиганда в циклопентадиенильных комплексах в металлоорганической химии . [6]
Производство и реакции [ править ]
Производство циклопентадиена обычно не отличается от образования дициклопентадиена, поскольку они взаимно превращаются. Их получают из каменноугольной смолы (около 10-20 г / т) , а также с помощью пара крекинга из нафты (около 14 кг / тонну). [7] Для получения циклопентадиенового мономера коммерческий дициклопентадиен подвергают крекингу при нагревании примерно до 180 ° C. Мономер собирают перегонкой и вскоре после этого используют. [8]
Сигматропная перестройка [ править ]
Атомы водорода в циклопентадиене претерпевают быстрые [1,5] -сигматропные сдвиги, о чем свидетельствуют спектры 1 H ЯМР, записанные при различных температурах. [9] Еще более подвижны производные C 5 H 5 E (CH 3 ) 3 (E = Si , Ge , Sn ), в которых более тяжелый элемент мигрирует от углерода к углероду с низким активационным барьером.
Реакции Дильса – Альдера [ править ]
Циклопентадиен является диеном с высокой реакционной способностью в реакции Дильса-Альдера, поскольку для достижения геометрии оболочки переходного состояния требуется минимальное искажение диена по сравнению с другими диенами. [10] Известно, что циклопентадиен димеризуется. Превращение происходит в часах при комнатной температуре, но мономер можно хранить в течение нескольких дней при -20 ° C. [7]
Депротонирование [ править ]
Соединение представляет собой необычно кислое (р К = 16) для углеводорода , и этот факт объясняется высокой стабильностью ароматического циклопентадиенильного аниона , C
5ЧАС-
5. Депротонирование может быть достигнуто с помощью различных оснований, обычно гидрида натрия, металлического натрия и бутиллития . Соли этого аниона являются коммерчески доступными, в том числе циклопентадиенилнатрий и cyclopentadienide лития . Их используют для получения циклопентадиенильных комплексов .
Производные металлоцена [ править ]
Металлоцены и родственные циклопентадиенильные производные были тщательно изучены и представляют собой краеугольный камень металлоорганической химии благодаря своей высокой стабильности. Первый охарактеризованный металлоцен, ферроцен , был получен так же, как и многие другие металлоцены: путем объединения производных щелочных металлов в форме MC 5 H 5 с дигалогенидами переходных металлов : [12] В качестве типичного примера, никелоцен образуется при обработке никеля (II ) хлорид с циклопентадиенидом натрия в ТГФ . [13]
- NiCl 2 + 2 NaC 5 H 5 → Ni (C 5 H 5 ) 2 + 2 NaCl
Металлоорганические комплексы, которые включают как циклопентадиенильный анион, так и сам циклопентадиен, известны, одним из примеров которых является производное родоцена , полученное из мономера родоцена в протонных растворителях . [14]
Органический синтез [ править ]
Это был исходный материал в синтезе додекаэдрана Лео Пакеттом в 1982 году . [15] Первый этап включал восстановительную димеризацию молекулы с образованием дигидрофульвалена , а не простое добавление с образованием дициклопентадиена.
Использует [ редактировать ]
Помимо использования в качестве предшественника катализаторов на основе циклопентадиенила, основным коммерческим применением циклопентадиена является его использование в качестве предшественника сомономеров . Полугидрогенизация дает циклопентен . Реакция Дильса-Альдера с бутадиеном дает этилиденнорборнен , сомономер при производстве каучуков EPDM .
Производные [ править ]
Циклопентадиен может замещать один или несколько атомов водорода, образуя производные с ковалентными связями:
- Объемные циклопентадиены
- Калицен
- Циклопентадиенон
- Ди- трет -butylcyclopentadiene
- Метилциклопентадиен
- Пентаметилциклопентадиен
- Пентацианоциклопентадиен
Большинство этих замещенных циклопентадиенов могут также образовывать анионы и присоединяться к циклопентадиенильным комплексам .
См. Также [ править ]
- Ароматичность
Ссылки [ править ]
- ^ a b c d e f g Карманное руководство NIOSH по химическим опасностям. «# 0170» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Уильям М. Хейнс (2016). Справочник по химии и физике CRC [ Физические константы органических соединений ]. 97 . CRC Press / Тейлор и Фрэнсис. п. 276 (3-138). ISBN 978-1498754286.
- ^ Фаустов, Валерий I .; Егоров, Михаил П .; Нефедов Олег М .; Молин, Юрий Н. (2000). «Ab initio G2 и DFT расчеты сродства к электрону циклопентадиена, силола, гермола и их 2,3,4,5-тетрафенилзамещенных аналогов: структура, стабильность и параметры ЭПР анион-радикалов». Phys. Chem. Chem. Phys . 2 (19): 4293–4297. Bibcode : 2000PCCP .... 2.4293F . DOI : 10.1039 / b005247g .
- ^ «Циклопентадиен» . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Лерой Х. Шарпен и Виктор В. Лори (1965): "Структура циклопентадиена". Журнал химической физики , том 43, выпуск 8, страницы 2765-2766. DOI : 10,1063 / 1,1697207
- Перейти ↑ Hartwig, JF (2010). Химия органических переходных металлов: от связывания до катализа . Нью-Йорк, Нью-Йорк: Университетские научные книги. ISBN 978-1-891389-53-5.
- ^ a b Hönicke, Дитер; Фёдиш, Ринго; Клаус, Питер; Олсон, Майкл. «Циклопентадиен и циклопентен». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH.
- ^ Моффетт, Роберт Брюс (1962). «Циклопентадиен и 3-хлорциклопентен» . Органический синтез .; Сборник , 4 , с. 238
- ^ Streitwieser, A .; Хиткок, Швейцария ; Kosower, EM (1998). Введение в органическую химию (4-е изд.). Река Аппер Сэдл, штат Нью-Джерси: Prentice Hall.[ ISBN отсутствует ]
- ^ Левандовски, Брайан; Хоук, Кен (2015). «Теоретический анализ паттернов реакционной способности в реакциях Дильса – Альдера циклопентадиена, циклогексадиена и циклогептадиена с симметричными и несимметричными диенофилами». J. Org. Chem. 80 (7): 3530–3537. DOI : 10.1021 / acs.joc.5b00174 . PMID 25741891 .
- ^ Фишер, EO ; Ваверсик, Х. (1966). "Über Aromatenkomplexe von Metallen: LXXXVIII. Über Monomeres und Dimeres Dicyclopentadienylrhodium und Dicyclopentadienyliridium und Uber Ein Neues Verfahren Zur Darstellung Ungeladener Metall-Aromaten-Komplexe of VIII." Об ароматических комплексах металлов VIII. О мономерном и димерном дициклопентадиенилродии и дициклопентадиенилиридии и новом методе представления незаряженных металл-ароматических комплексов. J. Organomet. Chem. (на немецком). 5 (6): 559–567. DOI : 10.1016 / S0022-328X (00) 85160-8 .
- ^ Джиролами, GS; Раухфус, ТБ; Angelici, RJ (1999). Синтез и техника в неорганической химии . Милл-Вэлли, Калифорния: Научные книги университета. ISBN 0-935702-48-2.
- Перейти ↑ Jolly, WL (1970). Синтез и характеристика неорганических соединений . Энглвуд Клиффс, Нью-Джерси: Прентис-Холл. ISBN 0-13-879932-6.
- ^ Kolle, U .; Груб, Дж. (1985). «Перметилметаллоцен: 5. Реакции катионов декаметилрутения». J. Organomet. Chem. 289 (1): 133–139. DOI : 10.1016 / 0022-328X (85) 88034-7 .
- ^ Пакетт, Луизиана ; Wyvratt, MJ (1974). «Реакции Домино Дильса – Альдера. I. Приложения к быстрому построению полифузных циклопентаноидных систем». Варенье. Chem. Soc. 96 (14): 4671–4673. DOI : 10.1021 / ja00821a052 .
- ^ Райнерс, Маттис; Эрлих, Нико; Уолтер, Марк Д. (2018). Синтез 1,3,5- Три- трет- бутилциклопента-1,3-диена и его металлических комплексов Na {1,2,4- (Me 3 C) 3 C 5 H 2 } и Mg { η 5 -1, 2,4- (Me 3 C) 3 C 5 H 2 ) 2 . Неорганические синтезы. 37 . п. 199. DOI : 10.1002 / 9781119477822.ch8 .
Внешние ссылки [ править ]
- Международная карта химической безопасности 0857
- Карманный справочник NIOSH по химической опасности