 | |||
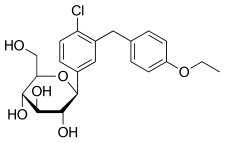 Проекция Хаворта (внизу) | |||
| |||
| Клинические данные | |||
|---|---|---|---|
| Произношение | / ˌ д æ р ə ɡ л ɪ е л oʊ г ɪ п / ДАФ -ə-glif- LOH -zin | ||
| Торговые наименования | Forxiga, Farxiga, Edistride, другие | ||
| Другие имена | БМС-512148; (1 S ) -1,5-ангидро-1- С - {4-хлор-3 - [(4-этоксифенил) метил] фенил} - D -glucitol | ||
| AHFS / Drugs.com | Монография | ||
| Данные лицензии |
| ||
Категория беременности |
| ||
| Пути администрирования | Внутрь ( таблетки ) | ||
| Класс препарата | Ингибитор ко-переносчика натрия-глюкозы 2 (SGLT2) | ||
| Код УВД | |||
| Легальное положение | |||
| Легальное положение | |||
| Фармакокинетические данные | |||
| Биодоступность | 78% (после дозы 10 мг) | ||
| Связывание с белками | ~ 91% | ||
| Метаболизм | UGT1A9 (основной), CYP (второстепенный) | ||
| Метаболиты | Дапаглифлозин 3- O- глюкуронид (неактивный) | ||
| Ликвидация Период полураспада | ~ 12,9 часов | ||
| Экскреция | Моча (75%), кал (21%) [2] | ||
| Идентификаторы | |||
| |||
| Количество CAS | |||
| PubChem CID |
| ||
| IUPHAR / BPS |
| ||
| DrugBank |
| ||
| ChemSpider |
| ||
| UNII |
| ||
| КЕГГ |
| ||
| ЧЭБИ |
| ||
| ЧЭМБЛ |
| ||
| CompTox Dashboard ( EPA ) |
| ||
| ECHA InfoCard | 100.167.331 | ||
| Химические и физические данные | |||
| Формула | C 21 H 25 Cl O 6 | ||
| Молярная масса | 408,88 г · моль -1 | ||
| 3D модель ( JSmol ) |
| ||
Улыбки
| |||
ИнЧИ
| |||
| | |||
Дапаглифлозин , продаваемый, в частности, под торговой маркой Farxiga , является лекарством, используемым для лечения диабета 2 типа и, с некоторыми ограничениями, диабета 1 типа . [2] Он также используется для лечения взрослых с сердечной недостаточностью с пониженной фракцией выброса, чтобы снизить риск смерти от сердечно-сосудистых заболеваний и госпитализации по поводу сердечной недостаточности. [3]
Наиболее частым побочным эффектом у людей с диабетом 2 типа является гипогликемия, особенно при использовании в сочетании с сульфонилмочевиной или инсулином. [4] Наиболее частым побочным эффектом у людей с диабетом 1 типа является генитальная инфекция, особенно у женщин, а частым побочным эффектом является диабетический кетоацидоз. [4] Он принадлежит к классу глифлозинов (ингибиторов SGLT2). [2]
Он был разработан Bristol-Myers Squibb в партнерстве с AstraZeneca . [ не подтверждено на теле ] В 2017 году это было 259-е место среди наиболее часто назначаемых лекарств в Соединенных Штатах, причем было выписано более миллиона рецептов. [5] [6]
Медицинское использование [ править ]
Дапаглифлозин используется вместе с диетой и физическими упражнениями для улучшения гликемического контроля у взрослых с диабетом 2 типа и для снижения риска госпитализации по поводу сердечной недостаточности среди взрослых с диабетом 2 типа и известными сердечно-сосудистыми заболеваниями или другими факторами риска. [7] [3] Он менее полезен, чем эмпаглифлозин . [8]
В США он также показан для лечения взрослых с сердечной недостаточностью с пониженной фракцией выброса, чтобы снизить риск смерти от сердечно-сосудистых заболеваний и госпитализации по поводу сердечной недостаточности. [3]
В Европейском союзе он показан взрослым для лечения недостаточно контролируемого сахарного диабета 2 типа в качестве дополнения к диете и упражнениям.
- в качестве монотерапии, когда метформин считается нецелесообразным из-за непереносимости. [4]
- в дополнение к другим лекарственным средствам для лечения сахарного диабета 2 типа. [4]
и для лечения недостаточно контролируемого сахарного диабета 1 типа в качестве дополнения к инсулину у пациентов с ИМТ ≥ 27 кг / м2, когда инсулин сам по себе не обеспечивает адекватный гликемический контроль, несмотря на оптимальную терапию инсулином. [4]
Одно исследование показало, что он не влияет на риск сердечных заболеваний или общий риск смерти у людей с диабетом. [9] Другое исследование показало, что при сердечной недостаточности со сниженной фракцией выброса дапаглифлозин снижает риск обострения сердечной недостаточности или прогрессирования до смерти от сердечно-сосудистых причин, независимо от диабетического статуса. [10]
Побочные эффекты [ править ]
Поскольку дапаглифлозин вызывает тяжелую глюкозурию (иногда до 70 граммов в день), он может привести к быстрой потере веса и усталости. Глюкоза действует как осмотическое диуретическое средство (этот эффект является причиной полиурии при диабете), что может привести к обезвоживанию . Повышенное количество глюкозы в моче также может усугубить инфекции, уже связанные с диабетом, особенно инфекции мочевыводящих путей и молочницу (кандидоз). В редких случаях применение препарата SGLT2, включая дапаглифлозин, связано с некротическим фасциитом промежности, также называемым гангреной Фурнье . [11]
Дапаглифлозин также связан с гипотензивными реакциями. Есть опасения, что это может увеличить риск диабетического кетоацидоза . [12]
Дапаглифлозин может вызвать обезвоживание, серьезные инфекции мочевыводящих путей и генитальные дрожжевые инфекции. [3] Пожилых людей, людей с проблемами почек, людей с низким кровяным давлением и людей, принимающих диуретики, следует обследовать на предмет их объема и функции почек. [3] Также следует обследовать людей с признаками и симптомами метаболического ацидоза или кетоацидоза (накопление кислоты в крови). [3] Дапаглифлозин может вызывать серьезные случаи некротического фасциита промежности (гангрена Фурнье) у людей с диабетом и низким уровнем сахара в крови в сочетании с инсулином. [3]
Чтобы снизить риск развития кетоацидоза (серьезного состояния, при котором организм вырабатывает высокие уровни кислот в крови, называемых кетонами) после операции, FDA одобрило изменения в информации о назначении лекарств от диабета с ингибиторами SGLT2, чтобы рекомендовать их временно прекратить перед плановой операцией. . Канаглифлозин, дапаглифлозин и эмпаглифлозин следует отменить по крайней мере за три дня до этого, а эртуглифлозин - по крайней мере за четыре дня до запланированной операции. [13]
Симптомы кетоацидоза включают тошноту, рвоту, боль в животе, усталость и затрудненное дыхание. [13]
Механизм действия [ править ]
Дапаглифлозин ингибирует подтип 2 белков транспорта натрия и глюкозы ( SGLT2 ), которые ответственны по крайней мере за 90% реабсорбции глюкозы в почках. Блокирование этого механизма переносчика вызывает вывод глюкозы из крови с мочой. [14] В клинических испытаниях дапаглифлозин снижал HbA 1c на 0,6 процентных пункта по сравнению с плацебо при добавлении к метформину. [15]
Что касается его защитного действия при сердечной недостаточности, то это в первую очередь связано с гемодинамическими эффектами, когда ингибиторы SGLT2 сильно уменьшают внутрисосудистый объем за счет осмотического диуреза и натрийуреза. Следовательно, это может привести к снижению преднагрузки и постнагрузки, тем самым уменьшая нагрузку на сердце и улучшая функцию левого желудочка. [16]
Избирательность [ править ]
IC 50 для SGLT2 составляет менее одной тысячной IC 50 для SGLT1 (1,1 по сравнению с 1390 нмоль / л), так что препарат не мешает абсорбции глюкозы кишечника. [17]
Имена [ править ]
Дапаглифлозина является Международное непатентованное название (МНН), [18] и названий США (USAN). [19]
Существует комбинированный препарат дапаглифлозин / метформин пролонгированного высвобождения с фиксированной дозой , который называется Xigduo XR. [20] [21] [22]
В июле 2016 года комбинация фиксированных доз саксаглиптина и дапаглифлозина была одобрена для медицинского применения в Европейском Союзе и продается под торговой маркой Qtern. [23] Комбинированный препарат был одобрен для медицинского применения в США в феврале 2017 года, где он продается под торговой маркой Qtern. [24] [25]
В мае 2019 года в США была одобрена комбинация фиксированных доз дапаглифлозина, саксаглиптина и метформина гидрохлорида в виде таблеток с пролонгированным высвобождением для улучшения гликемического контроля у взрослых с диабетом 2 типа при использовании в сочетании с диетой и упражнениями. FDA предоставило AstraZeneca одобрение Qternmet XR. [26] Комбинированный препарат был одобрен для использования в Европейском Союзе в ноябре 2019 года и продается под торговой маркой Qtrilmet. [27]
История [ править ]
В 2012 году Комитет по лекарственным средствам для человека (CHMP) Европейского агентства по лекарственным средствам (EMA) дал положительное заключение о препарате. [4]
Дапаглифлозин был признан эффективным в нескольких исследованиях с участием пациентов с диабетом 2 и 1 типа. [4] Основным показателем эффективности был уровень гликозилированного гемоглобина (HbA1c), который дает представление о том, насколько хорошо контролируется уровень глюкозы в крови. [4]
В двух исследованиях с участием 840 участников с диабетом 2 типа дапаглифлозин при использовании отдельно снижал уровни HbA1c на 0,66 процентных пункта больше, чем плацебо (фиктивное лечение) через 24 недели. [4] В четырех других исследованиях с участием 2370 участников добавление дапаглифлозина к другим лекарствам от диабета снизило уровень HbA1c на 0,54-0,68 процентных пункта больше, чем добавление плацебо через 24 недели. [4]
В исследовании с участием 814 участников с диабетом 2 типа дапаглифлозин, используемый в сочетании с метформином, был по крайней мере так же эффективен, как сульфонилмочевина (другой тип лекарств от диабета), используемая с метформином. [4] Обе комбинации снизили уровень HbA1c на 0,52 процентных пункта через 52 недели. [4]
В долгосрочном исследовании с участием более 17000 участников с диабетом 2 типа изучалось влияние дапаглифлозина на сердечно-сосудистые заболевания (сердце и кровообращение). [4] Исследование показало, что действие дапаглифлозина соответствовало эффектам других лекарств от диабета, которые также блокируют SGLT2. [4]
В двух исследованиях с участием 1648 участников с диабетом 1 типа, у которых уровень сахара в крови не контролировался достаточно хорошо с помощью одного инсулина, добавление 5 мг дапаглифлозина снизило уровень HbA1c через 24 часа на 0,37% и на 0,42% больше, чем добавление плацебо. [4]
Дапаглифлозин был одобрен для медицинского применения в Европейском Союзе в ноябре 2012 года. [4] Он продается в ряде европейских стран. [28]
Дапаглифлозин был одобрен для медицинского применения в США в январе 2014 г. [29]
В 2020 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) расширило показания для дапаглифлозина, включив в него лечение взрослых с сердечной недостаточностью с пониженной фракцией выброса, чтобы снизить риск сердечно-сосудистой смерти и госпитализации по поводу сердечной недостаточности. [3] Это первые в этом классе препаратов, ингибиторы ко-транспортера натрия-глюкозы 2 (SGLT2), которые были одобрены для лечения взрослых с сердечной недостаточностью II-IV функционального класса Нью-Йоркской кардиологической ассоциации с пониженной фракцией выброса. [3]
В клинических испытаниях было показано, что дапаглифлозин улучшает выживаемость и снижает потребность в госпитализации у взрослых с сердечной недостаточностью со сниженной фракцией выброса. [3] Безопасность и эффективность дапаглифлозина оценивались в рандомизированном двойном слепом плацебо-контролируемом исследовании с участием 4744 человек. [3] Средний возраст участников составлял 66 лет, и мужчин было больше (77%), чем женщин. [3] Чтобы определить эффективность препарата, исследователи изучили частоту случаев смерти от сердечно-сосудистых заболеваний, госпитализаций по поводу сердечной недостаточности и срочных посещений пациентов с сердечной недостаточностью. [3] Участников случайным образом распределили для получения ежедневной дозы 10 миллиграммов дапаглифлозина или плацебо (неактивное лечение). [3]Примерно через 18 месяцев у людей, получавших дапаглифлозин, было меньше случаев смерти от сердечно-сосудистых заболеваний, госпитализаций по поводу сердечной недостаточности и срочных посещений по поводу сердечной недостаточности, чем у тех, кто получал плацебо. [3]
В июле 2020 года FDA предоставило компании AstraZeneca статус ускоренного режима в США для разработки дапаглифлозина для снижения риска госпитализации по поводу сердечной недостаточности или смерти от сердечно-сосудистых заболеваний у взрослых после сердечного приступа . [30]
В августе 2020 года сообщалось, что подробные результаты исследования фазы III DAPA-CKD показали, что препарат AstraZeneca FARXIGA® (дапаглифлозин) в дополнение к стандартному лечению снижает совокупный показатель ухудшения функции почек или риска сердечно-сосудистых (CV) или почечных заболеваний. смерть на 39% по сравнению с плацебо (p <0,0001) у пациентов с хронической болезнью почек (ХБП) 2-4 стадии и повышенной экскрецией альбумина с мочой. Результаты были стабильными у пациентов с диабетом 2 типа (T2D) и без него [31]
Ссылки [ править ]
- ^ a b «Дапаглифлозин (Фарксига) Использование во время беременности» . Drugs.com . 30 августа 2018 . Дата обращения 5 мая 2020 .
- ^ a b c «Фарксига-дапаглифлозин таблетка, покрытая пленочной оболочкой» . DailyMed . 3 февраля 2020 . Дата обращения 5 мая 2020 .
- ^ a b c d e f g h i j k l m n o «FDA одобряет новый метод лечения сердечной недостаточности» . США пищевых продуктов и медикаментов (FDA) (Пресс - релиз). 5 мая 2020 . Дата обращения 5 мая 2020 .
 Эта статья включает текст из этого источника, который находится в общественном достоянии .
Эта статья включает текст из этого источника, который находится в общественном достоянии . - ^ Б с д е е г ч я J к л м п о р «Forxiga EPAR» . Европейское агентство по лекарственным средствам (EMA) . Дата обращения 17 февраля 2020 .Текст был скопирован из этого источника © European Medicines Agency. Воспроизведение разрешено при условии указания источника.
- ^ «Топ 300 2020» . ClinCalc . Проверено 11 апреля 2020 .
- ^ «Дапаглифлозин - Статистика употребления наркотиков» . ClinCalc . Проверено 11 апреля 2020 .
- ^ «FDA одобряет Farxiga для лечения диабета 2 типа» (пресс-релиз). США пищевых продуктов и медикаментов (FDA). 8 января 2014. Архивированы из оригинала 9 января 2014 года . Проверено 15 ноября +2016 .
 Эта статья включает текст из этого источника, который находится в общественном достоянии .
Эта статья включает текст из этого источника, который находится в общественном достоянии . - ^ Zelniker TA, Wiviott SD, Raz I, et al. (Январь 2019). «Ингибиторы SGLT2 для первичной и вторичной профилактики сердечно-сосудистых и почечных исходов при диабете 2 типа: систематический обзор и метаанализ исследований сердечно-сосудистых исходов». Ланцет . 393 (10166): 31–9. DOI : 10.1016 / S0140-6736 (18) 32590-X . PMID 30424892 . S2CID 53277899 .
Однако у пациентов с атеросклеротическим сердечно-сосудистым заболеванием влияние эмпаглифлозина на сердечно-сосудистую смерть было более выраженным, чем у канаглифлозина или дапаглифлозина.
- ^ «Диабет 2 типа. Сердечно-сосудистая оценка дапаглифлозина: нет прогресса» . Prescrire International . 29 (211): 23 января 2020 . Дата обращения 2 февраля 2020 .
- ^ МакМюррей JJ, Соломон С.Д., Inzucchi SE и др. (Ноябрь 2019 г.). «Дапаглифлозин у больных с сердечной недостаточностью и пониженной фракцией выброса» . Медицинский журнал Новой Англии . 381 (21): 1995–2008. DOI : 10.1056 / NEJMoa1911303 . PMID 31535829 .
- ^ «FDA предупреждает о редких случаях серьезной инфекции области гениталий ингибиторами SGLT2 от диабета» . США пищевых продуктов и медикаментов (FDA). 9 февраля 2019.
 Эта статья включает текст из этого источника, который находится в общественном достоянии .
Эта статья включает текст из этого источника, который находится в общественном достоянии . - ^ «Ингибиторы SGLT2: Сообщение о безопасности лекарств - FDA предупреждает, что лекарства могут привести к серьезным последствиям слишком большого количества кислоты в крови» . США пищевых продуктов и медикаментов (FDA). 15 мая 2015. Архивировано из оригинала 27 октября 2016 года . Проверено 15 ноября +2016 .
- ^ a b «FDA пересматривает этикетки ингибиторов SGLT2 для диабета, чтобы включить предупреждение» . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США . 19 марта 2020 . Дата обращения 6 июня 2020 .
 Эта статья включает текст из этого источника, который находится в общественном достоянии .
Эта статья включает текст из этого источника, который находится в общественном достоянии . - ^ "Науки о жизни - Clarivate" . Clarivate . Архивировано из оригинала 5 ноября 2007 года.
- ^ "UEndocrine: Интернет-эндокринологическое сообщество" . uendocrine.com . Архивировано из оригинала 5 февраля 2013 года .
- ^ Lan NS, Fegan PG, Yeap BB, Dwivedi G (октябрь 2019). «Влияние ингибиторов натрий-глюкозного котранспортера 2 на функцию левого желудочка: текущие данные и будущие направления» . ESC Heart Fail . 6 (5): 927–935. DOI : 10.1002 / ehf2.12505 . PMC 6816235 . PMID 31400090 .
- ^ Schubert-Zsilavecz, М, Wurglics, M, Neue Арцнаймиттель 2008/2009
- ^ «Международные непатентованные наименования фармацевтических субстанций (МНН). Рекомендуемые международные непатентованные наименования: Список 59» (PDF) . Всемирная организация здоровья. 2008. с. 50 . Проверено 15 ноября +2016 .
- ^ «Заявление о непатентованном названии, принятое Советом USAN» (PDF) . Американская медицинская ассоциация. Архивировано из оригинального (PDF) 7 февраля 2012 года . Проверено 15 ноября +2016 .
- ^ «US FDA одобряет ежедневные таблетки Xigduo XR для взрослых с диабетом 2 типа» . AstraZeneca. 30 октября 2014 г.
- ^ "Xigduo XR (дапаглифлозин и метформин HCl) таблетки с расширенной высвобождением" . США пищевых продуктов и медикаментов (FDA) . 7 апреля 2015 . Дата обращения 5 мая 2020 .
- ^ «Xigduo XR-дапаглифлозин и метформин гидрохлорид таблетка, покрытая пленкой, с пролонгированным высвобождением» . DailyMed . 3 февраля 2020 . Дата обращения 5 мая 2020 .
- ^ "Qtern EPAR" . Европейское агентство по лекарственным средствам (EMA) . Дата обращения 7 мая 2020 .
- ^ «Пакет одобрения лекарственных средств: Qtern (дапаглифлозин и саксаглиптин)» . США пищевых продуктов и медикаментов (FDA) . 10 октября 2018 . Дата обращения 8 мая 2020 .
- ^ «Qtern-дапаглифлозин и саксаглиптин в таблетках, покрытых пленочной оболочкой» . DailyMed . 24 января 2020 . Дата обращения 17 февраля 2020 .
- ^ «Пакет одобрения лекарств: Qternmet XR» . США пищевых продуктов и медикаментов (FDA) . 27 января 2020 . Дата обращения 17 февраля 2020 .
- ^ "Qtrilmet EPAR" . Европейское агентство по лекарственным средствам (EMA) . Проверено 30 марта 2020 .
- ^ "Forxiga" . Drugs.com . 4 мая 2020 . Дата обращения 5 мая 2020 .
- ^ «Пакет одобрения лекарственных средств: Фарксига (дапаглифлозин) Таблетки NDA № 202293» . США пищевых продуктов и медикаментов (FDA) . 24 декабря 1999 . Дата обращения 5 мая 2020 .
- ^ «FARXIGA получила ускоренное обозначение в США для сердечной недостаточности после острого инфаркта миокарда с использованием инновационного дизайна исследования на основе реестра» . www.businesswire.com . 16 июля 2020 . Дата обращения 20 июля 2020 .
- ^ https://www.businesswire.com/news/home/20200830005009/en/FARXIGA-Demonstrated-Unprecedented-Reduction-Risk-Kidney-Failure
Внешние ссылки [ править ]
- «Дапаглифлозин» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- «Смесь дапаглифлозина с гидрохлоридом метформина» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- «Смесь дапаглифлозина с саксаглиптином» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
