G-белок
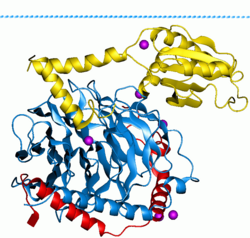
G-белки , также известные как белки, связывающие гуаниновые нуклеотиды , представляют собой семейство белков , которые действуют как молекулярные переключатели внутри клеток и участвуют в передаче сигналов от различных раздражителей снаружи клетки внутрь ее. Их активность регулируется факторами, которые контролируют их способность связываться и гидролизовать гуанозинтрифосфат (ГТФ) до гуанозиндифосфата (ГДФ). Когда они связаны с GTP, они «включены», а когда они связаны с GDP, они «выключены». G-белки принадлежат к большей группе ферментов, называемых GTPases .
Существует два класса G-белков. Первые функционируют как мономерные малые ГТФазы (малые G-белки), тогда как вторые функционируют как гетеротримерные комплексы G-белков . Последний класс комплексов состоит из альфа (α), бета (β) и гамма (γ) субъединиц . [1] Кроме того, бета- и гамма-субъединицы могут образовывать стабильный димерный комплекс, называемый бета-гамма-комплексом . [2]
Гетеротримерные G-белки, расположенные внутри клетки, активируются рецепторами, связанными с G-белками (GPCR), которые охватывают клеточную мембрану. [3] Сигнальные молекулы связываются с доменом GPCR, расположенным вне клетки, а внутриклеточный домен GPCR затем, в свою очередь, активирует определенный G-белок. Также было показано, что некоторые GPCR в активном состоянии «предварительно связаны» с G-белками. [4] Белок G активирует каскад дальнейших сигнальных событий, что в конечном итоге приводит к изменению функции клетки. Рецептор, связанный с G-белком, и G-белки, работающие вместе, передают сигналы от многих гормонов , нейротрансмиттеров и других сигнальных факторов. [5] G-белки регулируют метаболические ферменты., ионные каналы , транспортные белки и другие части клеточного механизма, контролирующие транскрипцию , подвижность , сократимость и секрецию , которые, в свою очередь, регулируют различные системные функции, такие как эмбриональное развитие , обучение и память, а также гомеостаз . [6]
История
G-белки были открыты, когда Альфред Г. Гилман и Мартин Родбелл исследовали стимуляцию клеток адреналином . Они обнаружили, что когда адреналин связывается с рецептором, рецептор не стимулирует ферменты (внутри клетки) напрямую. Вместо этого рецептор стимулирует G-белок, который затем стимулирует фермент. Примером может служить аденилатциклаза , которая продуцирует циклический АМФ вторичного мессенджера . [7] За это открытие они получили Нобелевскую премию по физиологии и медицине 1994 года . [8]
Нобелевские премии были присуждены за многие аспекты передачи сигналов G-белками и GPCR. К ним относятся антагонисты рецепторов , нейротрансмиттеры , обратный захват нейротрансмиттеров , рецепторы, связанные с G- белками, G-белки, вторичные мессенджеры , ферменты, запускающие фосфорилирование белков в ответ на цАМФ , и последующие метаболические процессы, такие как гликогенолиз .
Яркие примеры включают (в хронологическом порядке награждения):
- Нобелевская премия по физиологии и медицине 1947 года Карлу Кори , Герти Кори и Бернардо Хуссей за открытие того, как гликоген расщепляется до глюкозы и повторно синтезируется в организме для использования в качестве хранилища и источника энергии. Гликогенолиз стимулируется многочисленными гормонами и нейротрансмиттерами , включая адреналин .
- Нобелевская премия 1970 года по физиологии и медицине Юлиусу Аксельроду , Бернарду Кацу и Ульфу фон Эйлеру за их работу по высвобождению и обратному захвату нейротрансмиттеров .
- В 1971 году Нобелевская премия по физиологии и медицине была присуждена Эрлу Сазерленду за открытие ключевой роли аденилатциклазы , которая производит вторичный мессенджер циклического АМФ . [7]
- Нобелевская премия 1988 года по физиологии и медицине Джорджу Х. Хитчингсу , сэру Джеймсу Блэку и Гертруде Элион «за открытия важных принципов медикаментозного лечения», нацеленного на GPCR.
- Нобелевская премия 1992 года по физиологии и медицине Эдвину Г. Кребсу и Эдмонду Х. Фишеру за описание того, как обратимое фосфорилирование работает как переключатель для активации белков и регулирования различных клеточных процессов, включая гликогенолиз . [9]
- Нобелевская премия 1994 года по физиологии и медицине Альфреду Г. Гилману и Мартину Родбеллу за открытие «G-белков и роли этих белков в передаче сигнала в клетках». [10]
- Нобелевская премия 2000 года по физиологии и медицине Эрику Канделу , Арвиду Карлссону и Полу Грингарду за исследования нейротрансмиттеров , таких как дофамин , которые действуют через GPCR.
- Нобелевская премия по физиологии и медицине 2004 года Ричарду Акселю и Линде Б. Бак за их работу над обонятельными рецепторами , связанными с G-белком . [11]
- Нобелевская премия по химии 2012 года Брайану Кобилке и Роберту Лефковицу за их работу над функцией GPCR. [12]
Функция
G-белки являются важными молекулами, передающими сигнал в клетках. «Нарушение работы сигнальных путей GPCR [рецептора, связанного с G-белком] связано со многими заболеваниями, такими как диабет , слепота, аллергии, депрессия, сердечно-сосудистые дефекты и некоторые формы рака . По оценкам, около 30% современных лекарств клеточными мишенями являются GPCR». [13] Геном человека кодирует примерно 800 [14] рецепторов, связанных с G-белком , которые обнаруживают фотоны света, гормоны, факторы роста, лекарства и другие эндогенные лиганды . Приблизительно 150 GPCR, обнаруженных в геноме человека, до сих пор выполняют неизвестные функции.
В то время как G-белки активируются рецепторами, связанными с G-белками , они инактивируются белками RGS (от «Регулятор передачи сигналов G-белка»). Рецепторы стимулируют связывание GTP (включение G-белка). Белки RGS стимулируют гидролиз GTP (создавая GDP, тем самым отключая G-белок).
Разнообразие
Все эукариоты используют G-белки для передачи сигналов и развили большое разнообразие G-белков. Например, люди кодируют 18 различных белков Gα , 5 белков Gβ и 12 белков Gγ . [15]
Сигнализация
G-белок может относиться к двум различным семействам белков. Гетеротримерные G-белки , иногда называемые «большими» G-белками, активируются рецепторами, связанными с G-белками, и состоят из альфа (α), бета (β) и гамма (γ) субъединиц . «Малые» G-белки (20–25 кДа) принадлежат к суперсемейству Ras малых ГТФаз . Эти белки гомологичны субъединице альфа (α), обнаруженной в гетеротримерах, но на самом деле являются мономерными, состоящими только из одной единицы. Однако, как и их более крупные родственники, они также связывают GTP и GDP и участвуют в передаче сигнала .
гетеротримерный
Различные типы гетеротримерных G-белков имеют общий механизм. Они активируются в ответ на конформационные изменения в GPCR, заменяя GDP на GTP и диссоциируя, чтобы активировать другие белки в конкретном пути передачи сигнала. [16] Однако конкретные механизмы различаются между типами белков.
Механизм
G-белки, активируемые рецепторами, связаны с внутренней поверхностью клеточной мембраны . Они состоят из G α и тесно связанных субъединиц G βγ . Существует много классов субъединиц G α : G s α (G стимулирующие), G i α (G ингибирующие), G o α (другие G), G q/11 α и G 12/13 α являются некоторыми примерами. Они ведут себя по-разному при распознавании эффекторной молекулы, но имеют сходный механизм активации.
Активация
Когда лиганд активирует рецептор, связанный с G-белком , он индуцирует конформационные изменения в рецепторе, которые позволяют рецептору функционировать как фактор обмена гуаниновых нуклеотидов (GEF), который обменивает GDP на GTP. GTP (или GDP) связан с субъединицей G α с традиционной точки зрения активации гетеротримерных GPCR. Этот обмен запускает диссоциацию субъединицы G α (которая связана с GTP) от димера G βγ и рецептора в целом. Однако начинают приниматься модели, предполагающие молекулярную перестройку, реорганизацию и предварительное комплексообразование эффекторных молекул. [4] [18] [19] Оба G αЗатем -GTP и G βγ могут активировать различные сигнальные каскады (или пути вторичных мессенджеров ) и эффекторные белки, в то время как рецептор способен активировать следующий G-белок. [20]
Прекращение
Субъединица G α в конечном итоге гидролизует присоединенный GTP до GDP за счет присущей ей ферментативной активности, позволяя ей повторно ассоциироваться с G βγ и запуская новый цикл. Группа белков, называемых регуляторами передачи сигналов G-белка (RGS), действуют как белки, активирующие GTPase (GAP), специфичны для субъединиц Gα . Эти белки ускоряют гидролиз GTP до GDP, тем самым прерывая трансдуцированный сигнал. В некоторых случаях сам эффектор может обладать внутренней активностью GAP, которая затем может помочь дезактивировать путь. Это верно в случае фосфолипазы С -бета, которая обладает GAP-активностью в пределах своей активности.С-концевая область. Это альтернативная форма регуляции субъединицы Gα. Такие GαGAP не имеют каталитических остатков (специфических аминокислотных последовательностей) для активации белка Gα . Вместо этого они работают, снижая необходимую энергию активации для протекания реакции. [21]
Конкретные механизмы
G αs
Gαs активирует цАМФ - зависимый путь , стимулируя выработку циклического АМФ (цАМФ) из АТФ . Это достигается путем прямой стимуляции ассоциированного с мембраной фермента аденилатциклазы . цАМФ затем может действовать как вторичный мессенджер, который взаимодействует с протеинкиназой А (ПКА) и активирует ее. PKA может фосфорилировать множество нижестоящих мишеней.
Зависимый от цАМФ путь используется в качестве пути передачи сигнала для многих гормонов, включая:
- АДГ – способствует задержке воды почками (создается крупноклеточными нейросекреторными клетками задней доли гипофиза ) .
- GHRH – стимулирует синтез и высвобождение GH ( соматотропные клетки передней доли гипофиза )
- GHIH - ингибирует синтез и высвобождение GH (соматотропные клетки передней доли гипофиза)
- CRH – стимулирует синтез и высвобождение АКТГ (передняя доля гипофиза).
- АКТГ – стимулирует синтез и высвобождение кортизола ( пучковая зона коры надпочечников в надпочечниках)
- ТТГ – стимулирует синтез и высвобождение большей части Т4 (щитовидная железа) .
- ЛГ – стимулирует созревание фолликулов и овуляцию у женщин; или производство тестостерона и сперматогенез у мужчин
- ФСГ – стимулирует развитие фолликулов у женщин; или сперматогенез у мужчин
- ПТГ – повышает уровень кальция в крови. Это достигается через рецептор паратиреоидного гормона 1 (PTH1) в почках и костях или через рецептор паратиреоидного гормона 2 (PTH2) в центральной нервной системе и головном мозге, а также в костях и почках.
- Кальцитонин – снижает уровень кальция в крови (через кальцитониновые рецепторы в кишечнике, костях, почках и головном мозге).
- Глюкагон – стимулирует расщепление гликогена в печени.
- ХГЧ – способствует дифференцировке клеток и потенциально участвует в апоптозе . [22]
- Эпинефрин – высвобождается мозговым веществом надпочечников во время голодания, когда организм находится под метаболическим принуждением. Он стимулирует гликогенолиз , в дополнение к действию глюкагона .
G αi
G αi ингибирует продукцию цАМФ из АТФ. например соматостатин, простагландины
G αq/11
G αq/11 стимулирует связанную с мембраной фосфолипазу С бета, которая затем расщепляет PIP 2 (минорный мембранный фосфоинозитол ) на два вторичных мессенджера, IP3 и диацилглицерин (DAG). Инозитол-фосфолипид-зависимый путь используется в качестве пути передачи сигнала для многих гормонов, включая:
- АДГ ( вазопрессин /АВП) – индуцирует синтез и высвобождение глюкокортикоидов ( пучковая зона коры надпочечников ); Вызывает сужение сосудов (клетки V1 задней доли гипофиза )
- ТРГ – индуцирует синтез и высвобождение ТТГ ( передняя доля гипофиза ) .
- ТТГ – индуцирует синтез и высвобождение небольшого количества Т4 ( щитовидная железа ) .
- Ангиотензин II – индуцирует синтез и высвобождение альдостерона ( клубочковой зоны коры надпочечников в почках)
- ГнРГ – индуцирует синтез и высвобождение ФСГ и ЛГ (передняя доля гипофиза).
G α12/13
- G α12/13 участвуют в передаче сигналов ГТФаз семейства Rho (см. семейство ГТФаз Rho ). Это происходит через суперсемейство RhoGEF, включающее домен RhoGEF структур белков). Они участвуют в контроле ремоделирования клеточного цитоскелета и, таким образом, в регуляции миграции клеток.
G β
- Комплексы G βγ иногда также выполняют активные функции. Примеры включают связывание и активацию связанных с G-белком внутренних выпрямляющих калиевых каналов .
Малые ГТФазы
Малые GTPазы, также известные как малые G-белки, аналогичным образом связывают GTP и GDP и участвуют в передаче сигнала . Эти белки гомологичны субъединице альфа (α), обнаруженной в гетеротримерах, но существуют в виде мономеров. Это небольшие (от 20 до 25 кДа) белки , которые связываются с гуанозинтрифосфатом ( ГТФ ). Это семейство белков гомологично Ras GTPases и также называется суперсемейством Ras GTPases .
Липидация
Чтобы ассоциироваться с внутренним листком [ необходимо уточнение ] плазматической мембраны, многие G-белки и малые ГТФазы липидируются, то есть ковалентно модифицируются липидными удлинениями. Они могут быть миристоилированы , пальмитоилированы или пренилированы .
использованная литература
- ↑ Гуровиц Э. Х., Мельник Дж. М., Чен Ю. Дж., Курос-Мехр Х., Саймон М. И., Сидзуя Х. (апрель 2000 г.). «Геномная характеристика генов альфа-, бета- и гамма-субъединиц гетеротримерного G-белка человека» . Исследования ДНК . 7 (2): 111–20. doi : 10.1093/dnares/7.2.111 . PMID 10819326 .
- ^ Clapham DE, Neer EJ (1997). «Субъединицы бета-гамма белка G». Ежегодный обзор фармакологии и токсикологии . 37 : 167–203. doi : 10.1146/annurev.pharmtox.37.1.167 . PMID 9131251 .
- ^ «Семь трансмембранных рецепторов: Роберт Лефковиц» . 9 сентября 2012 г. . Проверено 11 июля 2016 г.
- ^ a b Цинь К., Донг С., Ву Г., Ламберт Н.А. (август 2011 г.). «Предварительная сборка рецепторов, связанных с G (q), и гетеротримеров G (q) в неактивном состоянии» . Природа Химическая Биология . 7 (10): 740–7. doi : 10.1038/nchembio.642 . ПВК 3177959 . PMID 21873996 .
- ^ Рис Дж., Китай (2002). Биология . Сан-Франциско: Бенджамин Каммингс. ISBN 0-8053-6624-5.
- ^ Невес С.Р., Рам П.Т., Айенгар Р. (май 2002 г.). «Пути G-белка». Наука . 296 (5573): 1636–169. Бибкод : 2002Sci...296.1636N . doi : 10.1126/science.1071550 . PMID 12040175 . S2CID 20136388 .
- ^ a b Нобелевская премия по физиологии и медицине 1994 г., иллюстрированная лекция.
- ↑ Пресс-релиз: Нобелевская ассамблея Каролинского института решила присудить Нобелевскую премию по физиологии и медицине за 1994 год совместно Альфреду Г. Гилману и Мартину Родбеллу за их открытие «G-белков и роли этих белков в передаче сигнала в клетки». 10 октября 1994 г.
- ^ «Пресс-релиз Нобелевской премии по физиологии и медицине 1992 г.» . Нобелевская ассамблея Каролинского института . Проверено 21 августа 2013 г.
- ^ Пресс-релиз
- ^ «Пресс-релиз: Нобелевская премия по физиологии и медицине 2004 г.» . Nobelprize.org . Проверено 8 ноября 2012 г.
- ↑ Шведская королевская академия наук (10 октября 2012 г.). «Нобелевская премия по химии 2012 г. Роберт Дж. Лефковиц, Брайан К. Кобилка» . Проверено 10 октября 2012 г.
- ↑ Bosch DE, Сидеровски Д.П. (март 2013 г.). «Передача сигналов G-белка у паразита Entamoeba histolytica» . Экспериментальная и молекулярная медицина . 45 (1038): e15. doi : 10.1038/emm.2013.30 . ПВК 3641396 . PMID 23519208 .
- ↑ Baltoumas FA, Theodoropoulou MC, Hamodrakas SJ (июнь 2013 г.). «Взаимодействия α-субъединиц гетеротримерных G-белков с GPCR, эффекторами и белками RGS: критический обзор и анализ взаимодействующих поверхностей, конформационных сдвигов, структурного разнообразия и электростатических потенциалов». Журнал структурной биологии . 182 (3): 209–18. doi : 10.1016/j.jsb.2013.03.004 . PMID 23523730 .
- ^ a b Сыроваткина В., Алегре К.О., Дей Р., Хуанг XY (сентябрь 2016 г.). «Регуляция, передача сигналов и физиологические функции G-белков» . Журнал молекулярной биологии . 428 (19): 3850–68. doi : 10.1016/j.jmb.2016.08.002 . ПМС 5023507 . PMID 27515397 .
- ^ Лим, Венделл (2015). Клеточная передача сигналов: принципы и механизмы . Брюс Майер, Т. Поусон. Нью-Йорк. ISBN 978-0-8153-4244-1. OCLC 868641565 .
- ^ Стюарт, Адель; Фишер, Рори А. (2015). Прогресс в молекулярной биологии и трансляционной науке . 133 . Эльзевир. стр. 1–11. doi : 10.1016/bs.pmbts.2015.03.002 . ISBN 9780128029381. PMID 26123299 .
- ↑ Digby GJ, Lober RM, Sethi PR, Lambert NA (ноябрь 2006 г.) . «Некоторые гетеротримеры G-белка физически диссоциируют в живых клетках» . Труды Национальной академии наук Соединенных Штатов Америки . 103 (47): 17789–94. Бибкод : 2006PNAS..10317789D . doi : 10.1073/pnas.0607116103 . ПВК 1693825 . PMID 17095603 .
- ↑ Хафизов К., Латтанзи Г., Карлони П. (июнь 2009 г.). «Неактивные и активные формы G-белка исследованы методами моделирования». Белки . 75 (4): 919–30. doi : 10.1002/прот.22303 . PMID 19089952 . S2CID 23909821 .
- ↑ Yuen JW, Poon LS, Chan AS, Yu FW, Lo RK, Wong YH (июнь 2010 г.). «Активация STAT3 специфическими субъединицами Galpha и несколькими димерами Gbetagamma». Международный журнал биохимии и клеточной биологии . 42 (6): 1052–1059. doi : 10.1016/j.biocel.2010.03.017 . PMID 20348012 .
- ^ Sprang SR, Chen Z, Du X (2007). «Структурные основы эффекторной регуляции и прекращения сигнала в гетеротримерных белках Gα». Структурные основы эффекторной регуляции и терминации сигнала в гетеротримерных Galpha белках . Достижения в области химии белков. 74 . стр. 1–65. doi : 10.1016/S0065-3233(07)74001-9 . ISBN 978-0-12-034288-4. PMID 17854654 .
- ^ Коул Л.А. (август 2010 г.). «Биологические функции ХГЧ и родственных ХГЧ молекул» . Репродуктивная биология и эндокринология . 8 (1): 102. doi : 10.1186/1477-7827-8-102 . ПВК 2936313 . PMID 20735820 .
внешняя ссылка
- GTP-связывающие белки в предметных медицинских рубриках Национальной медицинской библиотеки США (MeSH)
- G-белки
- Белки периферической мембраны
- Сотовая сигнализация
- Преобразование сигнала
- ЕС 3.6